Therapeutisch proces
C.1 Voorlichting en advies
Aanbeveling Bied patiënten met RA voorlichting en advies op maat ter ondersteuning van effectief zelfmanagement en optimalisering van gezondheid en welbevinden.
Toevoeging De therapeut geeft informatie en advies over de aandoening en de mogelijke gevolgen ervan, het belang van bewegen en een gezonde leefstijl (waaronder het verminderen van stress en terugdringen van vermoeidheid en de manier waarop deze leefstijl kan worden verkregen en behouden) en de behandelmogelijkheden.
Aan de orde komen:
- het gunstige effect van lichamelijke activiteit en individueel afgestemde oefeningen (voor verbetering van de spierkracht en het aerobe vermogen) op het fysiek en mentaal functioneren;
- het feit dat lichamelijke activiteit geen nadelige effecten heeft op ziekteactiviteit en radiologische schade;
- het preventieve en curatieve effect van voldoende lichamelijke activiteit en het beperken van sedentair gedrag bij RA in verband met het verhoogde cardiovasculaire risico bij deze ziekte;
- het belang van integratie van individuele oefeningen en/of lichamelijke activiteiten in het dagelijks leven om deze oefeningen en activiteiten vol te houden.
Voorlichting en advies wordt mondeling gegeven en schriftelijk en/of digitaal ondersteund, afgestemd op de wensen, voorkeuren en gezondheidsvaardigheden van de patiënt. De patiënt kan worden verwezen naar verschillende (digitale) informatiebronnen, als aanvulling op wat de therapeut aan voorlichting en advies aanbiedt:
Onderbouwing
Noot 9 Voorlichting en advies
Uitgangsvraag
Wat zijn de aanbevelingen voor voorlichting bij patiënten met RA?
Conclusie vanuit de literatuurstudie
In de internationale richtlijn met betrekking tot voorlichting bij patiënten met inflammatoire reumatische aandoeningen van de ‘European League Against Rheumatism’ (EULAR) zijn de volgende aanbevelingen geformuleerd:[1]
- Voorlichting is een interactief leerproces dat is ontwikkeld om de patiënt te ondersteunen en in staat te stellen hun leven met de aandoening te managen en hun gezondheid en welbevinden te optimaliseren.
- Communicatie en gezamenlijke besluitvorming van de patiënt en de zorgverlener zijn essentieel voor effectieve voorlichting.
- Voorlichting dient integraal onderdeel uit te maken van de geboden zorg om de patiëntbetrokkenheid bij het ziektemanagement en een gezonde leefstijl te bevorderen.
- Elke patiënt dient (toegang tot) voorlichting te krijgen gedurende het gehele ziekteproces, maar in ieder geval bij de diagnosestelling, bij wijzigingen in de medicamenteuze behandeling en bij lichamelijke en/of mentale problemen.
- De inhoud en vorm van voorlichting dient individueel afgestemd te worden op de behoefte van de pa-tiënt.
- Voorlichting dient face-to-face of online, individueel en/of in groepssessies te worden aangeboden, eventueel gecomplementeerd met telefonisch contact en informatie op papier of via multimedia.
- Voorlichtingsprogramma’s dienen gebaseerd te zijn op theoretische raamwerken en dienen evidence-based te zijn, bijvoorbeeld zelfmanagement, cognitieve gedragstherapie en stressmanagement.
- De effectiviteit van voorlichting dient te worden geëvalueerd en de gekozen uitkomstmaten dienen aan te sluiten bij het doel van de voorlichting.
- Voorlichting dient gegeven te worden door een competente zorgverlener en/of getrainde ervaringsdeskundigen, indien van toepassing in een multidisciplinair team.
- Zorgverleners die voorlichting geven, dienen toegang te hebben tot en gebruik te maken van specifieke deskundigheidsbevordering, om zodoende over de nodige kennis en vaardigheden te beschikken.
Bij het bevorderen van zelfmanagement is voorlichting en advies over een gezonde leefstijl van groot belang. Een gezonde leefstijl heeft algehele positieve gezondheidseffecten en is bovendien relevant in het kader van het verhoogde cardiovasculair risico bij patiënten met RA, en moet op grond daarvan aandacht krijgen bij de voorlichting aan deze patiëntengroep.[2,3]
Van bewijs naar aanbeveling
Op basis van de gevonden literatuur heeft de werkgroep een aanbeveling geformuleerd aangaande voorlichting en advies.
Aanbeveling
Bied patiënten met RA voorlichting en advies op maat ter ondersteuning van effectief zelfmanagement en optimalisering van gezondheid en welbevinden.
Complete uitgangsvraag volgens PICO
Wordt voorlichting en advies (I) al dan niet in aanvulling op de oefentherapeutische interventie aanbevolen bij patiënten met RA (P) ter bevordering van effectief zelfmanagement en een gezonde leefstijl (O).
Zoekstrategie
Er is door het KNGF op 3 maart 2017 een zoekactie uitgevoerd naar studies die beschrijven welke voorlichting fysiotherapeuten patiënten met RA moeten bieden om zelfmanagement te bevorderen.
Gevonden literatuur
In totaal zijn 755 referenties gevonden. Er is uiteindelijk 1 internationale EULAR-richtlijn geselecteerd voor de beantwoording van de uitgangsvraag.[1]
Beschrijving studies
In de EULAR-richtlijn is het bewijs t/m 2015 samengevat.[1] In deze richtlijn zijn 115 studies geïncludeerd, bestaande uit 11 systematische reviews of meta-analyses, 36 gerandomiseerde studies (gerapporteerd in 44 studies), zeven gecontroleerde studies, negen pre-post-teststudies, 23 cross-sectionele studies en 21 kwalitatieve studies. Op basis van deze studies zijn twee overkoepelende principes en acht specifieke aanbevelingen met betrekking tot voorlichting bij patiënten met inflammatoire reumatische aandoeningen geformuleerd. De EULAR-richtlijn is gebaseerd op literatuur over verschillende typen programma’s: educatieve programma’s (32 studies), zelfmanagementprogramma’s (7 studies), cognitieve gedragstherapie (9 studies) en stressmanagementprogramma’s (6 studies). Daarnaast zijn er drie systematische reviews met betrekking tot deze verschillende voorlichtingsprogramma’s geïncludeerd.
Effectiviteit en bewijskracht
Meerdere systematische reviews die opgenomen zijn in de EULAR-richtlijn hebben aangetoond dat met name programma’s die zijn gebaseerd op een theoretisch raamwerk (met name zelfmanagementprogramma’s, cognitieve gedragstherapie en stressmanagementprogramma’s) een klein maar positief effect hebben op zelfgerapporteerde mate van lichaamsbeweging, pijn, beperkingen in activiteiten, depressieve symptomen, angst en vermoeidheid (4-18 maanden follow-up). De EULAR-richtlijn had een redelijke kwaliteit volgens de AGREE 2.0 (5 van de 7 punten).
Van bewijs naar aanbeveling
De werkgroep heeft een aanbeveling geformuleerd voor de dagelijkse praktijk die is gebaseerd op de EULAR-richtlijn.
1. Zangi HA, Ndosi M, Adams J, Anderson L, Bode C, et al. EULAR recommendations for patient education for people with inflammatory arthritis. Ann Rheum Dis. 2015;74;6:1-9.
C.2 Oefentherapie
De aanbeveling voor oefentherapie bij patiënten met RA is opgesplitst in drie eerder gedefinieerde indicaties:
- instructies voor voornamelijk zelfstandig uit te voeren oefentherapie;
- oefentherapie met kortdurende begeleiding;
- oefentherapie met intensieve begeleiding.
Onderbouwing
Noot 10
Uitgangsvraag
Wordt oefentherapie bij patiënten met RA aanbevolen?
Om deze uitgangsvraag te beantwoorden, is een zoekactie uitgevoerd, waarna de literatuur is opgesplitst in:
- oefentherapie bij indicatie 1: studies waarbij het oefenprogramma minimaal 50% niet gesuperviseerd was;
- oefentherapie bij indicatie 2: volledig gesuperviseerde oefentherapie, en
- oefentherapie bij indicatie 3: volledig gesuperviseerde oefentherapie bij patiënten met een ernstig ziektebeloop en/of comorbiditeit.
Bij de beoordeling van de literatuur en het proces ‘van bewijs naar aanbeveling’ is onderscheid gemaakt tussen indicatie 1 (zie noot 11), indicatie 2 (zie noot 12) en indicatie 3 (zie noot 13).
Complete uitgangsvraag volgens PICO
Worden oefentherapeutische interventies (I), vergeleken met geen oefentherapie (C), aanbevolen voor de behandeling van patiënten met RA (P) ter verbetering van de kwaliteit van leven, fysiek functioneren, pijn, vermoeidheid, aerobe capaciteit, spierkracht, range of motion en arbeidsproductiviteit (O)? Tevens zijn de ongewenste effecten van oefentherapeutische interventies bepaald, gedefinieerd als een toename van de pijn, een toename van de ziekte activiteit en radiologische schade.
Zoekstrategie
Er is door het KNGF op 3 maart 2017 een zoekactie uitgevoerd naar samenvatting van de literatuur (i.e. systematische literatuurstudie) en gerandomiseerde gecontroleerde onderzoeken naar oefentherapie bij patiënten met RA. De zoektermen voor oefentherapie zijn opgenomen in de bijlage van deze noot. De selectiecriteria voor inclusie zijn weergegeven in de volgende tabel.
Selectiecriteria systematische literatuurstudie oefentherapie.
| Type studie | RCT’s |
|---|---|
| Type patiënt | volwassenen met de diagnose reumatoïde artritis volgens de ARA- or ACR/EULAR- classificatiecriteria |
| Type interventie | Indicatie 1 Elke vorm van oefentherapie (onafhankelijk van frequentie, intensiteit, type, duur en vorm) gericht op het verbeteren van de aerobe capaciteit, spierkracht van een of meer grote spiergroepen, range of motion van de grote gewrichten en/of balans- training. Daarnaast dient het oefenprogramma minimaal 50% niet gesuperviseerd te zijn. Indicatie 2 Elke vorm van volledig gesuperviseerde oefentherapie (onafhankelijk van fre- quentie, intensiteit, type, duur en vorm) gericht op het verbeteren van de aerobe capaciteit, spierkracht van een of meer grote spiergroepen, range of motion van de grote gewrichten en/of balanstraining. Indicatie 3 Elke vorm van volledig gesuperviseerde oefentherapie (onafhankelijk van fre- quentie, intensiteit, type, duur en vorm) gericht op het verbeteren van de aerobe capaciteit, spierkracht van een of meer grote spiergroepen, range of motion van de grote gewrichten en/of balanstraining bij patiënten met een ernstig ziektebeloop (ziekteactiviteit DAS28 > 5,3 en/of functional class III en IV, en/of comorbiditeit) |
| Type vergelijking | geen oefentherapie of ‘usual care’ (fysiotherapie in controlegroep aanvaardbaar) |
| Type uitkomst | cruciale uitkomstmaten: kwaliteit van leven, fysiek functioneren, pijn*, vermoeidheid belangrijke uitkomstmaten: aerobe capaciteit, spierkracht, range of motion, ziekteactiviteit*, radiologische schade*, arbeidsproductiviteit |
| Type tijdslijn | direct na de interventie |
Gevonden literatuur
De zoekactie van de literatuur leverde 1837 referenties op. Op basis van de kwaliteit, de eigenschappen van de geïncludeerde interventies, het aantal geïncludeerde uitkomstmaten en of GRADE is toegepast, is ervoor gekozen om de Cochrane review van Hurkmans et al.[1] als uitgangspunt te nemen voor de beantwoording van deze uitgangsvraag. Dit systematische literatuuronderzoek omvat literatuur tot december 2008 en scoort hoog op de AMSTAR (9 van de 11 punten). Het KNGF heeft het systematische literatuuronderzoek van Hurkmans et al. gecompleteerd met de inclusie van gerandomiseerde gecontroleerde onderzoeken tot 3 maart 2017. Daarnaast zijn de gerandomiseerde gecontroleerde onderzoeken die geëxcludeerd waren door Hurkmans et al., vanwege een lage intensiteit of minimale supervisie, alsnog geïncludeerd.
De literatuur is opgesplitst in oefentherapie bij indicatie 1, studies waarbij het oefenprogramma voor minimaal 50% niet gesuperviseerd was’, indicatie 2 ‘volledig gesuperviseerde oefentherapie’ en indicatie 3 ‘volledig gesuperviseerde oefentherapie bij patiënten met een ernstig ziektebeloop en/of comorbiditeit’. Uiteindelijk voldeden vier gerandomiseerde gecontroleerde onderzoeken aan de selectiecriteria voor indicatie 1 [2-5] en 19 gerandomiseerde gecontroleerde onderzoeken aan de selectiecriteria voor indicatie 2.[6-24] Er zijn geen studies gevonden voor indicatie 3.
De resultaten van de literatuurstudies van indicatie 1 staan in noot 11, die van indicatie 2 in noot 12 en die van indicatie 3 in noot 13.
De flowcharts van de systematische literatuurstudie(s) naar oefentherapie bij respectievelijk indicatie 1, indicatie 2 en indicatie 3 zijn opgenomen in de bijlage (opent in nieuw tabblad) van deze noot.
1. Hurkmans E, van der Giesen FJ, Vliet Vlieland TP, Schoones J, Van den Ende EC. Dynamic exercise programs (aerobic capacity and/or muscle strength training) in patients with rheumatoid arthritis. Cochrane Database Syst Rev. 2009;7:4.
2. Durcan L, Wilson F, Cunnane G. The effect of exercise on sleep and fatigue in rheumatoid arthritis: a randomized controlled study. J Rheumatol. 2014 Oct;41(10):1966-73.
3. Häkkinen A, Sokka T, Kotaniemi A, Hannonen P. A randomized two-year study of the effects of dynamic strength training on muscle strength, disease activity, functional capacity, and bone mineral density in early rheumatoid arthritis. Arthritis Rheum. 2001 Mar;44(3):515-22.
4. Manning VL, Hurley MV, Scott DL, Coker B, Choy E, Bearne LM. Education, self-management, and upper extremity exercise training in people with rheumatoid arthritis: a randomized controlled trial. Arthritis Care Res (Hoboken). 2014 Feb;66(2):217-27.
5. Stenström CH, Arge B, Sundbom A. Home exercise and compliance in inflammatory rheumatic diseases, a prospective clinical trial. J Rheumatol. 1997;24:2.
6. Baillet A, Payraud E, Niderprim VA, Nissen MJ, Allenet B, François P, et al. A dynamic exercise programme to improve patients’ disability in rheumatoid arthritis: a prospective randomized controlled trial. Rheumatology (Oxford). 2009 Apr;48(4):410-5.
7. Baslund B, Lyngberg K, Andersen V, Halkjaer Kristensen J, Hansen M, Klokker M, et al. Effect of 8 wk of bicycle training on the immune system of patients with rheumatoid arthritis. J Appl Physiol. 1993;75:1691-5.
8. Bearne LM, Scott DL, Hurley MV. Exercise can reverse quadriceps sensorimotor dysfunction that is associated with rheumatoid arthritis without exacerbating disease activity. Rheumatology (Oxford). 2002 Feb;41(2):157-66.
9. Bilberg A, Ahlmén M, Mannerkorpi K. Moderately intensive exercise in a temperate pool for patients with rheumatoid arthritis: a randomized controlled study. Rheumatology (Oxford). 2005 Apr;44(4):502-8.
10. Breedland I, van Scheppingen C, Leijsma M, Verheij-Jansen NP, van Weert E. Effects of a group-based exercise and educational program on physical performance and disease self-management in rheumatoid arthritis: a randomized controlled study. Phys Ther. 2011 Jun;91(6):879-93.
11. Da Silva KN, Teixeira LE, Imoto AM, Atallah AN, Peccin MS, Trevisani VF. Effectiveness of sensorimotor training in patients with rheumatoid arthritis: a randomized controlled trial. Rheumatol Int. 2013 Sep;33(9):2269-75.
12. de Jong Z, Munneke M, Zwinderman AH, Kroon HM, Jansen A, Ronday KH, et al. Is a long-term high-intensity exercise program effective and safe in patients with rheumatoid arthritis? Results of a randomized controlled trial. Arthritis Rheum. 2003;48(9):2415-24.
13. Flint-Wagner HG, Lisse J, Lohman TG, Going SB, Guido T, Cussler E, Gates D, Yocum DE. Assessment of a sixteen-week training program on strength, pain, and function in rheumatoid arthritis patients. J Clin Rheumatol. 2009 Jun;15(4):165-71,
14. Häkkinen A, Häkkinen K, Hannonen P. Effects of strength training on neuromuscular function and disease activity in patients with recent-onset inflammatory arthritis. Scand J Rheumatol. 1994;23(5):237-42.
15. Hansen TM, Hansen G, Langgaard AM, Rasmussen JO. Longterm physical training in rheumatoid arthritis. A randomized trial with different training programs and blinded observers. Scand J Rheumatol. 1993;22(3):107-12.
16. Harkcom TM, Lampman RM, Banwell BF, Castor CW. Therapeutic value of graded aerobic exercise training in rheumatoid arthritis. Arthr Rheum. 1985;28(1):32-9.
17. Lemmey AB, Marcora SM, Chester K, Wilson S, Casanova F, Maddison PJ. Effects of high-intensity resistance training in patients with rheumatoid arthritis: a randomized controlled trial. Arthritis Rheum. 2009 Dec 15;61(12):1726-34.
18. Lyngberg KK, Harreby M, Bentzen H, Frost B. Elderly rheumatoid arthritis on steroid treatment tolerate physical training without an increase in disease activity. Arch Phys Med Rehab. 1994;75:1189-95.
19. McMeeken J, Stillman B, Story I, Kent P, Smith J. The effects of knee extensor and flexor muscle training on the timed-up-and-go test in individuals with rheumatoid arthritis. Physiother Res Int. 1999;4(1):55-67.
20. Minor MA, Hewett JE, Webel RR, Anderson SK, Kay DR. Efficacy of physical conditioning exercise in patients with rheumatoid arthritis and osteoarthritis. Arthritis Rheum. 1989;32(11):1396-405.
21. Sanford-Smith S, Mackay-Lyons M, Nunes-Clement S. Therapeutic benefit of aquaerobics for individuals with rheumatoid arthritis. Physiotherapy Canada 1998;Winter:40-6.
22. Siqueira US, Orsini Valente LG, de Mello MT, Szejnfeld VL, Pinheiro MM. Effectiveness of aquatic exercises in women with rheumatoid arthritis: a randomized, controlled, 16-week intervention – the HydRA Trial. Am J Phys Med Rehabil. 2017 Mar;96(3):167-75.
23. Strasser B, Leeb G, Strehblow C, Schobersberger W, Haber P, Cauza E. The effects of strength and endurance training in patients with rheumatoid arthritis. Clin Rheumatol. 2011 May;30(5):623-32.
24. van den Ende CHM, Hazes JMW, Le Cessie S, Mulder WJ, Belfor DG, Breedveld FC, et al. Comparison of high and low intensity training in well controlled rheumatoid arthritis. Results of a randomized clinical trial. Ann Rheum Dis. 1996;55(11):798-805.
C.2.1 Indicatie 1: Instructies voor voornamelijk zelfstandig uit te voeren oefentherapie
Aanbeveling Overweeg oefentherapie bij patiënten met indicatie 1 in de vorm van instructies voor voornamelijk zelfstandig uit te voeren oefeningen. Zorg dat de oefeningen aansluiten op de hulpvraag van de patiënt en hanteer de uitgangspunten voor de frequentie, de intensiteit, het type en de duur van de oefentherapie.
Toevoeging Pas bij voorkeur geen begeleide oefentherapie toe, en laat de begeleiding, als deze toch nodig is, kortdurend zijn, om te monitoren of de oefentherapie juist wordt uitgevoerd. Bepaal de mate van de begeleiding in overleg met de patiënt. Streef naar maximaal drie tot zes keer begeleide oefentherapie, verspreid over een behandelperiode van drie tot zes maanden. De behandelingen kunnen kort na elkaar plaatsvinden of verspreid over een bepaalde periode.
Oefentherapie wordt altijd aangeboden in combinatie met voorlichting en advies – ter bevordering van de algehele lichamelijke activiteit – aan de hand van de ‘Beweegrichtlijnen van de Gezondheidsraad’.
Onderbouwing
Noot 11
Uitgangsvraag
Wordt oefentherapie bij patiënten met indicatie 1 aanbevolen?
Conclusie vanuit de literatuurstudie
Uit de literatuur blijkt een matig tot groot effect van oefentherapie met beperkte supervisie op de (cruciale) uitkomstmaten ‘kwaliteit van leven’, ‘fysiek functioneren’ en ‘pijn’, vergeleken met geen oefentherapie met beperkte supervisie. De kwaliteit van bewijs varieert van zeer laag tot laag.
Tevens blijkt uit de literatuur een gering effect van oefentherapie met beperkte supervisie op de uitkomstmaat ‘spierkracht’, vergeleken met geen oefentherapie met beperkte supervisie, waarbij de kwaliteit van bewijs redelijk is. De effectiviteit van oefentherapie met beperkte supervisie op ‘vermoeidheid’, ‘range of motion’ en ‘arbeidsproductiviteit’ is onbekend.
Ongewenste effecten van oefentherapie bij indicatie 1, oftewel een toename van de pijn, een toename van de ziekteactiviteit en/of radiologische schade konden worden uitgesloten.
Van bewijs naar aanbeveling
Op basis van de gewenste effecten van oefentherapie bij indicatie 1 en het ontbreken van ongewenste
effecten, de waarschijnlijkheid van kosteneffectiviteit en de hoge mate van aanvaardbaarheid en haalbaarheid van oefentherapie bij indicatie 1, is de werkgroep van mening dat oefentherapie bij indicatie 1 overwogen kan worden.
Aanbeveling voor oefentherapie bij indicatie 1
Overweeg oefentherapie bij patiënten met indicatie 1 in de vorm van instructies voor voornamelijk zelfstandig uit te voeren oefeningen. Zorg dat de oefeningen aansluiten op de hulpvraag van de patiënt en hanteer de uitgangspunten voor de frequentie, de intensiteit, het type en de duur van de oefentherapie.
Complete uitgangsvraag volgens PICO
Voor de beantwoording van deze uitgangsvraag is een gezamenlijke PICO uitgangsvraag geformuleerd voor indicatie 1, 2 en 3 (zie noot 10).
Zoekstrategie
Er is een gezamenlijke zoekactie uitgevoerd voor indicatie 1, 2 en 3 (zie noot 10).
Gevonden literatuur
Uiteindelijk voldeden vier gerandomiseerde gecontroleerde onderzoeken aan de selectiecriteria voor indicatie 1 [1-4]. Hoe tot deze literatuur gekomen is staat beschreven in noot 10.
Beschrijving studies
De geïncludeerde patiënten (n = 282) waren gemiddeld 54 jaar oud en 68% was vrouw. In drie studies bestond de interventie uit eenmalige instructies over hoe de deelnemers het oefenprogramma zelfstandig thuis konden uitvoeren.[1-3] In de vierde studie betrof de interventie vier keer een groepsinstructie (educatie en oefeningen), waarna de patiënten het oefenprogramma zelfstandig thuis uitvoerden.[4] In één studie ontving de controlegroep de gebruikelijke zorg [4], en in drie studies eenmalig advies over respectievelijk de toegevoegde waarde van oefeningen [1], rekken en range-of-motionoefeningen [2], en ontspanningsoefeningen [3].
Effectiviteit en bewijskracht
De beoordeling van de onderzoeksopzet en uitvoering van de geselecteerde artikelen is opgenomen in de bijlage (opent in nieuw tabblad) van deze noot. Hierna volgt per uitkomstmaat een beschrijving van de effectiviteit en de bewijskracht van oefentherapie voor indicatie 1. Zie ook het GRADE-profiel van oefentherapie bij indicatie 1.
Gewenste effecten
Cruciale uitkomstmaten
- Uitkomstmaat ‘kwaliteit van leven’ (2 studies):
- Er bestaat een matig effect (SMD = 0,44; 95%-BI = -0,34-1,22) van oefentherapie met beperkte supervisie op de uitkomstmaat ‘kwaliteit van leven’ bij patiënten met RA, vergeleken met geen behandeling met oefentherapie met beperkte supervisie.
- De bewijskracht voor de uitkomstmaat ‘kwaliteit van leven’ is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’ gezien tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘fysiek functioneren’ (3 studies):
- Er bestaat een matig effect (SMD = 0,32; 95%-BI = 0,02-0,62) van behandeling met oefentherapie met beperkte supervisie op fysiek functioneren bij patiënten met RA, vergeleken met geen behandeling met oefentherapie met beperkte supervisie.
- De bewijskracht voor de uitkomstmaat ‘fysiek functioneren’ is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’ gezien beperkingen in de onderzoeksopzet en uitvoering en het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘vermoeidheid’ (1 studie):
- Het effect van behandeling met oefentherapie met beperkte supervisie op vermoeidheid bij patiënten met RA, vergeleken met geen behandeling met oefentherapie met beperkte supervisie is onbekend (SMD niet beschikbaar).
- De bewijskracht voor de uitkomstmaat ‘vermoeidheid’ is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’ gezien beperkingen in de onderzoeksopzet en uitvoering en het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘pijn’ (4 studies):
- Er bestaat een groot effect (SMD = 0,54; 95%-BI = 0,22-0,87) van behandeling met oefentherapie Met beperkte supervisie op pijn bij patiënten met RA, vergeleken met geen behandeling met oefentherapie met beperkte supervisie.
- De bewijskracht voor de uitkomstmaat ‘pijn’ is met drie niveaus verlaagd tot ‘zeer lage kwaliteit van bewijs’ gezien beperkingen in de onderzoeksopzet en uitvoering, tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
Belangrijke uitkomstmaten
- Uitkomstmaat ‘aerobe capaciteit’ (geen studies): de effectiviteit en bewijskracht kon niet worden bepaald.
- Uitkomstmaat ‘spierkracht’ (1 studie):
- Er bestaat een gering effect (SMD = 0,24; 95%-BI = -0,09-0,57) van behandeling met oefen- therapie met beperkte supervisie op spierkracht bij patiënten met RA, vergeleken met geen behandeling met oefentherapie met beperkte supervisie.
- De bewijskracht voor de uitkomstmaat ‘spierkracht’ is met één niveau verlaagd tot ‘redelijke kwaliteit van bewijs’ gezien het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘range of motion’ (geen studies): de effectiviteit en de bewijskracht kon niet worden bepaald.
- Uitkomstmaat ‘arbeidsproductiviteit’ (geen studies): de effectiviteit en bewijskracht kon niet worden bepaald.
Ongewenste effecten
- Uitkomstmaat ‘ziekteactiviteit’ (2 studies):
- Er bestaat een gering effect (SMD = 0,60; 95%-BI = -0,56-1,77) in het voordeel van behandeling met oefentherapie met beperkte supervisie op ziekteactiviteit bij patiënten met RA, vergeleken met geen behandeling met oefentherapie met beperkte supervisie.
- De bewijskracht voor de uitkomstmaat ‘ziekteactiviteit’ is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’ gezien tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘radiologische schade’ (2 studies):
- Er bestaat een matig effect (SMD = 0,32; 95%-BI = -0,43-1,07) in het voordeel van behandeling met oefentherapie met beperkte supervisie op radiologische schade bij patiënten met RA, vergeleken met geen behandeling met oefentherapie met beperkte supervisie.
- De bewijskracht voor de uitkomstmaat ‘radiologische schade’ is met drie niveaus verlaagd tot ‘zeer lage kwaliteit van bewijs’ gezien beperkingen in de onderzoeksopzet en uitvoering, tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
GRADE-profiel van oefentherapie bij indicatie 1.link
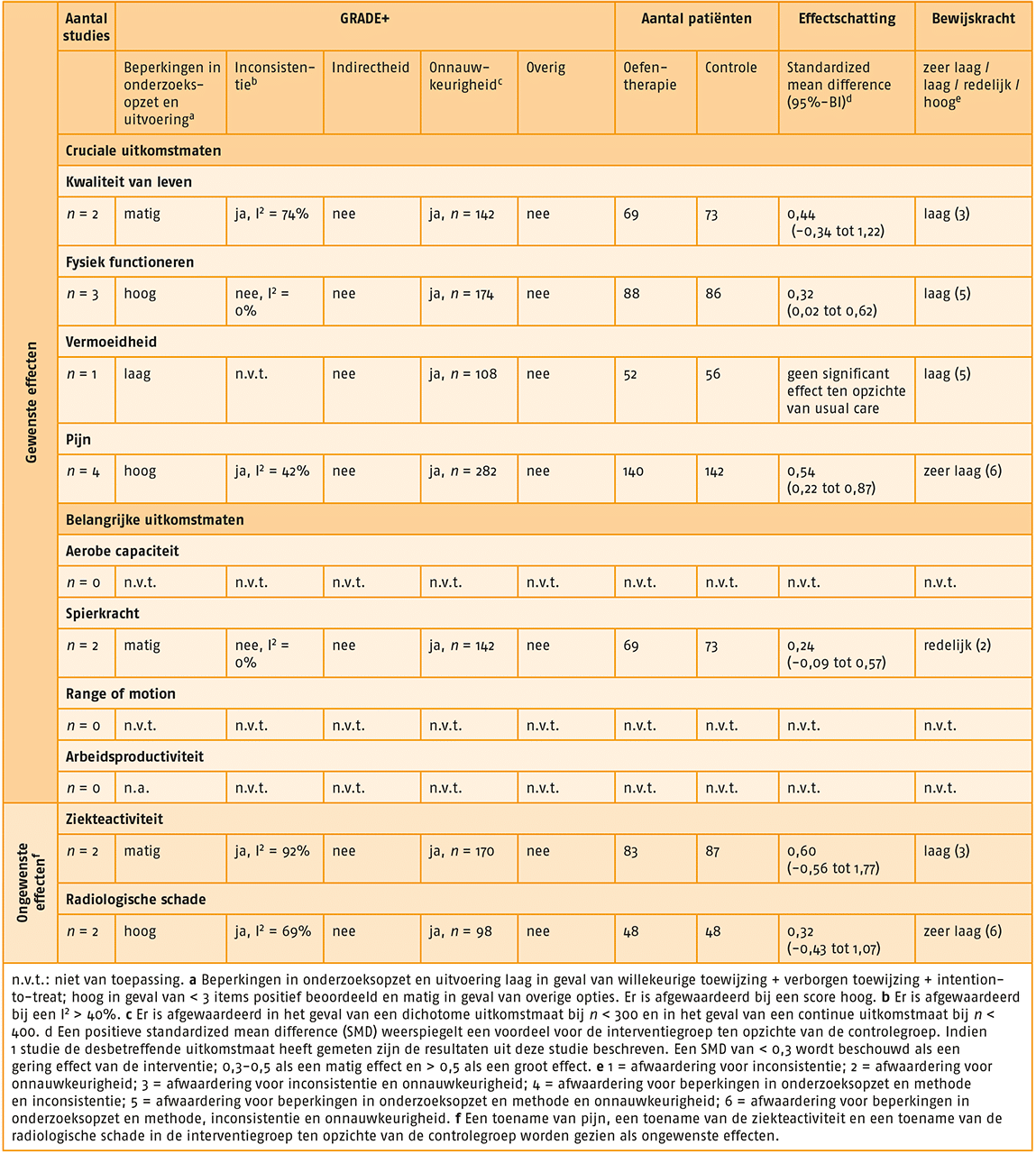
Van bewijs naar aanbeveling
Bij de formulering van de aanbeveling (richting en sterkte) voor oefentherapie bij indicatie 1 heeft de werkgroep de volgende aanvullende overwegingen gemaakt. Zie ook het beoordelingsformulier van bewijs naar aanbeveling voor oefentherapie bij indicatie 1 in de bijlage (opent in nieuw tabblad) van deze noot.
- De gewenste effecten (verbetering van de kwaliteit van leven, de mate van fysieke activiteit en vermoeidheid) van oefentherapie zijn aanwezig, terwijl de ongewenste effecten (een toename van de pijn, ziekteactiviteit en/of radiologische schade) juist in het voordeel waren van de oefentherapie. Alhoewel de effectschattingen van beperkte omvang zijn en er onzekerheid is over de waarschijnlijkheid van de effectschattingen, is de werkgroep van mening dat de gewenste effecten de ongewenste effecten overstijgen.
- Welke waarde patiënten aan handoefeningen hechten zal waarschijnlijk van patiënt tot patiënt verschillen. De werkgroep schat in dat de meeste patiënten positief staan tegenover oefentherapie, vanwege de gunstige effecten ervan en omdat patiënten eenvoudig kunnen inpassen in hun dagelijks leven.
- De kosten van de oefentherapie voor de patiënt zijn afhankelijk van de vigerende overheidsbepalingen ten aanzien van ziektekosten (zie Rijksoverheid.nl), maar blijven in het algemeen beperkt doordat de fysiotherapeut zo weinig mogelijk begeleiding geeft. De fysiotherapeut heeft weinig tot geen kosten aan de oefentherapie, indien er vanuit wordt gegaan dat de benodigde oefenapparatuur reeds aanwezig is.
- De kosteneffectiviteit van een oefenprogramma met beperkte begeleiding van een fysiotherapeut is aangetoond (ICER: € 3.122).[5] Bij een willingness-to-pay van £ 20.000 per QALY, kwamen de onderzoekers tot een waarschijnlijkheid van 65% dat oefentherapie met beperkte supervisie de meest kosteneffectieve optie was, waarbij de kwaliteit van bewijs volgens de CHEC-lijst voor economische evaluaties werd beoordeeld met een score van 14 op de schaal van 19 (d.i. de hoogste kwaliteit).
- De implementatie van de interventie in de dagelijkse praktijk wordt door de werkgroep als aanvaardbaar en haalbaar ingeschat, omdat de interventie als meest aangewezen behandeloptie wordt beschouwd en er geen specifieke middelen voor vereist zijn.
1. Durcan L, Wilson F, Cunnane G. The effect of exercise on sleep and fatigue in rheumatoid arthritis: a randomized controlled study. J Rheumatol. 2014 Oct;41(10):1966-73.
2. Häkkinen A, Sokka T, Kotaniemi A, Hannonen P. A randomized two-year study of the effects of dynamic strength training on muscle strength, disease activity, functional capacity, and bone mineral density in early rheumatoid arthritis. Arthritis Rheum. 2001 Mar;44(3):515-22.
3. Manning VL, Hurley MV, Scott DL, Coker B, Choy E, Bearne LM. Education, self-management, and upper extremity exercise training in people with rheumatoid arthritis: a randomized controlled trial. Arthritis Care Res (Hoboken). 2014 Feb;66(2):217-27.
4. Stenström CH, Arge B, Sundbom A. Home exercise and compliance in inflammatory rheumatic diseases, a prospective clinical trial. J Rheumatol. 1997;24:2.
5. Manning VL, Kaambwa B, Ratcliffe J, Scott DL, Choy E, Hurley MV, Bearne LM. Economic evaluation of a brief education, self-management and upper limb exercise training in people with rheumatoid arthritis (EXTRA) programme: a trial-based analysis. Rheumatology (Oxford). 2015 Feb;54(2):302-9.
C.2.2 Indicaties 2: Oefentherapie met kortdurende begeleiding
Aanbeveling Bied patiënten met indicatie 2 oefentherapie aan, die aansluit op de hulpvraag van de patiënt en hanteer de uitgangspunten voor de frequentie, de intensiteit, het type en de duur van de oefentherapie.
Toevoeging Overweeg in eerste instantie twee keer per week begeleide oefentherapie, aangevuld met zelfstandig uitgevoerde oefeningen.
Oefentherapie wordt altijd aangeboden in combinatie met voorlichting en advies – ter bevordering van de algehele lichamelijke activiteit – aan de hand van de ‘Beweegrichtlijnen van de Gezondheidsraad’.
De begeleiding wordt gedurende de behandelperiode, indien toelaatbaar, in overleg met de patiënt afgebouwd. Hierbij is het van belang dat de frequentie van oefenen niet afneemt; het accent verschuift naar zelfstandig oefenen en bewegen.
Onderbouwing
Noot 12
Uitgangsvraag
Wordt oefentherapie bij patiënten met indicatie 2 aanbevolen?
Conclusie vanuit de literatuurstudie
Uit de literatuur blijkt dat het effect van gesuperviseerde oefentherapie op de (cruciale) uitkomstmaten ‘kwaliteit van leven’, ‘fysiek functioneren’ en ‘pijn’ respectievelijk groot, matig en gering is, vergeleken met ‘geen behandeling’. De kwaliteit van bewijs van deze studies is respectievelijk laag, matig en zeer laag. Tevens
blijkt uit de literatuur een groot effect van gesuperviseerde oefentherapie op ‘spierkracht’ en ‘range of motion’ en een matig effect op ‘aerobe capaciteit’, vergeleken met geen gesuperviseerde oefentherapie, hoewel de kwaliteit van het bewijs laag tot matig is. Het effect van gesuperviseerde oefentherapie op ‘vermoeidheid’ en ‘arbeidsproductiviteit’ is onbekend.
Ongewenste effecten van oefentherapie bij indicatie 2, oftewel een toename van de pijn, een toename van de ziekteactiviteit en/of radiologische schade konden worden uitgesloten.
Van bewijs naar aanbeveling
Op basis van de grote gewenste effecten van oefentherapie bij indicatie 2 (met een redelijke kwaliteit van bewijs) en het ontbreken van ongewenste effecten, de verwachting dat de meerderheid van de patiënten positief staat tegenover oefentherapie vanwege de gunstige effecten ervan en de hoge mate van aanvaardbaarheid en haalbaarheid van oefentherapie bij indicatie 2, is de werkgroep van mening dat oefentherapie bij indicatie 2 sterk aanbevolen kan worden (‘bied oefentherapie aan’).
Aanbeveling voor oefentherapie bij indicatie 2
Bied patiënten met indicatie 2 oefentherapie aan, die aansluit op de hulpvraag van de patiënt en hanteer de uitgangspunten voor de frequentie, de intensiteit, het type en de duur van de oefentherapie zoals beschreven in paragraaf C.3.2.
Complete uitgangsvraag volgens PICO
Voor de beantwoording van deze uitgangsvraag is een gezamenlijke PICO uitgangsvraag geformuleerd voor indicatie 1, 2 en 3 (zie noot 10).
Zoekstrategie
Er is een gezamenlijke zoekactie uitgevoerd voor indicatie 1, 2 en 3 (zie noot 10).
Gevonden literatuur
Uiteindelijk voldeden 19 gerandomiseerde gecontroleerde onderzoeken aan de selectiecriteria voor indicatie 2.[1-19] Hoe tot deze literatuur gekomen is staat beschreven in noot 10.
Beschrijving studies
De geïncludeerde patiënten (n = 1101) waren gemiddeld 54 jaar oud en 70% was vrouw. In 14 studies hadden de patiënten gemiddeld een lage ziekteactiviteit en in vijf studies een matige ziekteactiviteit. In het merendeel van de geïncludeerde studies zijn patiënten met comorbiditeit geëxcludeerd, met uitzondering van één studie waarin 16% van de patiënten hypertensie had. In zes studies zijn patiënten met functional class III en IV geëxcludeerd. In één studie zijn patiënten met ‘functional class III’ wel geïncludeerd. In de overige 12 studies is de ‘functional class’ niet gerapporteerd. In acht studies bestond de interventie uit een combinatie van oefeningen ter verbetering van kracht en uithoudingsvermogen.[1,4,5,7,9,13,17-19] In vijf studies was de oefentherapie gericht op het verbeteren van kracht [3,8,12,14,19], en in vijf studies op het verbeteren van het uithoudingsvermogen.[2,10,11,15,16] In een studie was de interventie gericht op het verbeteren van de balans.[6] De interventie in de controlegroep bestond in 11 studies uit geen interventie [2,6-11,13-15,17], in drie studies uit (instructies voor) huiswerkoefeningen [4,12,18], in twee studies uit een wachtlijst [3,5], in twee studies uit range of motion oefeningen [16,19] en in één studie uit educatie [1].
Effectiviteit en bewijskracht
De beoordeling van de onderzoeksopzet en uitvoering van de geselecteerde artikelen is opgenomen in de bijlage (opent in nieuw tabblad) van deze noot.
Hierna volgt per uitkomstmaat een beschrijving van de effectiviteit van oefentherapie voor indicatie 2 en de bewijskracht daarvoor. Zie ook het GRADE-profiel van oefentherapie bij indicatie 2.
Gewenste effecten
Cruciale uitkomstmaten
- Uitkomstmaat ‘kwaliteit van leven’ (3 studies):
- Er bestaat een groot effect (SMD = 0,70; 95%-BI = 0,14-1,25) van een behandeling met gesuperviseerde oefentherapie op de kwaliteit van leven, vergeleken met geen behandeling met gesuperviseerde oefentherapie.
- De bewijskracht voor de uitkomstmaat ‘kwaliteit van leven’ is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’ gezien tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘fysiek functioneren’ (17 studies):
- Er bestaat een matig effect (SMD = 0,43; 95%-BI = 0,18-0,68) van een behandeling met gesuperviseerde oefentherapie op fysiek functioneren, vergeleken met geen behandeling met gesuperviseerde oefentherapie.
- De bewijskracht voor de uitkomstmaat ‘fysiek functioneren’ is met één niveau verlaagd tot ‘matige kwaliteit van bewijs’ gezien tegenstrijdige resultaten (inconsistentie).
- Uitkomstmaat ‘vermoeidheid’ (geen studies): de effectiviteit en de bewijskracht kon niet worden bepaald.
- Uitkomstmaat ‘pijn’ (3 studies):
- Er bestaat een matig effect (SMD = 0,49; 95%-BI = 0,13-1,11) van behandeling met gesuperviseerde oefentherapie op pijn, vergeleken met geen behandeling met gesuperviseerde oefentherapie.
- De bewijskracht voor de uitkomstmaat ‘pijn’ is met drie niveaus verlaagd tot ‘zeer lage kwaliteit van bewijs’ gezien beperkingen in de onderzoeksopzet en uitvoering, tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
Belangrijke uitkomstmaten
- Uitkomstmaat ‘aerobe capaciteit’ (11 studies):
- Er bestaat een matig effect (SMD = 0,49; 95%-BI = 0,33-0,65) van behandeling met gesuperviseerde oefentherapie op aerobe capaciteit, vergeleken met geen behandeling met gesuperviseerde oefentherapie.
- De bewijskracht voor de uitkomstmaat ‘aerobe capaciteit’ is niet verlaagd.
- Uitkomstmaat ‘spierkracht’ (12 studies):
- Er bestaat een groot effect (SMD = 0,63; 95%-BI = 0,21-1,05) van behandeling met gesuperviseerde oefentherapie op spierkracht, vergeleken met geen behandeling met gesuperviseerde oefentherapie.
- De bewijskracht voor de uitkomstmaat ‘spierkracht’ is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’ gezien beperkingen in de onderzoeksopzet en uitvoering, en tegenstrijdige resultaten (inconsistentie).
- Uitkomstmaat ‘range of motion’ (2 studies):
- Er bestaat een groot effect (SMD = 0,59; 95%-BI = 0,17-1,01) van behandeling met gesuperviseerde oefentherapie op range of motion, vergeleken met geen behandeling met gesuperviseerde oefentherapie.
- De bewijskracht voor de uitkomstmaat ‘range of motion’ is met één niveau verlaagd tot ‘matige kwaliteit van bewijs’ gezien het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘arbeidsproductiviteit’ (0 studies): de effectiviteit en bewijskracht kon niet worden bepaald.
Ongewenste effecten
- Uitkomstmaat ‘ziekteactiviteit’ (9 studies):
- Er bestaat een gering effect (SMD = 0,23; 95%-BI = 0,16-0,62) in het voordeel van behandeling met gesuperviseerde oefentherapie op ziekteactiviteit, vergeleken met geen behandeling met gesuperviseerde oefentherapie.
- De bewijskracht voor de uitkomstmaat ‘ziekteactiviteit’ is met één niveau verlaagd tot ‘matige kwaliteit van bewijs’ gezien tegenstrijdige resultaten (inconsistentie).
- Uitkomstmaat ‘radiologische schade’ (2 studies):
- Er bestaat een gering effect (SMD = 0,09; 95%-BI = 0,14-0,31) in het voordeel van behandeling met gesuperviseerde oefentherapie op radiologische schade, vergeleken met geen behandeling met gesuperviseerde oefentherapie.
- De bewijskracht voor de uitkomstmaat ‘radiologische schade’ is met één niveau verlaagd tot ‘matige kwaliteit van bewijs’ gezien het geringe aantal patiënten (onnauwkeurigheid).
GRADE-profiel van oefentherapie bij indicatie 2. [link]
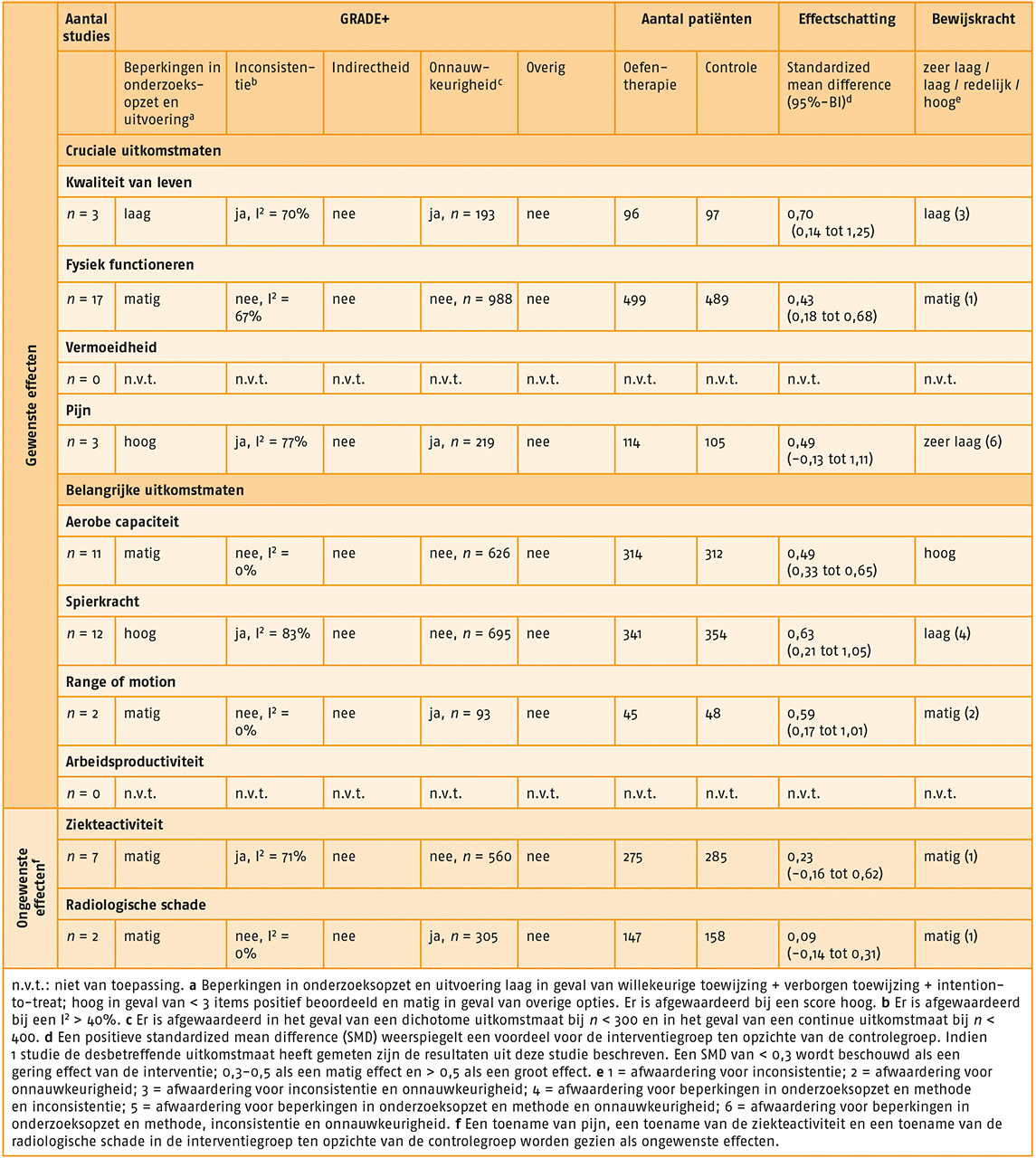
Van bewijs naar aanbeveling
- Bij de formulering van de aanbeveling (richting en sterkte) voor oefentherapie bij indicatie 1 heeft de werkgroep de volgende aanvullende overwegingen gemaakt. Zie ook het beoordelingsformulier van bewijs naar aanbeveling voor oefentherapie bij indicatie 2 in de bijlage (opent in nieuw tabblad) van deze noot.
- De gewenste effecten (verbetering van de kwaliteit van leven en verbetering van de mate van fysieke) van oefentherapie zijn aanwezig, terwijl de ongewenste effecten (een toename van de pijn, ziekteactiviteit en/of radiologische schade) juist in het voordeel waren van de oefentherapie. Op basis hiervan wordt door de werkgroep de inschatting gemaakt dat de gewenste effecten de ongewenste effecten overstijgen.
- Welke waarde patiënten aan oefentherapie hechten, zal waarschijnlijk van patiënt tot patiënt verschillen. De werkgroep schat in dat de meeste patiënten positief staat tegenover oefentherapie, vanwege de gunstige effecten ervan en omdat patiënten oefentherapie eenvoudig kunnen inpassen in hun dagelijks leven.
- De kosten van de oefentherapie voor de patiënt zijn afhankelijk van de vergoeding door de zorgverzekeraar (en de vigerende overheidsbepalingen ten aanzien van ziektekosten, zie Rijksoverheid.nl, maar blijven in het algemeen beperkt doordat de fysiotherapeut maar gedurende korte tijd begeleiding geeft. De fysiotherapeut heeft weinig tot geen kosten aan de oefentherapie, indien er vanuit wordt gegaan dat de benodigde oefenapparatuur reeds aanwezig is.
- Een langdurig oefenprogramma van twee jaar lijkt vanuit sociaal perspectief en zonder rekening te houden met preventieve gezondheidseffecten op lange termijn, onvoldoende verbetering op te leveren in de waardering van de gezondheid om de extra kosten te rechtvaardigen (ICER € 6.7000 per QALY)20 waarbij de kwaliteit van bewijs volgens de CHEC-lijst voor economische evaluaties is beoordeeld met een score van 11 op de schaal van 19 (d.i. de hoogste kwaliteit). Volgens deze richtlijn wordt echter bij indicatie 2 een behandelduur van drie tot zes maanden aangehouden en daarvan is de kosteneffectiviteit nog onbekend.
- De implementatie van de interventie in de dagelijkse praktijk wordt door de werkgroep als aanvaardbaar en haalbaar ingeschat, omdat de interventie als meest aangewezen behandeloptie wordt beschouwd en er geen specifieke middelen voor vereist zijn.
1. Baillet A, Payraud E, Niderprim VA, Nissen MJ, Allenet B, François P, et al. A dynamic exercise programme to improve patients’ disability in rheumatoid arthritis: a prospective randomized controlled trial. Rheumatology (Oxford). 2009 Apr;48(4):410-5.
2. Baslund B, Lyngberg K, Andersen V, Halkjaer Kristensen J, Hansen M, Klokker M, et al. Effect of 8 wk of bicycle training on the immune system of patients with rheumatoid arthritis. J Appl Physiol. 1993;75:1691-5.
3. Bearne LM, Scott DL, Hurley MV. Exercise can reverse quadriceps sensorimotor dysfunction that is associated with rheumatoid arthritis without exacerbating disease activity. Rheumatology (Oxford). 2002 Feb;41(2):157-66.
4. Bilberg A, Ahlmén M, Mannerkorpi K. Moderately intensive exercise in a temperate pool for patients with rheumatoid arthritis: a randomized controlled study. Rheumatology (Oxford). 2005 Apr;44(4):502-8.
5. Breedland I, van Scheppingen C, Leijsma M, Verheij-Jansen NP, van Weert E. Effects of a group-based exercise and educational program on physical performance and disease self-management in rheumatoid arthritis: a randomized controlled study. Phys Ther. 2011 Jun;91(6):879-93.
6. Da Silva KN, Teixeira LE, Imoto AM, Atallah AN, Peccin MS, Trevisani VF. Effectiveness of sensorimotor training in patients with rheumatoid arthritis: a randomized controlled trial. Rheumatol Int. 2013 Sep;33(9):2269-75.
7. de Jong Z, Munneke M, Zwinderman AH, Kroon HM, Jansen A, Ronday KH, et al. Is a long-term high-intensity exercise program effective and safe in patients with rheumatoid arthritis? Results of a randomized controlled trial. Arthritis Rheum. 2003;48(9):2415-24.
8. Flint-Wagner HG, Lisse J, Lohman TG, Going SB, Guido T, Cussler E, Gates D, Yocum DE. Assessment of a sixteen-week training program on strength, pain, and function in rheumatoid arthritis patients. J Clin Rheumatol. 2009 Jun;15(4):165-71,
9. Häkkinen A, Häkkinen K, Hannonen P. Effects of strength training on neuromuscular function and disease activity in patients with recent-onset inflammatory arthritis. Scand J Rheumatol. 1994;23(5):237-42.
10. Hansen TM, Hansen G, Langgaard AM, Rasmussen JO. Longterm physical training in rheumatoid arthritis. A randomized trial with different training programs and blinded observers. Scand J Rheumatol. 1993;22(3):107-12.
11. Harkcom TM, Lampman RM, Banwell BF, Castor CW. Therapeutic value of graded aerobic exercise training in rheumatoid arthritis. Arthr Rheum. 1985;28(1):32-9.
12. Lemmey AB, Marcora SM, Chester K, Wilson S, Casanova F, Maddison PJ. Effects of high-intensity resistance training in patients with rheumatoid arthritis: a randomized controlled trial. Arthritis Rheum. 2009 Dec 15;61(12):1726-34.
13. Lyngberg KK, Harreby M, Bentzen H, Frost B. Elderly rheumatoid arthritis on steroid treatment tolerate physical training without an increase in disease activity. Arch Phys Med Rehab. 1994;75:1189-95.
14. McMeeken J, Stillman B, Story I, Kent P, Smith J. The effects of knee extensor and flexor muscle training on the timed-up-and-go test in individuals with rheumatoid arthritis. Physiother Res Int. 1999;4(1):55-67.
15. Minor MA, Hewett JE, Webel RR, Anderson SK, Kay DR. Efficacy of physical conditioning exercise in patients with rheumatoid arthritis and osteoarthritis. Arthritis Rheum. 1989;32(11):1396-405.
16. Sanford-Smith S, Mackay-Lyons M, Nunes-Clement S. Therapeutic benefit of aquaerobics for individuals with rheumatoid arthritis. Physiotherapy Canada 1998;Winter:40-6.
17. Siqueira US, Orsini Valente LG, de Mello MT, Szejnfeld VL, Pinheiro MM. Effectiveness of aquatic exercises in women with rheumatoid arthritis: a randomized, controlled, 16-week intervention – the HydRA Trial. Am J Phys Med Rehabil. 2017 Mar;96(3):167-75.
18. Strasser B, Leeb G, Strehblow C, Schobersberger W, Haber P, Cauza E. The effects of strength and endurance training in patients with rheumatoid arthritis. Clin Rheumatol. 2011 May;30(5):623-32.
19. van den Ende CHM, Hazes JMW, Le Cessie S, Mulder WJ, Belfor DG, Breedveld FC, et al. Comparison of high and low intensity training in well controlled rheumatoid arthritis. Results of a randomized clinical trial. Ann Rheum Dis. 1996;55(11):798-805.
20. van den Hout WB, de Jong Z, Munneke M, Hazes JM, Breedveld FC, Vliet Vlieland TP. Cost-utility and cost-effectiveness analyses of a long-term, high-intensity exercise program compared with conventional physical therapy in patients with rheumatoid arthritis. Arthritis Rheum. 2005 Feb 15;53(1):39-47
C.2.3 Indicatie 3: Oefentherapie met intensieve begeleiding
Uitgangsvraag
Wordt oefentherapie bij patiënten met indicatie 3 aanbevolen?
Aanbevelingen
Bied langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie aan bij patiënten met Reumatoïde Artritis (RA) met ernstige functionele beperkingen in het dagelijks leven, met als doel het dagelijks functioneren en de participatie te verbeteren en behouden, waarbij:
- behandeldoelen regelmatig (minimaal één keer per drie maanden) worden geëvalueerd (en waar nodig bijgesteld) of opnieuw worden geformuleerd, aangezien de aard en ernst van de problematiek fluctueren;
- deze altijd aangeboden wordt in combinatie met voorlichting en advies (module C.1. Voorlichting en advies) ter bevordering van de algehele lichamelijke activiteit in het dagelijks leven van de patiënt aan de hand van de ‘Beweegrichtlijnen’ van de Gezondheidsraad;
- de frequentie gedurende de behandelperiode, indien toelaatbaar en in overleg met de patiënt, wordt afgebouwd; hierbij is het van belang dat reeds vanaf een vroeg stadium gestreefd wordt naar toenemende zelfstandigheid en verminderde therapie afhankelijkheid. Zie ook module C.6 Afsluiting van de behandeling’.
Toelichting C.2.3
Aanleiding
De fysio- of oefentherapeut begeleidt de patiënt bij het proces van het voorkomen of verminderen van en/of het leren omgaan met beperkingen in activiteiten van het dagelijks leven en maatschappelijke participatie ten gevolge van RA. De belangrijkste middelen om dit doel te bereiken, zijn het geven van voorlichting en advies, en oefentherapie.
In 2024 is de ‘Longstanding EXercise Therapy for people with Rheumatoid Arthritis (L-EXTRA)-studie’ naar de effecten van langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie gepubliceerd (3).
Naar aanleiding van deze L-EXTRA-studie is door het Zorginstituut geconcludeerd dat langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie (≥ 52 weken) onder supervisie van een fysio- of oefentherapeut beschouwd kan worden als effectieve behandeling bij volwassen patiënten (≥ 18 jaar) met RA met ernstige functionele beperkingen in het dagelijks leven. Deze interventie voldoet bij de genoemde indicatie daarom aan ‘de stand van de wetenschap en praktijk’.
Naar aanleiding van dit onderzoek is de minister geadviseerd om, gelet op de weging van de vier pakketcriteria (de ‘stand van de wetenschap en praktijk’, kosteneffectiviteit, noodzakelijkheid en uitvoerbaarheid), langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie bij deze indicatie op te nemen in de basisverzekering. De minister is hiermee akkoord gegaan, onder de voorwaarde dat onder andere de huidige KNGF-richtlijn Reumatoïde artritis (2018) wordt herzien op twee modules, namelijk B.4 ‘Indicatiestelling’ en C.3.2 ‘Oefentherapie met intensieve begeleiding’.
In deze module wordt ingegaan op de vraag of oefentherapie aanbevolen wordt voor patiënten met RA met ernstige functionele beperkingen.
Rationale van de aanbeveling
De werkgroep heeft besloten om een sterke aanbeveling voor langdurige (≥ 52 weken) gepersonaliseerde gesuperviseerde actieve oefentherapie in deze richtlijn op te nemen.
De resultaten uit de L-EXTRA-studie laten zien dat langdurige (≥ 52 weken) gepersonaliseerde gesuperviseerde actieve oefentherapie bij patiënten met RA met ernstige functionele beperkingen, resulteert in overwegend klinisch relevante effecten op de cruciale uitkomstmaten en geen (belangrijke) bijwerkingen geeft.
De werkgroep is van mening dat de gewenste effecten (positieve effecten op fysiek functioneren en kwaliteit van leven) de ongewenste effecten (één ongewenst ongeval, vermoeidheid en spierpijn) lijken te overtreffen. De economische overwegingen, gezondheidsgelijkheid en kosteneffectiviteit, waarden en voorkeuren van patiënten lijken in het voordeel van de langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie. De overige criteria waarop de literatuur beoordeeld is, in het proces van bewijs naar aanbeveling (aanvaardbaarheid, haalbaarheid en implementatie), zijn als niet-bezwaarlijk of waarschijnlijk realiseerbaar bevonden, waarbij men wel aangeeft dat de verplichte training voor fysio- en oefentherapeuten een belemmering vormt voor de implementatie en haalbaarheid.
Concluderend stelt de werkgroep op basis van de literatuur dat langdurige (≥ 52 weken) gesuperviseerde gepersonaliseerde actieve oefentherapie bij patiënten met RA met ernstige functionele beperkingen resulteert in overwegend klinisch relevante effecten op de cruciale uitkomstmaten en geen (belangrijke) bijwerkingen geeft. De werkgroep is van mening dat de gunstige effecten overheersen, waardoor er een sterke aanbeveling voor de langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie is geformuleerd.
Literatuuronderzoek
Onderzoeksvraag
Om de uitgangsvraag te kunnen beantwoorden is een systematische literatuuranalyse verricht naar de volgende onderzoeksvraag:
Wat is het effect van langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie bij patiënten met reumatoïde artritis met ernstige functionele beperkingen in het dagelijks leven?
De werkgroep achtte fysiek functioneren en kwaliteit van leven voor de besluitvorming als cruciale uitkomstmaten en ervaren bijwerkingen, pijn en vermoeidheid, stoppen met de interventie (door bijwerkingen van de interventie, andere redenen) en ervaren effect als belangrijke uitkomstmaten.
Hierbij is aangesloten bij de uitkomsten en klinische-relevantiegrenzen, die gehanteerd worden in het adviesrapport van het Zorginstituut Nederland (4, 5). Daar waar geen klinische relevantie grens is beschreven, is deze ook niet door het Zorginstituut bepaald en gehanteerd.
Per cruciale uitkomstmaat worden de klinische-relevantiegrenzen beschreven:
- Het gestandaardiseerde gemiddelde verschil (SMD):
De werkgroep definieerde een effect > 0,3 als een belangrijk effect (klinisch relevant verschil). Er is hier rekening gehouden met het feit dat eerstelijnsoefentherapie, gegeven door een fysio- of oefentherapeut, een niet-invasieve behandeling is die waarschijnlijk geen bijwerkingen kent, en daarnaast wordt vergeleken met gebruikelijke zorg waarbij ook adviezen en instructies over bewegen naast fysio- en oefentherapie worden gegeven. Daarom hanteren wij in deze richtlijn geen SMD van 0,5, maar een SMD van 0,3 als klinische-relevantiegrens.
Het gemiddeld verschil van:
- Fysiek functioneren: fysiek functioneren wordt onderverdeeld in zelf-gerapporteerd fysiek functioneren en fysiek functioneren als performance.
- Zelf-gerapporteerd fysiek functioneren: dit betreft het ervaren fysiek functioneren in het algemeen dagelijks leven van de patiënt zelf.
- Patiënt Specifieke Klachten (PSK).
De moeilijkheid die een patiënt ervaart met activiteiten die voor hem/haar het meest relevant zijn, wordt uitgedrukt op een Visual Analogue Scale (VAS-schaal) van 0 tot 100 punten of op een Numeric Rating Scale (NRS) van 0 tot 10 punten, respectievelijk geen enkele moeite tot onmogelijk. Een hogere score komt overeen met meer moeite bij het uitvoeren van de activiteit. De werkgroep definieerde een verandering van 2 punten op een NRS-schaal van 0-10 als een belangrijk effect voor patiënten (klinisch relevant verschil).
- Patient Reported Outcomes Measurement Information System for Physical Function
10-item (PROMIS PF-10).
Een hogere score op de PROMIS PF-10 hangt samen met een beter fysiek functioneren. De werkgroep hanteerde een hogere score op de PROMIS PF-10 als een belangrijk effect voor patiënten (klinisch relevant verschil) (7).
- Health Assessment Questionnaire-Disability Index (HAQ-DI).
De totaalscore wordt berekend op een schaal van 0 tot 3, waarbij 0 zonder enige moeite betekent en 3 onmogelijk uit te voeren. De werkgroep definieerde een verandering van 0,22 units binnen een groep patiënten als een belangrijk effect voor patiënten (klinisch relevant verschil) (8, 9).
- Fysiek functioneren als performance: hierbij wordt het fysiek functioneren gemeten met fysieke testen.
- 6 Minuten Wandeltest (6MWT).
Hoe meer meters er zijn afgelegd, hoe beter het functioneren. Een verschil van 25-50 meter binnen een groep patiënten wordt volgens de KNGF-richtlijn als klinisch relevant beschouwd (10-12).
- Kwaliteit van leven: kwaliteit van leven kan gemeten worden met ziekte specifieke vragenlijsten en met algemene/generieke vragenlijsten.
- Short-Form-36 for Quality of Life (SF-36).
Het instrument bevat schalen voor fysiek functioneren (PCS), sociaal functioneren, rolbeperkingen door fysieke of emotionele problemen, mentale gezondheid (MCS), energie, pijn en algemene gezondheidsbeleving. De scores per domein variëren van 0 tot 100, waarbij een hogere score overeenkomt met een betere gezondheidstoestand en kwaliteit van leven (13).
- Rheumatoid Arthritis Quality of Life questionnaire (RAQoL).
Items worden gescoord als 1 voor ‘ja’ en 0 voor ‘nee’. De totaalscore betreft het aantal items waarop met ‘ja’ is geantwoord en varieert daarmee van 0 tot 30, waarbij een hogere score een lagere kwaliteit van leven betekent (8).
Per belangrijke uitkomstmaat worden de klinische-relevantiegrenzen beschreven:
- Serious adverse event (SAE)/ernstig ongewenst ongeval.
Gedefinieerd als een gebeurtenis die de dood tot gevolg heeft of levensbedreigend is, waarvoor een ziekenhuisopname nodig is of die aanzienlijke gevolgen heeft of blijvende (verergering van) invaliditeit of arbeidsongeschiktheid direct gerelateerd aan de oefentherapeutische behandeling (14).
De werkgroep definieerde elk ernstig ongewenst ongeval in relatie tot de oefentherapeutische behandeling als klinisch relevant.
- Adverse event/ongewenst ongeval.
Gedefinieerd als een ongunstige gebeurtenis die rechtstreeks verband houdt met lichaamsbeweging, therapiebehandeling, maar niet ernstig is, zoals een tijdelijke onderbreking van de therapie wegens misselijkheid of een val zonder letsel (14).
De werkgroep definieerde een ongewenst ongeval in relatie tot de oefentherapeutische behandeling als klinisch relevant.
- Ervaren bijwerkingen of effecten.
Gedefinieerd als bijwerkingen of effecten die rechtstreeks verband houden met lichaamsbeweging, therapiebehandeling, maar niet ernstig zijn.
De werkgroep definieerde bijwerkingen zoals spierpijn en vermoeidheid, in relatie tot de oefentherapeutische behandeling als niet relevant, maar als symptomen die passend zijn bij het uitvoeren van de oefentherapeutische behandeling.
Zoeken en selecteren
De volgende inclusiecriteria zijn gedefinieerd om artikelen te selecteren:
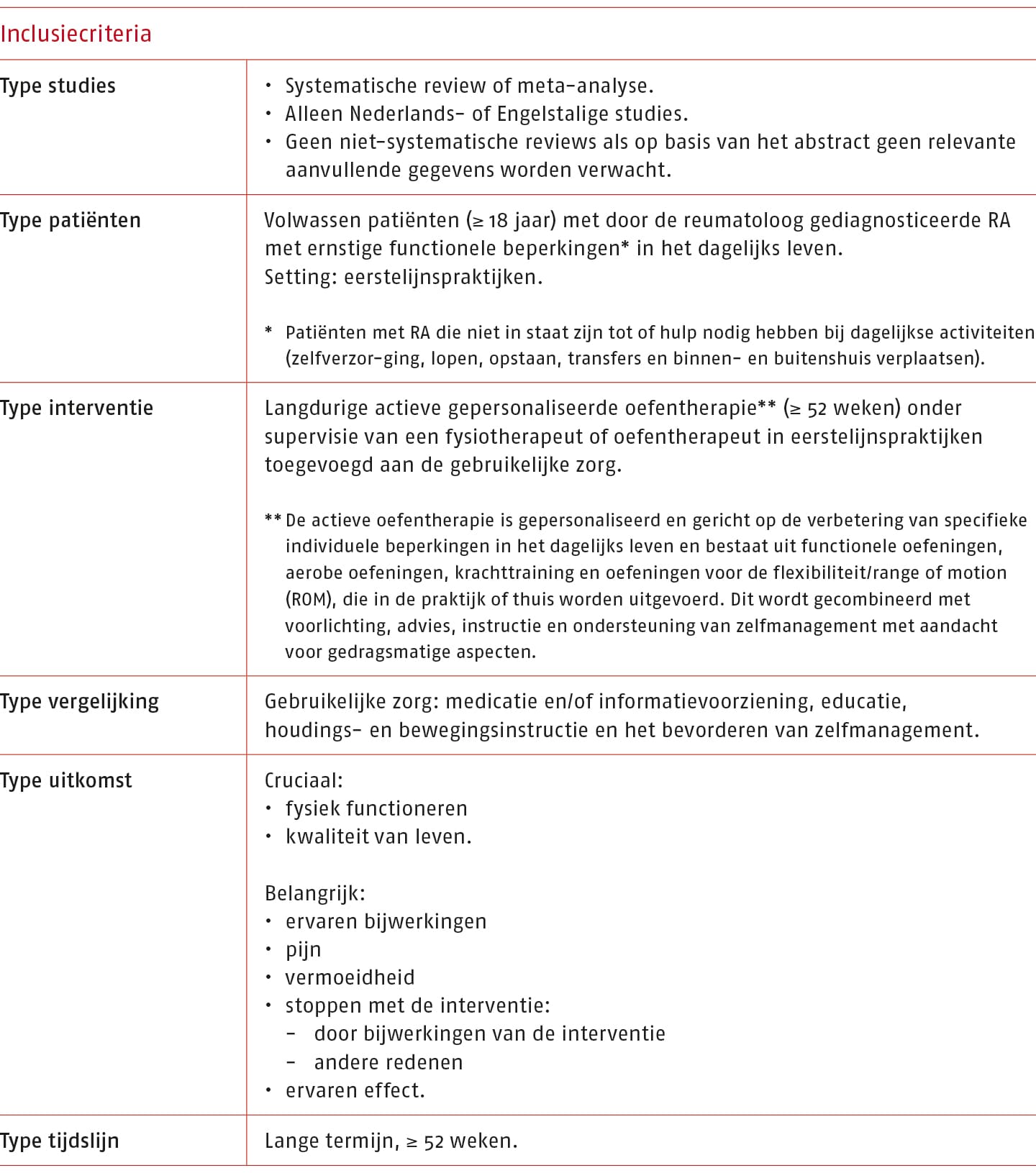
Op 24 april 2023 is door het Zorginstituut Nederland een systematische zoekactie uitgevoerd in Embase, Medline en CINAHL (zie bijlage C.2.3-1 (opent in nieuw tabblad) voor de zoekverantwoording). De systematische zoekactie leverde 238 records en na verwijderen van de duplicaten 165 unieke treffers op. Na screening van de titel en het abstract op de inclusiecriteria zijn 158 artikelen geëxcludeerd. Van 6 artikelen is het volledige artikel gescreend. De artikelen die op basis van de volledige tekst zijn geëxcludeerd, en de reden van exclusie zijn weergegeven in bijlage C.2.3-3. (opent in nieuw tabblad) Uiteindelijk leverde de zoekactie 0 studies op. Zie bijlage C.2.3-2 (opent in nieuw tabblad) voor het stroomdiagram van het inclusieproces.
Karakteristieken van geïncludeerde studies
Op 27 juni 2023 heeft het Zorginstituut Nederland een onderzoeksverslag en de conceptmanuscripten ontvangen met de resultaten van de L-EXTRA-studie. In deze studie is ook een uitgebreide zoekstrategie uitgevoerd in diverse databases t/m juni 2023. Deze zoekstrategie heeft ook geen artikelen opgeleverd die voldoen aan de PICOT (Patient, Interventie, Comparison, Outcome, Time). De voorliggende beoordeling is dan ook volledig gebaseerd op de resultaten van de L-EXTRA-studie (14).
De L-EXTRA-studie betreft een longitudinaal gerandomiseerd, gecontroleerd, enkelblind, multicenter onderzoek in Nederland naar de effectiviteit van langdurige (≥ 52 weken) gepersonaliseerde actieve oefentherapie bij patiënten met RA met ernstige functionele beperkingen toegevoegd aan de gebruikelijke zorg in vergelijking met gebruikelijke zorg.
De langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie is gericht op individuele behandeldoelen en aangepast aan de functionele mogelijkheden en gezondheidsstatus van de patiënt, en bestaat uit oefeningen voor de conditie, kracht, functie en mobiliteit. De interventie wordt uitsluitend aangeboden door fysio- en oefentherapeuten in de eerste lijn die een verplichte specifieke training hebben gevolgd via een digitale scholingstool (app) of een live online trainingssessie. Het belangrijkste onderdeel van de training is de langdurige gepersonaliseerde actieve gesuperviseerde oefentherapie, die bestaat uit het vaststellen van gepersonaliseerde behandeldoelen en behandelmodaliteiten (aerobe capaciteit, spierkrachttraining, flexibiliteit, gewricht range of motion en functioneel trainen van motorische vaardigheden, patiënteducatie en stimuleren van lichamelijke activiteit). De fysiotherapeut/oefentherapeut werd geïnstrueerd om te starten met 2 sessies per week gedurende de eerste 12 weken. Daarna moest de frequentie worden afgebouwd naar 1 keer per week. Indien nodig, konden in het eerste jaar 14 extra sessies ingezet worden. Patiënten in de interventiegroep werden niet aangemoedigd om oefentherapie te krijgen in aanvulling op de interventie.
De controlegroep kreeg gebruikelijke zorg. Uit de L-EXTRA-studie blijkt dat dit ook fysio- of oefentherapie kon zijn. Na 52 weken hadden zowel patiënten in de interventiegroep als patiënten in de controlegroep voortzetting van of respectievelijk toegang tot de langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie.
Uitkomsten zijn de veranderingen in individuele beperkte activiteiten gemeten met de PSK, zelf-gerapporteerd fysiek functioneren (PROMIS PF-10, HAQ-DI), fysiek functioneren gemeten met fysieke testen (6MWT) en kwaliteit van leven (RAQoL, SF-36). Deze uitkomsten zijn gemeten op baseline, 26 weken (m.u.v. 6MWT), 52 weken en 104 weken (range 80-122 weken). Ook werd bij de interventiegroep het optreden van (zeer) ernstige complicaties gerapporteerd door de behandelend fysiotherapeut of oefentherapeut. Bij 52 weken werd patiënten gevraagd naar de ernst van de spierpijn en vermoeidheid gerelateerd aan de interventie.
Ten behoeve van de economische analyse werden vragenlijsten over zorggebruik, informele zorg, huishoudelijke hulp, arbeidsproductiviteit en waardering van kwaliteit van leven gemeten met de EuroQol-5D-5L en EQ-VAS, afgenomen.
Er werden 394 deelnemers gescreend op de in- en exclusiecriteria. Tijdens de screening zijn 177 deelnemers (45%) afgevallen, waarvan 74 deelnemers omdat de functionele beperkingen niet ernstig genoeg waren en 19 deelnemers omdat de diagnose niet werd bevestigd door de reumatoloog. Er werden 217 patiënten gerandomiseerd in de interventiegroep en controlegroep. Na 1 uitvaller in beide groepen zaten er 109 patiënten in de interventiegroep (leeftijd in jaren (SD) 59,4 (12,1)) en 106 (leeftijd in jaren (SD) 58,1 (13,6)) in de controlegroep.
Het percentage vrouwen was 89 in de interventiegroep en 92 in de controlegroep. De duur van de zelf-gerapporteerde klachten in jaren (SD) was 21,6 (12,6) in de interventiegroep en 21,6 (14,0) in de controlegroep.
De metingen waren bij 52 weken compleet van 105 patiënten in de interventiegroep en 99 in de controlegroep. In de ITT-analyse zitten 104 patiënten van de interventiegroep en 98 van de controlegroep, omdat in beide groepen van 1 patiënt de metingen niet voltooid waren binnen het vooraf gedefinieerde tijdsbestek van 6 weken. Van de 109 patiënten in de interventiegroep maakten 99 patiënten (91%) daadwerkelijk gebruik van de interventie in de eerste 52 weken. Het gemiddeld aantal sessies van deze 99 patiënten was 39. In de controlegroep maakte 70 patiënten (66%) gebruik van fysio- of oefentherapie.
Tussen 52 en 104 weken maakten 74 van de 105 patiënten (70%) uit de interventiegroep, die op 52 weken nog in de studie zaten, gebruik van de interventie. Het gemiddeld aantal sessies van deze patiënten was 20 (SD 16). Het tijdstip van de 104 weken of eindmeting varieerde tussen de 80 en 122 weken ten opzichte van de baseline. Van de 99 patiënten die gebruikelijke zorg kregen en die op 52 weken nog in de studie zaten, maakten 61 patiënten (62%) gebruik van de interventie. De kenmerken van de geïncludeerde studie zijn weergegeven in bijlage C.3.2-4. (opent in nieuw tabblad)
Individuele studiekwaliteit (RoB)
Het risico op vertekening (risk of bias, RoB) is door het Zorginstituut Nederland gescoord met behulp van de Cochrane Risk-of-Bias tool (15). Een overzicht van de beoordeling van de studiekwaliteit (RoB) per studie is weergegeven in bijlage C.3.2-5 (opent in nieuw tabblad) Risk-of-biastabel.
Het risico op vertekening als gevolg van de studieopzet en -uitvoering (RoB) wordt als niet ernstig beschouwd ondanks het ontbreken van blindering van behandelaars en patiënten. Bij de interventie actieve fysio- of oefentherapie en een controlegroep is blindering van patiënten en behandelaars niet mogelijk.
Resultaten
Hieronder volgt per uitkomstmaat een samenvatting van de resultaten (effectgrootte gemiddeld verschil (MD), relatief risico (RR), risicoverschil (RV)). Per uitkomstmaat is de kwaliteit van het bewijs beoordeeld met de GRADE-methodiek. De bewijskracht, ‘certainty of the evidence’, reflecteert de mate van vertrouwen dat de schatting van een gevonden effect juist is.
Langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie versus gebruikelijke zorg
Het effect van langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie vergeleken met gebruikelijke zorg is beschreven in 1 studie (14). Een overzicht van de resultaten van deze studie wordt weergegeven in de volgende tabel. Voor de effectschatting wordt de gemiddelde verschilscore van baseline tot 52 weken gebruikt tussen de groepen. Als de gemiddelde verschilscore niet bekend is, wordt de postscore na 52 weken tussen de groepen gebruikt.
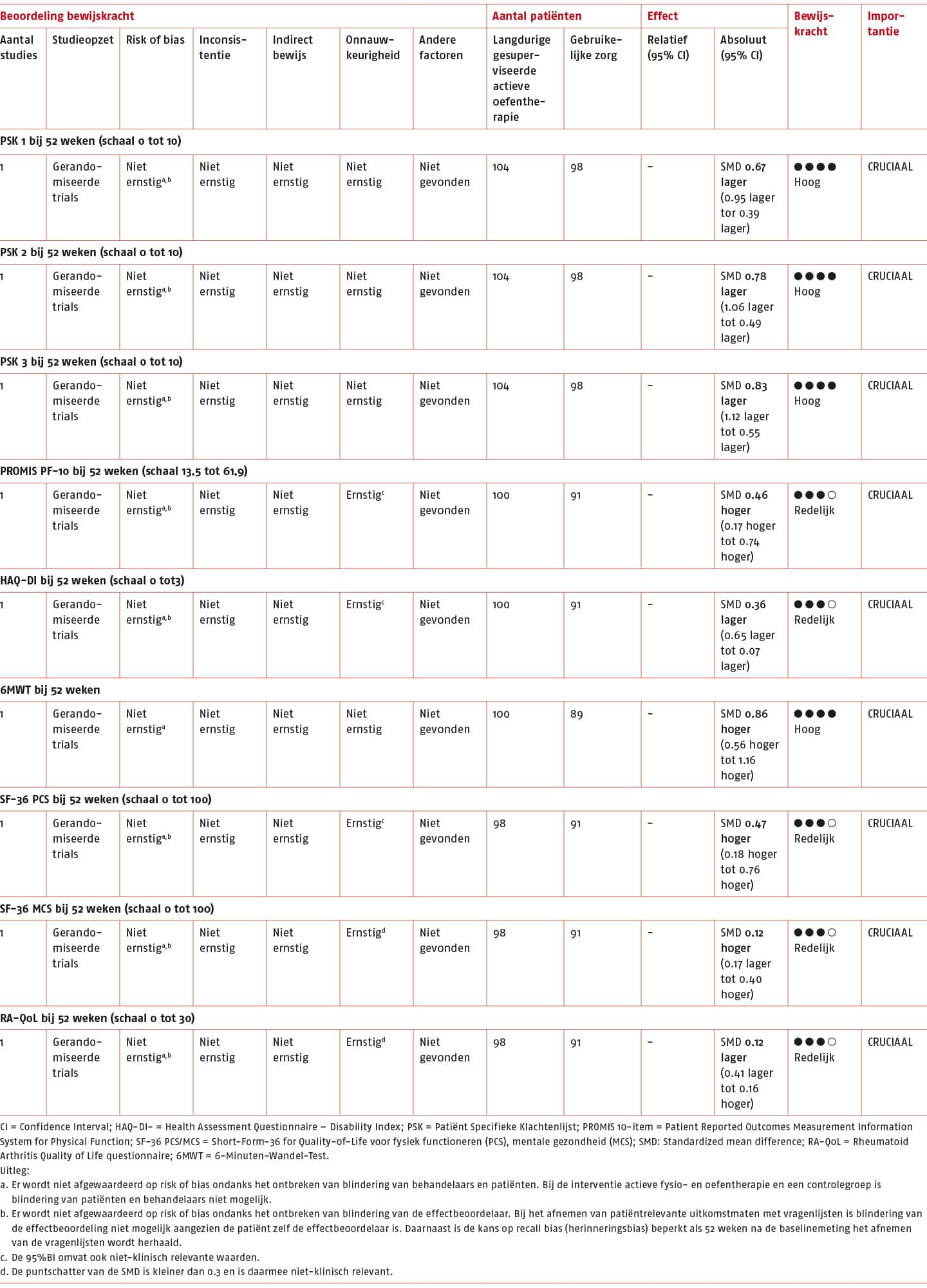
Fysiek functioneren op 52 weken – Zelf-gerapporteerd fysiek functioneren
PSK
In de L-EXTRA-studie is de effectiviteit van langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie vergeleken met gebruikelijke zorg gemeten op de PSK (14).
PSK 1 (eerst gerangschikte activiteit gescoord op de NRS).
Het gemiddelde verschil (MD) van de PSK 1 tussen de groepen op korte termijn was -1,70 punten (95% BI: -2,40 tot 1,00; n = 202) en daarmee is de SMD van de PSK 1 -0,67 (95% BI: -0,95 tot -0,39) in het voordeel van de interventiegroep.
Dit effect overschrijdt de vooraf gedefinieerde drempelwaarde (0,3) voor klinische relevantie.
De bewijskracht is niet verlaagd en komt daarmee tot hoog uit.
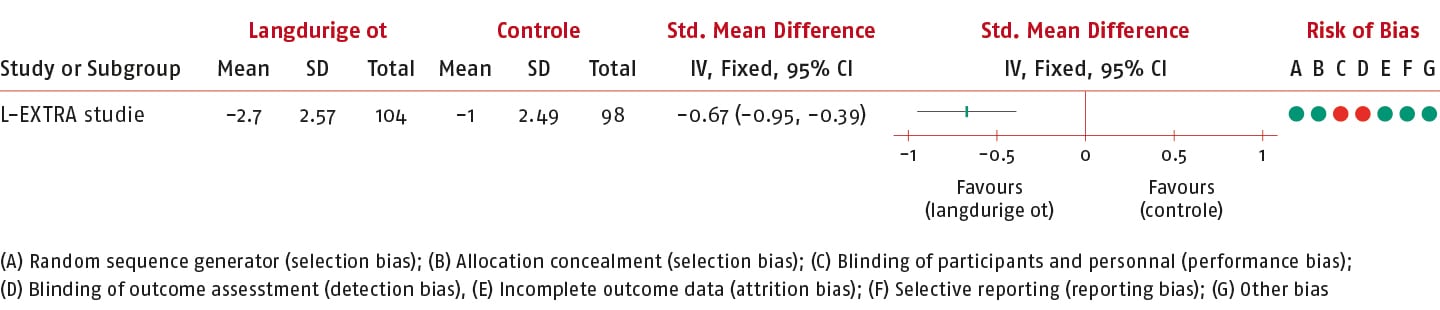
PSK 2 (opvolgende (tweede) gerangschikte activiteit gescoord op de NRS).
Het gemiddelde verschil (MD) van de PSK 2 tussen de groepen op korte termijn was -1,80 punten (95% BI: -2,43 tot 1,17; n = 202) en daarmee is de SMD van de PSK 2 -0,78 (95% BI: -1,06 tot -0,49) in het voordeel van de interventiegroep.
Dit effect overschrijdt de vooraf gedefinieerde drempelwaarde (0,3) voor klinische relevantie.
De bewijskracht is niet verlaagd en komt daarmee tot hoog uit.
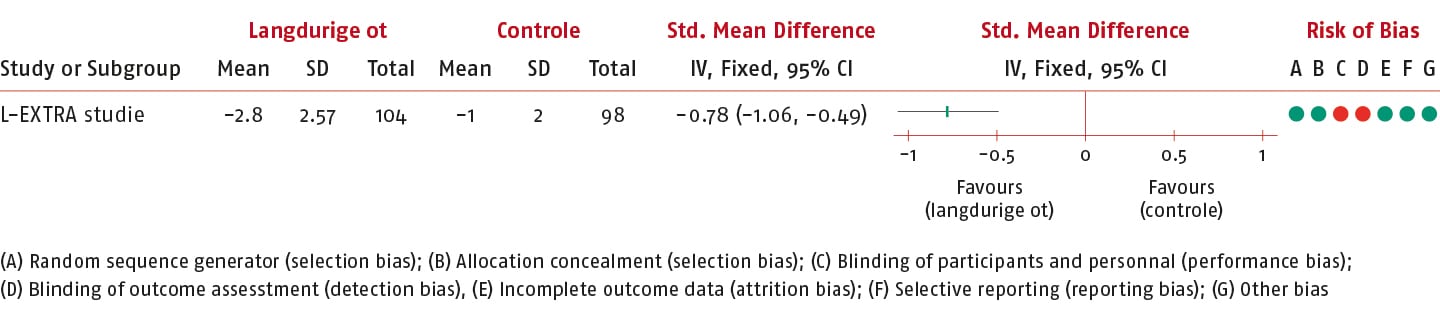
PSK 3 (opvolgende (derde) gerangschikte activiteit gescoord op de NRS).
Het gemiddelde verschil (MD) van de PSK 3 tussen de groepen op korte termijn was -1,70 punten (95% BI: -2,26 tot -1,14; n = 202) en daarmee is de SMD van de PSK 3 -0,83 (95% BI; -1,12 tot -0,55) in het voordeel van de interventiegroep.
Dit effect overschrijdt de vooraf gedefinieerde drempelwaarde (0,3) voor klinische relevantie.
De bewijskracht is niet verlaagd en komt daarmee tot hoog uit.
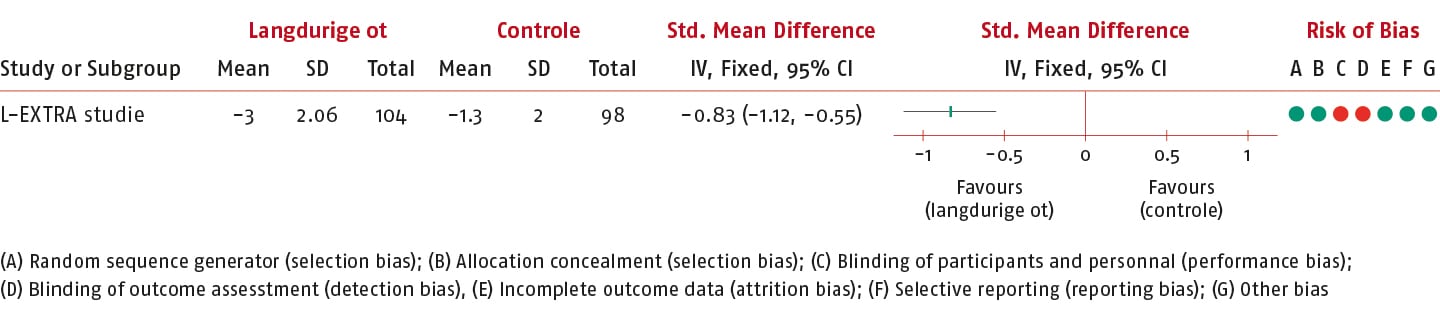
PROMIS PF-10
In de L-EXTRA-studie is de effectiviteit van langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie vergeleken met gebruikelijke zorg gemeten op de PROMIS PF-10 (14).
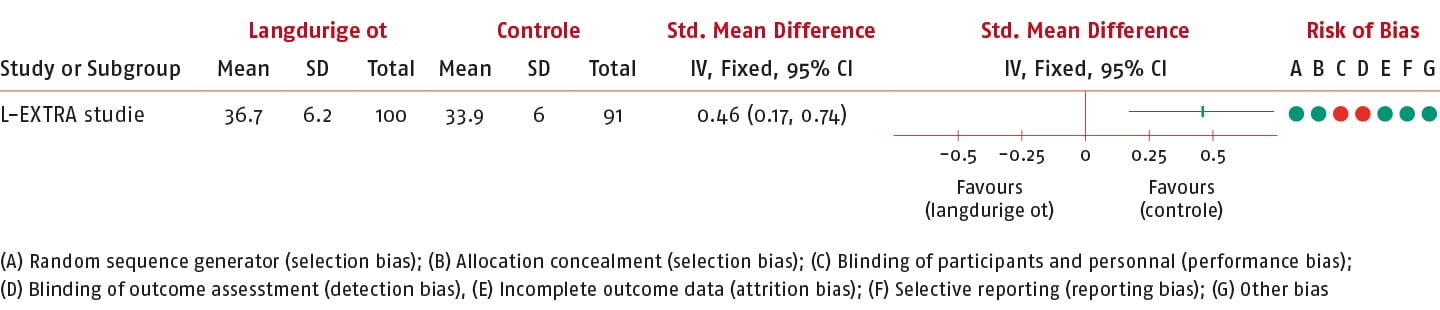
Het gemiddelde verschil (MD) van de PROMIS PF-10 is 2,80 punten (95% BI: 1,07 tot 4,53; n = 191) en daarmee is de SMD van de PROMIS PF-10 0,46 (95% BI: 0,17 tot 0,74) in het voordeel van de interventiegroep.
Dit effect overschrijdt de vooraf gedefinieerde drempelwaarde (0,3) voor klinisch relevantie.
De bewijskracht is verlaagd tot een redelijk niveau. Er is één keer afgewaardeerd vanwege onnauwkeurigheid.
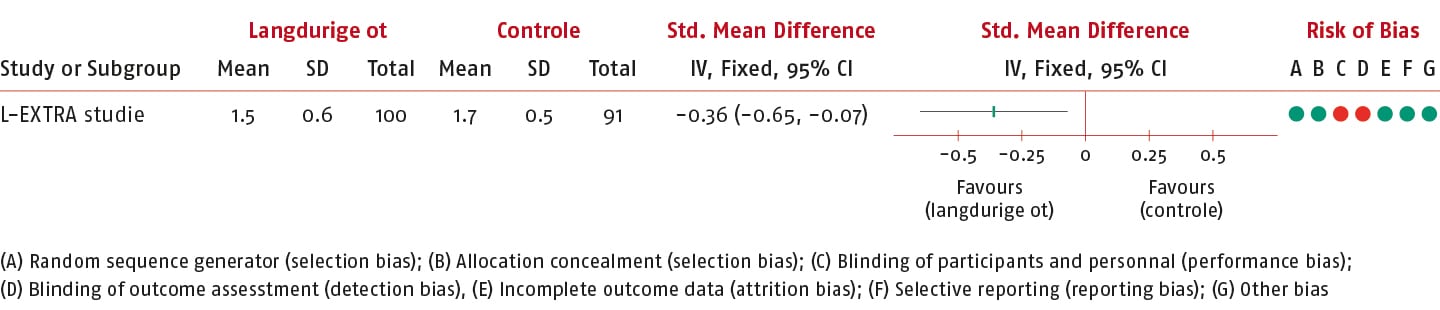
HAQ-DI
In de L-EXTRA-studie is de effectiviteit van langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie vergeleken met gebruikelijke zorg gemeten op de HAQ-DI (14).
Het gemiddelde verschil (MD) is -0,20 punten (95% BI: -0,36 tot -0,04) en daarmee is de SMD van de HAQ-DI -0,36 (95% BI: -0,65 tot -0,07) in het voordeel van de interventiegroep.
Dit effect overschrijdt de vooraf gedefinieerde drempelwaarde (0,3) voor klinisch relevantie.
De bewijskracht is verlaagd tot een redelijk niveau. Er is één keer afgewaardeerd vanwege onnauwkeurigheid.
Fysiek functioneren op 52 weken – Gemeten met fysieke testen
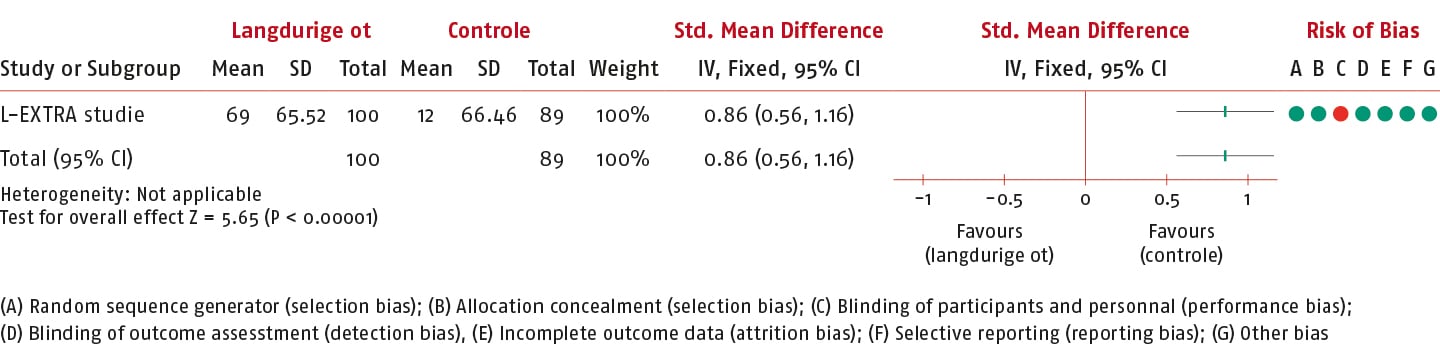
6MWT
In de L-EXTRA-studie is de effectiviteit van langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie vergeleken met gebruikelijke zorg gemeten op de 6MWT (14).
Het gemiddelde verschil (MD) van de 6MWT tussen de groepen op korte termijn was 57 punten (95% 37,14 tot 75,89; n = 189) en daarmee is de SMD van de 6MWT 0,86 (95% BI: 0,56 tot 1,16) in het voordeel van de interventiegroep.
Dit effect overschrijdt de vooraf gedefinieerde drempelwaarde (0,3) voor klinische relevantie.
De bewijskracht is niet verlaagd en komt daarmee tot hoog uit.
Kwaliteit van leven op 52 weken
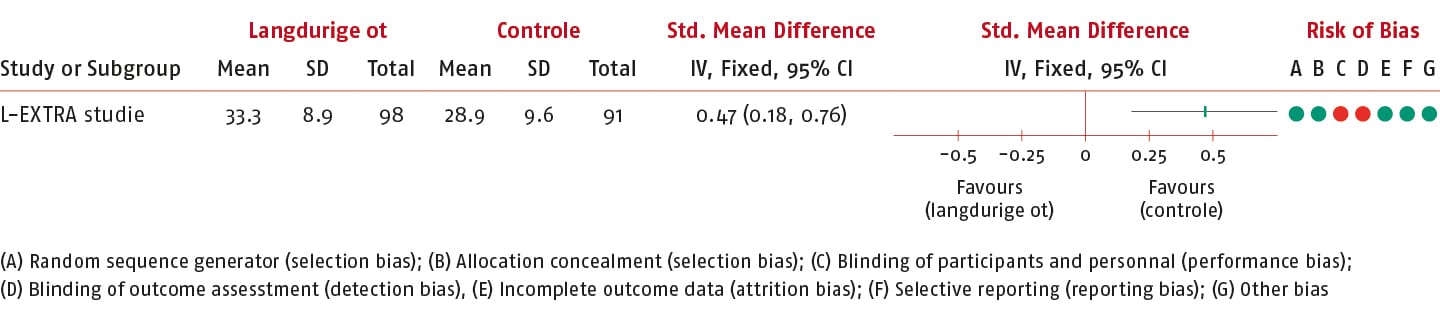
SF-36 Physical Component Score (PCS)
In de L-EXTRA-studie is de effectiviteit van langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie op kwaliteit van leven vergeleken met gebruikelijke zorg gemeten met de SF-36 PCS (14).
Het gemiddelde verschil (MD) van de SF-36 PCS tussen de groepen op korte termijn was 4,40 punten (95% BI: 1,75 tot 7,05; n = 189) en daarmee is de SMD van de SF-36 PCS 0,47 (95% BI: 0,18 tot 0,76) in het voordeel van de interventiegroep.
Dit effect overschrijdt de vooraf gedefinieerde drempelwaarde (0,3) voor klinische relevantie.
De bewijskracht is verlaagd tot een redelijk niveau. Er is één keer afgewaardeerd vanwege onnauwkeurigheid.
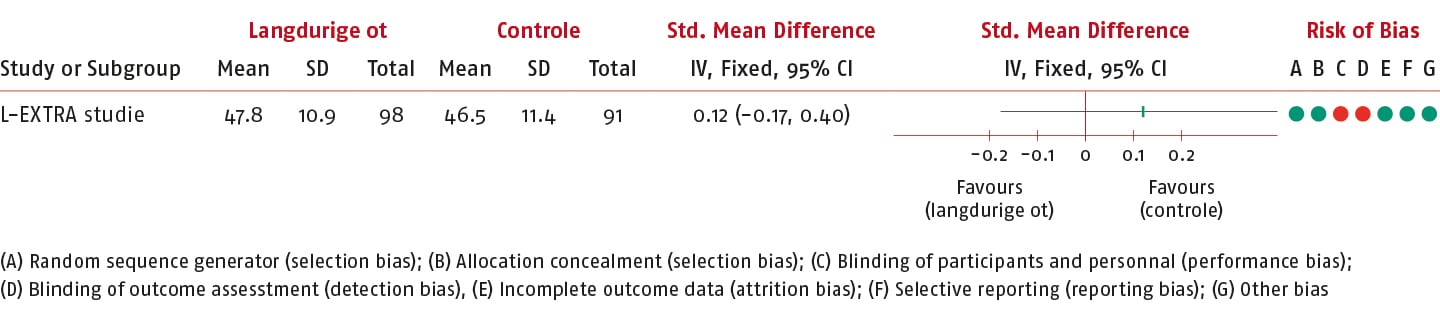
SF-36 Mental Component Score (MCS)
In de L-EXTRA-studie is de effectiviteit van langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie vergeleken met gebruikelijke zorg gemeten op de SF-36 MCS (10).
Het gemiddelde verschil (MD) van de SF-36 MCS tussen de groepen op korte termijn was 1,30 punten (95% BI: -1,88 tot 4,48; n = 189) en daarmee is de SMD van de SF-36 MCS 0,12 (95% BI: 0,17 tot 0,40) in het voordeel van de interventiegroep.
Dit effect overschrijdt de vooraf gedefinieerde drempelwaarde (0,3) voor klinische relevantie niet.
De bewijskracht is verlaagd tot een redelijk niveau. Er is één keer afgewaardeerd vanwege onnauwkeurigheid.
RA-QoL
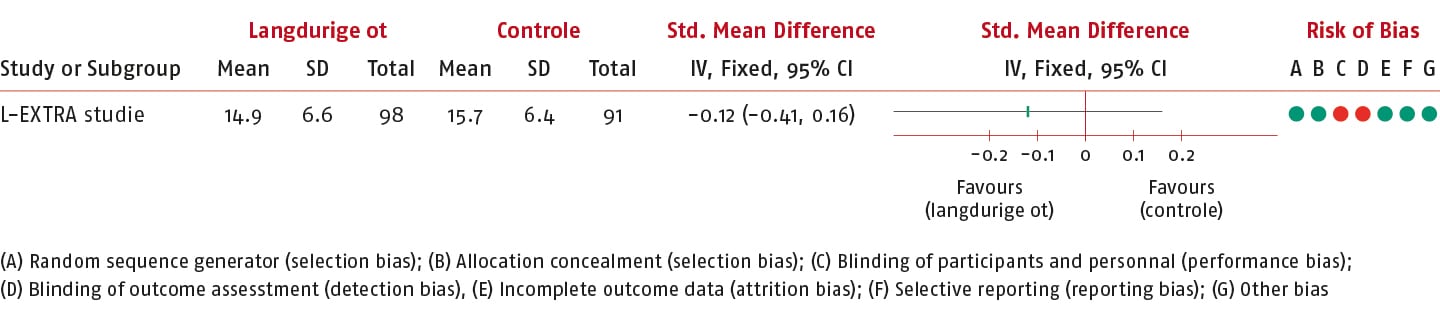
In de L-EXTRA-studie is de effectiviteit van langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie vergeleken met gebruikelijke zorg gemeten op de RA-QoL (10).
Het gemiddelde verschil (MD) van de RA-QoL tussen de groepen op korte termijn was -0,80 punten (95% BI: -2,66 tot 1,06; n = 189) en daarmee is de SMD van de RA-QoL -0,12 (95% BI: -0,41 tot 0,16) in het voordeel van de interventiegroep.
Dit effect overschrijdt de vooraf gedefinieerde drempelwaarde (0,3) voor klinische relevantie niet.
De bewijskracht is verlaagd tot een redelijk niveau. Er is één keer afgewaardeerd vanwege onnauwkeurigheid.
Belangrijke uitkomstmaten
(Ernstige) ongewenste ongevallen op 52 weken
Er werden geen ernstige ongewenste ongevallen gerapporteerd gedurende de 52 weken. Twee patiënten zijn overleden, maar niet in relatie tot de oefentherapiebehandeling (kanker). Eén ongewenst ongeval is gemeld in de interventiegroep, waarbij de patiënt duizelig en misselijk was gedurende de aerobe training. De symptomen verdwenen na 10 minuten rust en de behandeling is voortgezet.
Ervaren bijwerkingen en effecten
Spierpijn op 52 weken
Het optreden van spierpijn gerelateerd aan de interventie werd gemeld door 70% (n = 62 van 89) ten opzichte van spierpijn gerelateerd aan de gebruikelijke zorg 60% (n = 27 van 45). De gemiddelde ernst van de spierpijn was 3,9 (SD 2,2) en 4,3 (SD 2,6) in respectievelijk de interventiegroep en gebruikelijke zorggroepen.
Vermoeidheid op 52 weken
Het optreden van vermoeidheid gerelateerd aan de interventie werd gemeld door 71% (n = 63 van 89) ten opzichte van vermoeidheid gerelateerd aan de gebruikelijke zorg 64% (n = 29 van 45). De gemiddelde ernst van de vermoeidheid was 4,4 (SD 2,4) en 3,9 (SD 2,9) op een schaal van 1-10 in respectievelijk de interventiegroep en gebruikelijke zorggroepen.
Er zijn verder geen belangrijke uitkomstmaten gerapporteerd.
Conclusies op basis van de literatuur
Om de uitgangsvraag te kunnen beantwoorden, heeft de werkgroep de resultaten uit de geselecteerde literatuur gewogen. Weging vond plaats op basis van de grootte van het effect en de bewijskracht, waarna de resultaten gestandaardiseerd zijn geformuleerd. Deze gestandaardiseerde formuleringen zijn internationaal geaccepteerd en doen een uitspraak over de zekerheid van het bewijs dat in een bepaald onderzoek is gevonden (Langendam 2022).
Cruciale uitkomstmaten







Belangrijke uitkomstmaten

De werkgroep is van mening dat er geen relevante (serieuze) ernstige ongevallen zijn voorgevallen.

De werkgroep is van mening dat er geen relevante verschillen in ervaren bijwerkingen en effecten zijn tussen de interventie- en controlegroep.
Van bewijs naar aanbeveling – overwegingen
Van bewijs naar aanbeveling
Er zijn internationaal erkende criteria gehanteerd voor het beoordelen van het bewijs dat ten grondslag ligt aan de aanbevelingen. Deze criteria, evenals de overige overwegingen die de werkgroep formuleerde, bepalen de sterkte van de aanbeveling.
Het onderdeel van bewijs naar aanbeveling bevat de hieronder opgesomde criteria.
1. Gewenste effecten
De werkgroep beoordeelt de gewenste effecten van langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie ten opzichte van gebruikelijk zorg als:
- klinisch relevant voor het fysiek functioneren op 52 weken (zelf-gerapporteerd of gemeten met fysieke testen) met een hoge (PSK 1,2,3, 6MWT) of redelijke (PROMIS PF-10, HAQ-DI) bewijskracht.
- Niet klinisch relevant voor de kwaliteit van leven op 52 weken (SF-36 MCS, RA-QoL) met een redelijke bewijskracht, met uitzondering van de SF-36 PCS met een klinisch relevant verschil (redelijke bewijskracht).
Additionele gewenste effecten:
De effecten houden aan als de patiënten in de interventiegroep de langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie voortzetten, aangezien de scores tussen 52 en 104 weken vergelijkbaar blijven (4, 14).
2. Ongewenste effecten
Er is geen literatuur gevonden die rechtstreeks de bewijskracht definieert voor de ongewenste effecten.
Wel zijn de absolute getallen en effecten van (ernstige) ongewenste ongevallen, spierpijn en vermoeidheid (op 52 weken) beschreven in de L-EXTRA-studie(14).
De werkgroep beoordeelt de ongewenste effecten van langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie ten opzichte van gebruikelijk zorg als:
- niet klinisch relevant voor de (ernstige) ongewenste ongevallen (SAEs en AEs). De werkgroep beoordeelt de opgetreden SAEs niet in relatie staand met de langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie en de AEs als veelvoorkomende, accepteerbare, niet-risicovolle symptomen bij het aanbieden van oefentherapie.
- niet klinisch relevant voor de ervaren bijwerkingen en effecten. De werkgroep beoordeelt de ervaren bijwerkingen en effecten (spierpijn en vermoeidheid) als een logisch en niet ernstig gevolg van oefentherapie en deze worden daarom als een niet relevant ongewenst effect beschouwd. Dit wordt bevestigd door de data vanuit de L-EXTRA-studie. Hierin is gekeken naar ervaren effect, tevredenheid met de behandeling en ervaren bijwerking (zie bijlage C.2.3-7 (opent in nieuw tabblad)). Hierin zien we dat het waargenomen effect op de dimensie pijn als 3 (mediaan, (2-3 IQR)) en de dimensie vermoeidheid ook als 3 (mediaan, (2,5, 4 IQR)) wordt beschreven, waarbij 1 een zeer sterk verbeterd en 7 een zeer sterk verslechterd effect betekent. De ernst van de spierpijn en vermoeidheid wordt respectievelijk als 4,0 (mean, 2,4 SD ) en 4,8 (mean, 2,8 SD) beschreven, waarbij 0 geen en 10 zeer ernstige spierpijn beschrijft.
3. Kwaliteit van bewijs
De werkgroep beoordeelt de bewijskracht van de gewenste effecten als redelijk tot hoog.
Er is geen bewijskracht gedefinieerd voor ongewenste effecten, maar de werkgroep beoordeelt dat er geen belangrijke bijwerkingen zijn vastgesteld.
4. Waarden en voorkeuren van patiënten
De werkgroep heeft de ervaring dat de patiënten grote waarde hechten aan de interventie. De ervaring is dat RA-patiënten gemotiveerd zijn om te oefenen (104 van de 109 patiënten volgden de interventie na 52 weken)en daarbij behoefte hebben aan langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie. De ervaring is ook dat RA-patiënten met ernstige functionele beperkingen óók na 52 weken een actieve hulpvraag hebben en daarbij ondersteuning wensen van de fysio- of oefentherapeut.
Deze ervaring wordt bevestigd door data vanuit de L-EXTRA-studie (zie bijlage C.2.3-7 (opent in nieuw tabblad)). Hierin zien we dat het globaal waargenomen effect als 2 (mediaan (IQR: 2-3)) wordt beschreven, waarbij 1 een zeer sterk verbeterd en 7 een zeer sterk verslechterd effect betekent.
5. Balans gewenste en ongewenste effecten
De werkgroep is tot het volgende oordeel gekomen:
De gewenste effecten overtreffen zeker de ongewenste effecten. De motivatie hiervoor is dat bij patiënten met RA met ernstige functionele beperkingen, langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie resulteert in klinisch relevante effecten op de cruciale uitkomsten fysiek functioneren en kwaliteit van leven en geen (belangrijke) bijwerkingen geeft.
Het is van belang te benoemen dat de balans is opgemaakt op basis van de bevindingen van één studie, waardoor deze bevindingen met enige onzekerheid geïnterpreteerd moeten worden. Echter omdat deze studie een kwalitatief goede studie is, en er geen ander bewijs is, vindt de werkgroep het formuleren van een sterke aanbeveling gepast.
6. Economische overwegingen en kosteneffectiviteit
In de L-EXTRA-studie is ook een economische evaluatie uitgevoerd (4).De onderzoekers hebben hierbij de volgende resultaten beschreven.
Kosteneffectiviteitsanalyse
Kwaliteit van leven is gemeten met de EQ-5D-5L-vragenlijst, waarbij gebruik is gemaakt van de Nederlandse tarieven, zoals aanbevolen door de Nederlandse richtlijn voor economische evaluaties (16).
De kosteninformatie is verzameld vanuit een maatschappelijk perspectief. Identificatie en volume van de meest relevante kosteenheden zijn verzameld met behulp van de Productivity Cost Questionaire (iPCQ)- en Medical Consumption Questionaire (iMCQ)-vragenlijst.
Uit de analyse van de onderzoekers blijkt dat de patiënten die gepersonaliseerde gesuperviseerde actieve oefentherapie ontvingen, in het eerste jaar geen significante verschillen in kwaliteit van leven en kosten hadden ten opzichte van de gebruikelijke zorg.
De onderzoekers rapporteren een verschil in kwaliteit van leven van 0,02 QALY per patiënt (95% BI: -0,05 tot 0,09) in het voordeel van de interventiegroep.
De meerkosten van langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie (totale kosten: € 26.441) ten opzichte van de gebruikelijke zorg (totale kosten: € 26.261) vanuit een maatschappelijk perspectief bedragen € 180 (95% BI: -€ 4.493 tot € 4.852) per patiënt.
Dit resulteert in een incrementele kosteneffectiviteitsratio (ICER) van € 9.000/QALY.
Het Zorginstituut Nederland hanteert een referentiewaarde van € 50.000/QALY op basis van de ziektelast voor deze patiëntengroep.
Op basis van de base case analysis is de kans dat de interventie kosteneffectief is 53%, 60% en 64% voor een referentiewaarde van respectievelijk € 20.000/QALY, € 50.000/QALY en € 80.000/QALY, waarbij QALY staat voor quality-adjusted life year (voor kwaliteit van leven gecorrigeerde levensjaren).. De onderzoekers rapporteren hierbij dat de berekende ICER door het gebrek aan statistisch significante verschillen in kosten en effecten onzeker is.
Aangezien de indicatie een chronische aandoening betreft en de functionele beperkingen van permanente aard zijn, is het waarschijnlijk dat langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie ook chronisch toegepast zal gaan worden. Dit zorgt voor extra onzekerheid over de effecten van de behandeling op kwaliteit van leven en kosten over de periode na 1 jaar.
Budgetimpactanalyse (BIA)
Voor de berekening van de budgetimpact is ervan uitgegaan dat er in Nederland 3.750 tot 4.500 patiënten per jaar, met RA en ernstige functionele beperkingen, in aanmerking komen voor langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie. Daarnaast is ervan uitgegaan dat een patiënt in het eerste jaar gemiddeld 39 behandelingen ontvangt en in het tweede jaar 20 behandelingen, gebaseerd op de L-EXTRA-studie (14). Ook is rekening gehouden met een afname van het aantal patiënten vanaf het tweede jaar van 30% (14).
Zie bijlage 6 voor de tabellen van de BIA. Op basis hiervan is de budgetimpact op een bedrag tussen de € 3,7 en € 4,4 miljoen in het eerste jaar vastgesteld. Uitbreiding van het basispakket, met langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie voor patiënten met RA en ernstige functionele beperkingen, kost vanaf het tweede behandeljaar naar schatting tussen de € 0,8 en € 0,9 miljoen per jaar.
Hierbij kan worden opgemerkt dat in deze raming geen rekening gehouden is met de uitgaven aan (minder) complicaties en andere indirecte kosten, omdat precieze gegevens hierover ontbreken. Daarnaast is een deel van de patiënten gediagnosticeerd met RA voordat verbeterde medicamenteuze behandeling (rond 2000) beschikbaar kwam. Er wordt verwacht dat de aanwas van deze patiënten zal afnemen (4).
De werkgroep beoordeelt dat de kosteneffectiviteit van langdurige gepersonaliseerde gesuperviseerde actieve
oefentherapie ten opzichte van gebruikelijke zorg bij patiënten met RA met ernstige functionele beperkingen, onzeker is.
Voor fysio- en oefentherapeuten wordt de eis gesteld dat zij een verplichte scholing volgen om deze specifieke patiëntengroep te kunnen behandelen. De kosten die hiermee gepaard gaan, zijn wel een investering, echter de werkgroep ervaart deze als laag. De werkgroep beoordeelt de benodigde middelen voor de interventie als verwaarloosbaar.
7. Gelijkheid
De werkgroep verwacht dat het aanbevelen van de interventie niet zal leiden tot een toename of afname van de gezondheidsgelijkheid. Hierbij wordt ervan uitgegaan dat de fysio- of oefentherapeutische zorg van patiënten met RA met ernstige functionele beperkingen, al is opgenomen in het basispakket. Het wel of niet toepassen van deze specifieke interventie, binnen het basispakket, heeft (ook voor specifieke patiëntencategorieën) geen gevolgen.
8. Aanvaardbaarheid
De werkgroep verwacht dat de interventie door alle key stakeholders zal worden geaccepteerd. De middelen die van de therapeut nodig zijn (tijd en trainingsinvestering), worden door de werkgroep als verwaarloosbaar beschouwd en wegen op tegen het mogen toepassen van deze interventie bij deze specifieke patiëntengroep.
9. Haalbaarheid
De implementatie van langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie wordt door de werkgroep als waarschijnlijk wel realistisch beoordeeld, indien de therapeut beschikt over de juiste competenties. De werkgroep geeft echter aan dat het een belemmerende factor kan zijn dat er voor fysio- of oefentherapeuten een verplichte training is vereist voordat zij patiënten met RA met ernstige functionele beperkingen, vanuit het basispakket kunnen behandelen.
Voor fysio- of oefentherapeuten betekent dit dat zij moeten investeren in het volgen van een training, wat hen mogelijk ervan weerhoudt om dit te doen.
Voor patiënten kan het betekenen dat zij geen fysio- of oefentherapeut in de buurt kunnen vinden om hen te behandelen. Daarnaast kan het betekenen dat zij bij hun vertrouwde therapeut, bij wie ze al onder behandeling zijn (bijv. vanwege comorbiditeit) de behandeling niet voort kunnen zetten.
Eventuele additionele overwegingen
Er zijn geen additionele overwegingen geformuleerd.
Aandachtspunten voor implementatie
Zie het onderdeel ‘haalbaarheid’.
Kennislacunes
De werkgroep is van mening dat er meer onderzoek uitgevoerd zou moeten worden naar dezelfde onderzoeksvraag, waardoor de effecten niet enkel berusten op één onderzoek.
Overige informatie C.2.3
Initiatiefnemers
Het initiatief voor deze modulaire herziening lag bij het Koninklijk Nederlands Genootschap Fysiotherapie (KNGF), in samenwerking met de Vereniging van Oefentherapeuten Cesar en Mensendieck (VvOCM).
Betrokkenheid van belanghebbenden (auteurs)
Voor het ontwikkelen van de richtlijnmodule is in 2024 een projectgroep samengesteld, bestaande uit een kerngroep en een multidisciplinaire werkgroep. De werkgroep bestaat uit vertegenwoordigers van alle primair betrokken professionals bij de zorg voor RA. De werkgroep werd ondersteund in de ontwikkeling door richtlijnadviseurs vanuit het KNGF en de VvOCM.
De rollen en taken van de belanghebbenden van de richtlijn worden beschreven in de KNGF-richtlijnenmethodiek (8).
Richtlijnadviseurs KNGF en VvOCM
Werkgroep
Belangen
Voorafgaand aan en bij afsluiting van het project hebben alle projectgroep leden een belangenverklaring ingevuld. De belangenverklaringen zijn beoordeeld door de richtlijnadviseurs en indien nodig (bij een ‘conflict of interest’) werden gedurende het richtlijnproject maatregelen getroffen (bijv. het niet participeren in het proces ‘van bewijs naar aanbeveling’ in de werk- of klankbordgroep) om (schijn van) oneigenlijke beïnvloeding door belangenverstrengeling zo veel mogelijk te voorkomen, conform de KNGF-richtlijnenmethodiek 2022. (9)
In de belangenverklaringen is een overzicht opgenomen met de affiliaties (de organisatie of instelling en plaats van werkzaamheden) van de leden van de projectgroep.
Autoriserende partijen
De volgende partijen hebben deze module geautoriseerd:
- Koninklijk Nederlands Genootschap Fysiotherapie (KNGF);
- Vereniging van Oefentherapeuten Cesar en Mensendieck (VvOCM);
- Nederlandse Vereniging voor Reumatologie (NVR);
- ReumaNederland;
- Vereniging voor Sportgeneeskunde (VSG);
- Nationale Vereniging Reumazorg Nederland.
De volgende partij heeft een verklaring van geen bezwaar afgegeven:
- Nederlands Huisartsen Genootschap (NHG).
Geldigheid en onderhoudsprocedure
Publicatiedatum:5 december 2024
Laatst beoordeeld:5 december 2024
Laatst geautoriseerd:5 december 2024
De eerstvolgende beoordeling op actualiteit vindt plaats in 2029.
Zie de KNGF-richtlijnenmethodiek voor informatie over het beleid wat betreft richtlijnenonderhoud.
Financiering
De ontwikkeling van deze module is gefinancierd door het KNGF.
Toepassing van de KNGF-richtlijnenmethodiek
De ontwikkeling van deze module heeft plaatsgevonden volgens de KNGF-richtlijnenmethodiek 2022. Deze methodiek is gebaseerd op het AGREE II-instrument en de AQUA-leidraad. Binnen de KNGF-richtlijnenmethodiek wordt gebruikgemaakt van GRADE voor de beoordeling van de bewijskracht en voor het proces van ‘evidence to decision’(18).
Bijlagen bij C.2.3
Bronnen C.2.3
- Wettenbank On. Bijlage 1. van het Besluit zorgverzekering 2012. Available from: https://wetten.overheid.nl/BWBR0018492/2006-10-01/3/#Bijlage1.
- Nederland Z. Pakketadvies fysiotherapie en oefentherapie bij artrose aan heup en knie, reumatoïde artritis en spondyloartritis en radiculair syndroom (hernia) met motorische uitval 2017. Available from: https://www.zorginstituutnederland.nl/publicaties/adviezen/2017/03/08/pakketadvies-fysiotherapie-en-oefentherapie-bij-artrose-aan-heup-en-knie-reumatoide-artritis-en-spondyloartritis-en-radiculair-syndroom-hernia-met-motorische-uitval.
- van Wissen MAT, Teuwen MMH, van den Ende CHM, Vliet Vlieland TPM, den Broeder AA, van den Hout WB, et al. Effectiveness and cost-effectiveness of longstanding exercise therapy versus usual care in patients with axial spondyloarthritis or rheumatoid arthritis and severe limitations: The protocols of two parallel randomized controlled trials. Physiother Res Int. 2022;27(1):e1933.
- Nederland Z. Advies Langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie bij patiënten met reumatoïde artritis met ernstige functionele beperkingen 2024. Available from: https://www.zorginstituutnederland.nl/publicaties/adviezen/2024/02/27/advies-langdurige-persoonsgerichte-actieve-ot-bij-ernstige-ra.
- Nederland Z. Beoordeling Stand van de wetenschap en praktijk. Langdurige gesuperviseerde actieve oefentherapie bij patiënten met reumatoïde artritis met ernstige functionele beperkingen. 2023.
- Salaffi F, Stancati A, Silvestri CA, Ciapetti A, Grassi W. Minimal clinically important changes in chronic musculoskeletal pain intensity measured on a numerical rating scale. Eur J Pain. 2004;8(4):283-91.
- Beurskens AJ, de Vet HC, Köke AJ, Lindeman E, van der Heijden GJ, Regtop W, et al. A patient-specific approach for measuring functional status in low back pain. J Manipulative Physiol Ther. 1999;22(3):144-8.
- Hurkmans EJ, Peter WFH, Swart N, Meerhoff GA, Vliet Vlieland TPM. KNGF-richtlijn Reumatoïde artritis Amersfoort: Koninklijk Nederlands Genootschap voor Fysiotherapie (KNGF); 2018 .
- Bruce B, Fries JF. The Stanford Health Assessment Questionnaire: dimensions and practical applications. Health Qual Life Outcomes. 2003;1:20.
- Jones CJ, Rikli RE. Measuring functional fitness of older adults. The Journal on Active Aging. 2002;March April:24-30.
- Kosak M, Smith T. Comparison of the 2-, 6-, and 12-minute walk tests in patients with stroke. J Rehabil Res Dev. 2005;42(1):103-7.
- Steffen TM, Hacker TA, Mollinger L. Age- and gender-related test performance in community-dwelling elderly people: Six-Minute Walk Test, Berg Balance Scale, Timed Up & Go Test, and gait speeds. Phys Ther. 2002;82(2):128-37.
- Ware JE, Jr., Sherbourne CD. The MOS 36-item short-form health survey (SF-36). I. Conceptual framework and item selection. Med Care. 1992;30(6):473-83.
- Teuwen MMH, van Weely SFE, Vliet Vlieland TPM, van Wissen MAT, Peter WF, den Broeder AA, et al. Effectiveness of longstanding exercise therapy compared with usual care for people with rheumatoid arthritis and severe functional limitations: a randomised controlled trial. Ann Rheum Dis. 2024;83(4):437-45.
- Higgins JPT, Green S. Cochrane Handbook for Systematic Reviews of Interventions: The Cochrane Collaboration; 2011 [updated March 2011. Version 5.1.0. [Available from: www.cochrane-handbook.org (opent in nieuw tabblad).
- Nederland Z. Richtlijn voor het uitvoeren van economische evaluaties in de gezondheidszorg. Diemen 2015.
- Zorginstituut Nederland. AQUA-Leidraad: Zorginstituut Nederland; 2021. Available from: https://www.zorginzicht.nl/ontwikkeltools/ontwikkelen/aqua-leidraad.
- Koninklijk Nederlands Genootschap voor Fysiotherapie, Vreeken H, Van Doormaal MCM, Conijn D, Meerhoff G, Swart N. KNGF-richtlijnenmethodiek: ontwikkeling en implementatie van KNGF-richtlijnen, versie 3 Amersfoort: Koninklijk Nederlands Genootschap voor Fysiotherapie (KNGF); 2022. Available from: https://www.kngf.nl/kennisplatform/richtlijnen.
- Koninklijke Nederlandse Akademie van Wetenschappen. Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling 2016 [cited 2024 24 mei]. Available from: https://www.knaw.nl/nl/publicaties/code-ter-voorkoming-van-oneigenlijke-beinvloeding-door-belangenverstrengeling.
- Vreeken H, Van Doormaal MCM, Conijn D, Meerhoff G, Swart N. KNGF-richtlijnenmethodiek: ontwikkeling en implementatie van KNGF-richtlijnen, versie 3 Amersfoort: Koninklijk Nederlands Genootschap voor Fysiotherapie (KNGF); 2022. Richtlijnontwikkeling | Kennisplatform Fysiotherapie
C.3 Frequentie, intensiteit, type en duur van oefentherapie
Ter ondersteuning van de invulling van de oefentherapie zijn er aanbevelingen geformuleerd ten aanzien van de frequentie, intensiteit, type en duur van de oefentherapie.
Onderbouwing
Noot 14
Uitgangsvraag
Welke frequentie, intensiteit, type en duur van de oefentherapeutische interventies wordt aanbevolen bij patiënten met RA?
Om deze uitgangsvraag te beantwoorden, is een zoekactie uitgevoerd, waarna de literatuur is onderverdeeld over de verschillende FITT-factoren. De resultaten zijn aangevuld met bevindingen uit de richtlijnen voor oefentherapie bij artritis van de ‘American College of Sports Medicine’ (ACSM).[1]
Bij de beoordeling van de literatuur en het proces ‘van bewijs naar aanbeveling’ is onderscheid gemaakt tussen de frequentie (zie noot 15), de intensiteit (zie noot 16), het type (zie noot 17) en de duur (zie noot 18) van de oefentherapie.
Complete uitgangsvraag volgens PICO
Welke frequentie, intensiteit, type en duur van de oefentherapeutische interventies (I) worden aanbevolen, vergeleken met een oefentherapeutische interventie met een andere frequentie, intensiteit, type of duur (C) bij patiënten met RA (P) ter verbetering van de kwaliteit van leven, fysiek functioneren, pijn, vermoeidheid, aerobe capaciteit, spierkracht, range of motion, ziekte activiteit, radiologische schade en arbeidsproductiviteit (O)?
Zoekstrategie
Er is door het KNGF op 3 maart 2017 een zoekactie uitgevoerd naar samenvatting van de literatuur (i.e. systematische literatuurstudie) en gerandomiseerde gecontroleerde onderzoeken naar oefentherapie bij patiënten met RA. Details van deze zoekactie staan beschreven in de volgende tabel. De zoektermen (algemeen voor alle FITT-factoren) zijn opgenomen in de bijlage van deze noot.
Selectiecriteria systematische literatuurstudie FITT-factoren.
| Type studie | RCT’s |
|---|---|
| Type patiënt | volwassenen met de diagnose reumatoïde artritis volgens de ARA or ACR/EULAR classificatiecriteria |
| Type interventie | elke vorm van oefentherapie |
| Type vergelijking | elke vorm van oefentherapie waarbij er een verschil is in duur, frequentie, intensiteit, opbouw, type oefeningen of vorm |
| Type uitkomst | cruciale uitkomstmaten: kwaliteit van leven, fysiek functioneren, pijn*, vermoeidheid belangrijke uitkomstmaten: aerobe capaciteit, spierkracht, range of motion, ziekteactiviteit*, radiologische schade*, arbeidsproductiviteit |
| Type tijdslijn | direct na de interventie |
Gevonden literatuur
De zoekactie van de literatuur leverde 1837 referenties op. Twaalf gerandomiseerde gecontroleerde onderzoeken voldeden aan de inclusiecriteria voor de beantwoording van de uitgangsvraag met betrekking tot de FITT-factoren.1-12 Zie ook de resultaten van de literatuurstudies van de frequentie, intensiteit, type en duur van de oefentherapie (noot 15 t/m 18). Algemene aanbevelingen voor oefentherapie beschreven staan in noot 19.
1. Bostrom C, Harms-Ringdahl K, Karreskog H, Nordemar R. Effects of static and dynamic shoulder rotator exercises in women with rheumatoid arthritis: a randomised comparison of impairment, disability, handicap, and health. Scand J Rheumatol. 1998;27(4):281-90.
2. Ekdahl C, Andersson SI, Moritz U, Svensson B. Dynamic versus static training in patients with rheumatoid arthritis. Scand J Rheumatol. 1990;19(1):17-26.
3. van den Ende CHM, Hazes JMW, le Cessie S, Mulder WJ, Belfor DG, Breedveld FC, Dijkmans BA. Comparison of high and low intensity training in well controlled rheumatoid arthritis. Results of a randomized clinical trial. Ann Rheum Dis. 1996;55(11):798-805.
4. van den Ende CHM, Breedveld FC, le Cessie S, Dijkmans BAC, de Mug AW, Hazes JMW. Effect of intensive exercise on patients with active rheumatoid arthritis: a randomised clinical trial. Ann Rheum Dis. 2000;59:615-21.
5. Harkcom TM, Lampman RM, Banwell BF, Castor CW. Therapeutic value of graded aerobic exercise training in rheumatoid arthritis. Arthr Rheum. 1985;28(1):32-9.
6. Minor MA, Hewett JE, Webel RR, Anderson SK, Kay DR. Efficacy of physical conditioning exercise in patients with rheumatoid arthritis and osteoarthritis. Arthritis Rheum. 1989;32(11):1396-405.
7. Dogu B, Sirzai H, Yilmaz F, Polat B, Kuran B. Effects of isotonic and isometric hand exercises on pain, hand functions, dexterity and quality of life in women with rheumatoid arthritis. Rheumatol Int. 2013;33(10):2625-30,
8. Cima SR, Barone A, Porto JM, de Abreu DC. Strengthening exercises to improve hand strength and functionality in rheumatoid arthritis with hand deformities: a randomized, controlled trial. Rheumatol Int. 2013;33(3):725-32.
9. Lamb SE, Williamson EM, Heine PJ, Adams J, Dosanjh S, Dritsaki M, et al. Exercises to improve function of the rheumatoid hand (SARAH): a randomised controlled trial. Lancet. 2015;385(9966):421-9.
10. O’Brien AV, Jones P, Mullis R, Mulherin D, Dziedzic K. Conservative hand therapy treatments in rheumatoid arthritis-a randomized controlled trial. Rheumatology (Oxford). 2006;45(5):577-83.
11. Minor MA, Hewett JE, Webel RR, Anderson SK, Kay DR. Efficacy of physical conditioning exercise in patients with rheumatoid arthritis and osteoarthritis. Arthritis and Rheumatism 1989;32(11):1396-405.
12. Siqueira US, Orsini Valente LG, de Mello MT, Szejnfeld VL, Pinheiro MM. Effectiveness of aquatic exercises in women with rheumatoid arthritis: a randomized, controlled, 16-week intervention-the HydRA Trial. Am J Phys Med Rehabil. 2017 Mar;96(3):167-75.
C.3.1 Frequentie
Aanbeveling Streef naar de volgende frequentie om tevens te voldoen aan de ‘Beweegrichtlijn van de Gezondheidsraad’:
- Spierkrachtoefeningen en/of activiteiten: Bij voorkeur dagelijks, maar minimaal twee dagen per week training van een specifieke spiergroep. Hanteer na een intensieve spierkrachttraining voor de getrainde spiergroep een herstelperiode van 48 uur. Stem de opbouw af op de belastbaarheid van de patiënt.
- Aerobe oefeningen en/of activiteiten: Bij voorkeur dagelijks, maar minimaal vijf dagen per week gedurende ten minste 30 minuten per keer. Stem de opbouw af op de belastbaarheid van de patiënt.
- Functionele oefeningen en/of activiteiten: Bij voorkeur dagelijks, maar minimaal twee dagen per week. Besteed tevens aandacht aan botversterkende oefeningen. Stem de opbouw af op de belastbaarheid van de patiënt.
Onderbouwing
Noot 15
Uitgangsvraag
Welke frequentie van oefentherapie wordt aanbevolen bij patiënten met RA?
Conclusie vanuit de literatuurstudie
De literatuur toont een groot effect voor oefentherapie met een frequentie van twee keer per week op de uitkomstmaten ‘kwaliteit van leven’ (lage kwaliteit van bewijs) en ‘fysiek functioneren’ (redelijke kwaliteit van bewijs). Het effect van oefentherapie met een frequentie van drie keer per week is onbekend voor ‘kwaliteit van leven’ en gering voor ‘fysiek functioneren’ (lage kwaliteit van bewijs). Het effect van oefentherapie met een frequentie van vier à vijf keer per week op ‘kwaliteit van leven’ en ‘fysieke functioneren’ is onbekend.
Van bewijs naar aanbeveling
Op basis van de omvang van de effectschattingen en het kwaliteit van bewijs, die in het voordeel zijn van een frequentie van twee keer per week ten opzichte van een frequentie van drie keer, of vier tot vijf keer per week, is de werkgroep van mening dat een frequentie van twee keer per week begeleide oefentherapie de voorkeur verdient (bij indicatie 2), aangevuld met zelfstandig uitgevoerde oefeningen.
Op basis van de ACSM-richtlijnen [20] wordt hieraan toegevoegd dat spierkracht of functionele oefeningen en/of activiteiten bij voorkeur dagelijks, maar minimaal twee dagen per week geadviseerd worden en aerobe oefeningen en/of activiteiten bij voorkeur dagelijks, maar minimaal vijf dagen per week ten minste 30 minuten per keer, om tevens te voldoen aan de ‘Beweegrichtlijnen van de Gezondheidsraad’.
Aanbeveling voor de frequentie van de oefentherapie
Streef naar de volgende frequentie om tevens te voldoen aan de ‘Beweegrichtlijn van de Gezondheidsraad’:
- Spierkrachtoefeningen en/of activiteiten. Bij voorkeur dagelijks, maar minimaal twee dagen per week training van een specifieke spiergroep. Hanteer na een intensieve spierkrachttraining voor de getrainde spiergroep een herstelperiode van 48 uur. Stem de opbouw af op de belastbaarheid van de patiënt.
- Aerobe oefeningen en/of activiteiten. Bij voorkeur dagelijks, maar minimaal vijf dagen per week gedurende ten minste 30 minuten per keer. Stem de opbouw af op de belastbaarheid van de patiënt.
- Functionele oefeningen en/of activiteiten. Bij voorkeur dagelijks, maar minimaal twee dagen per week. Besteed tevens aandacht aan botversterkende oefeningen. Stem de opbouw af op de belastbaarheid van de patiënt.
Complete uitgangsvraag volgens PICO
Voor de beantwoording van deze uitgangsvraag is een gezamenlijke PICO uitgangsvraag geformuleerd voor de frequentie, intensiteit, type en duur van oefentherapie (zie noot 14).
Zoekstrategie
Er is een gezamenlijke zoekactie uitgevoerd voor de frequentie, intensiteit, type en duur van oefentherapie (zie noot 14).
Gevonden literatuur
Er zijn geen gerandomiseerde gecontroleerde onderzoeken gevonden waarin een vergelijking is gemaakt in de frequentie van oefentherapie (zie noot 14). Om toch een aanbeveling te kunnen formuleren over de frequentie is een subgroepanalyse uitgevoerd met de geïncludeerde studies voor de uitgangsvraag over oefentherapie, om te bepalen welke frequentie het optimale resultaat oplevert.
Beschrijving studies
Van de 19 geïncludeerde studies naar de effectiviteit van oefentherapie hadden tien studies een frequentie van twee keer per week [3-7, 10, 12-14, 18], zeven studies een frequentie van drie keer per week [8,9.11,15-17,19] en twee studies een frequentie van vier tot vijf keer per week.[1,2] De karakteristieke van de studies worden beschreven in noot 10.
Effectiviteit en bewijskracht
De beoordeling van de onderzoeksopzet en uitvoering per studie is opgenomen in de bijlage (opent in nieuw tabblad) van deze noot.
Hierna volgt per uitkomstmaat een beschrijving van de effectiviteit van oefentherapie in relatie tot de frequentie ervan en de bewijskracht daarvoor. Zie ook de GRADE-profielen van oefentherapie twee keer per week, drie keer per week en vier tot vijf keer per week.
Gewenste effecten
Cruciale uitkomstmaten
- Uitkomstmaat ‘kwaliteit van leven’:
- Er bestaat een groot effect (SMD = 0,77; 95%-BI = -0,08-1,62) van oefentherapie met een frequentie van twee keer per week (2 studies) op kwaliteit van leven bij patiënten met RA, vergeleken met de controlegroep. Het effect van oefentherapie met een frequentie van drie keer per week (0 studies) en van vier tot vijf keer per week (1 studie; SMD niet beschikbaar) is onbekend.
- De bewijskracht voor de uitkomstmaat ‘kwaliteit van leven’ bij een frequentie van twee keer per week is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, gezien beperkingen, tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid). De bewijskracht voor de uitkomstmaat ‘kwaliteit van leven’ bij een frequentie van vier tot vijf keer per week is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, gezien de beperkingen, de tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘fysiek functioneren’:
- Er bestaat een groot effect (SMD = 0,50; 95%-BI = 0,19-0,82) van oefentherapie met een frequentie van twee keer per week (8 studies) op fysiek functioneren bij patiënten met RA, vergeleken met de controlegroep. Het effect van oefentherapie met een frequentie van drie keer per week (7 studies) is gering (SMD = 0,28; 95%-BI = -0,01-0,57) en het effect van oefentherapie met een frequentie van vier tot vijf keer per week (1 studie) is onbekend (SMD niet beschikbaar).
- De bewijskracht voor de uitkomstmaat ‘fysiek functioneren’ bij een frequentie van twee keer per week is met één niveau verlaagd tot ‘redelijke kwaliteit van bewijs’, gezien de tegenstrijdige resultaten (inconsistentie). De bewijskracht voor de uitkomstmaat ‘fysiek functioneren’ bij een frequentie van drie keer per week is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, gezien de beperkingen in de onderzoeksopzet en de uitvoering, en het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘vermoeidheid’:
- Het effect van oefentherapie met een frequentie van twee keer per week, drie keer per week of vier tot vijf keer per week op de vermoeidheid en de bewijskracht is onbekend (0 studies).
- Uitkomstmaat ‘pijn’:
- Er bestaat een matig effect (SMD = 0,42; 95%-BI = -0,40-1,24) van oefentherapie met eenfrequentie van twee keer per week (2 studies) op pijn bij patiënten met RA, vergeleken met de controlegroep. Het effect van oefentherapie met een frequentie van drie keer per week (1 studie; SMD niet beschikbaar) en vier tot vijf keer per week (0 studies) op pijn is onbekend.
- De bewijskracht voor de uitkomstmaat ‘pijn’ bij een frequentie van twee keer per week is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, gezien tegenstrijdige resultaten (inconistentie) en het geringe aantal patiënten (onnauwkeurigheid). De bewijskracht voor de uitkomstmaat ‘pijn’ bij een frequentie van drie keer per week is met twee niveaus verlaagd tot ‘zeer lage kwaliteit van bewijs’, gezien de beperkingen in de onderzoeksopzet en de uitvoering, de tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
Belangrijke uitkomstmaten
- Uitkomstmaat ‘aerobe capaciteit’:
- Er bestaat een matig effect (SMD = 0,44; 95%-BI = 0,25-0,64) van oefentherapie met een frequentie van twee keer per week (5 studies) op aerobe capaciteit bij patiënten met RA, vergeleken met de controlegroep. Het effect van oefentherapie met een frequentie van drie keer per week (4 studies) is groot (SMD = 0,59; 95%-BI = -0,25-0,92) en het effect van oefentherapie met een frequentie van vier tot vijf keer per week (2 studie) is eveneens groot (SMD = 0,61; 95%- BI = 0,08-1,14).
- De bewijskracht voor de uitkomstmaat ‘aerobe capaciteit’ bij een frequentie van twee keer per week is hoog (er is niet afgewaardeerd). De bewijskracht voor de uitkomstmaat ‘aerobe capaciteit’ bij een frequentie van drie keer per week is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, gezien de beperkingen in de onderzoeksopzet en methode en het geringe aantal patiënten (onnauwkeurigheid). De bewijskracht voor de uitkomstmaat ‘aerobe capaciteit’ bij een frequentie van vier tot vijf keer per week is met een niveau verlaagd tot redelijke kwaliteit van bewijs, gezien het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘spierkracht’:
- Er bestaat een groot effect (SMD = 0,72; 95%-BI = 0,20-1,23) van oefentherapie met een frequentie van twee keer per week (9 studies) op de spierkracht bij patiënten met RA, vergeleken met de controlegroep. Het effect van oefentherapie met een frequentie van drie keer per week (2 studies) is eveneens groot (SMD = 0,53; 95%-BI = -0,02-1,07). Het effect van oefentherapie met een frequentie van vier tot vijf keer per week op de spierkracht is onbekend (0 studies).
- De bewijskracht voor de uitkomstmaat ‘spierkracht’ bij een frequentie van twee keer per week is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, gezien beperkingen in onderzoeksopzet en methode en inconsistentie. De bewijskracht voor de uitkomstmaat ‘spierkracht’ bij een frequentie van drie keer per week is verlaagd tot ‘lage kwaliteit van bewijs’, gezien beperkingen in onderzoeksopzet en methode en het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘range of motion’:
- Het effect van oefentherapie met een frequentie van twee keer per week (1 studie) op de range of motion bij patiënten met RA is onbekend (SMD niet beschikbaar). Het effect van oefentherapie met een frequentie van drie keer per week (1 studie) op de range of motion is eveneens onbekend (SMD niet beschikbaar). Het effect van oefentherapie met een frequentie van vier tot vijf keer per week is onbekend (0 studies).
- De bewijskracht voor de uitkomstmaat ‘range of motion’ bij een frequentie van twee keer per week is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, voor tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid). De bewijskracht voor de uitkomstmaat ‘range of motion’ bij een frequentie van drie keer per week is eveneens met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, voor tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘arbeidsproductiviteit’:
- De effectiviteit en bewijskracht kon niet worden bepaald (0 studies).
Ongewenste effecten
- Uitkomstmaat ‘ziekteactiviteit’:
- Er bestaat een matig effect (SMD = 0,33; 95%-BI = -0,28-0,95) van oefentherapie met een frequentie van twee keer per week (4 studies) op de ziekteactiviteit bij patiënten met RA, vergeleken met de controlegroep. Het effect van oefentherapie met een frequentie van drie keer per week (3 studies) is gering (SMD = 0.04; 95%-BI = -0,70-0,79) en het effect van oefentherapie met een frequentie van vier tot vijf keer per week (2 studie) is eveneens gering (SMD = 0,06; 95%-BI = -1,64-1,77).
- De bewijskracht voor de uitkomstmaat ‘ziekteactiviteit’ bij een frequentie van twee keer per week is met een niveau verlaagd tot ‘redelijke kwaliteit van bewijs’, voor inconsistentie. De bewijskracht voor de uitkomstmaat ‘ziekteactiviteit’ bij een frequentie van drie keer per week is met drie niveaus verlaagd tot ‘zeer lage kwaliteit van bewijs’, gezien beperkingen in onder zoeksopzet en methode, tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid). De bewijskracht voor de voor de uitkomstmaat ‘ziekteactiviteit’ bij een frequentie van vier tot vijf keer per week is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, voor tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘radiologische schade’:
- Er bestaat een gering effect (SMD = -0,09; 95%-BI = -0,14-0,31) van oefentherapie met een frequentie van twee keer per week (2 studies) op de radiologische schade bij patiënten met RA, vergeleken met de controlegroep. Het effect van oefentherapie met een frequentie van drie, of vier à vijf keer per week is onbekend (0 studies).
- De bewijskracht voor de uitkomstmaat ‘radiologische schade’ bij een frequentie van twee keer per week is met een niveau verlaagd tot ‘redelijke kwaliteit van bewijs’, gezien het geringe aantal patiënten (onnauwkeurigheid).
GRADE-profiel van oefentherapie met een frequentie van twee keer per week.[link]
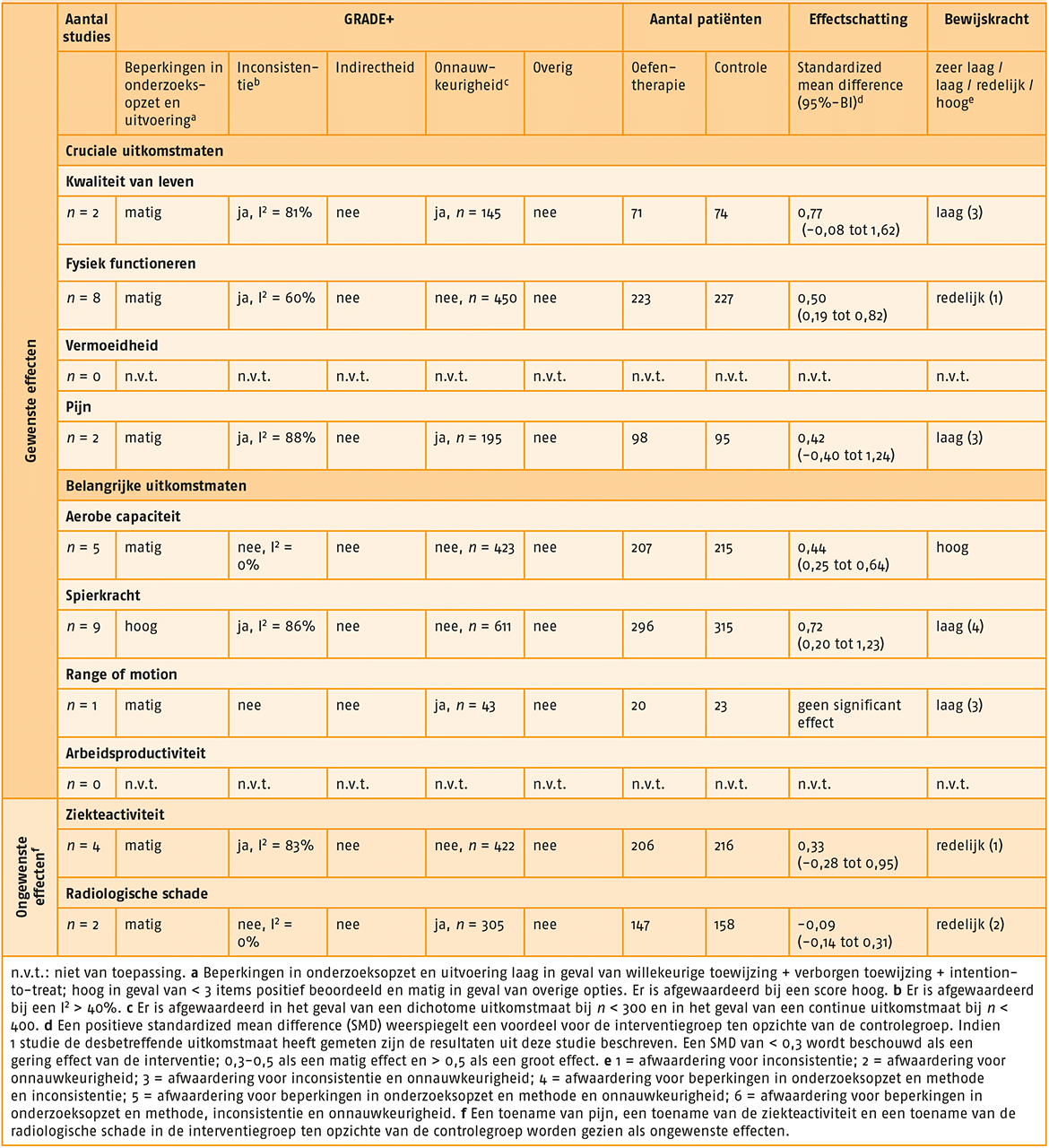
GRADE-profiel van oefentherapie met een frequentie van drie keer per week.[link]
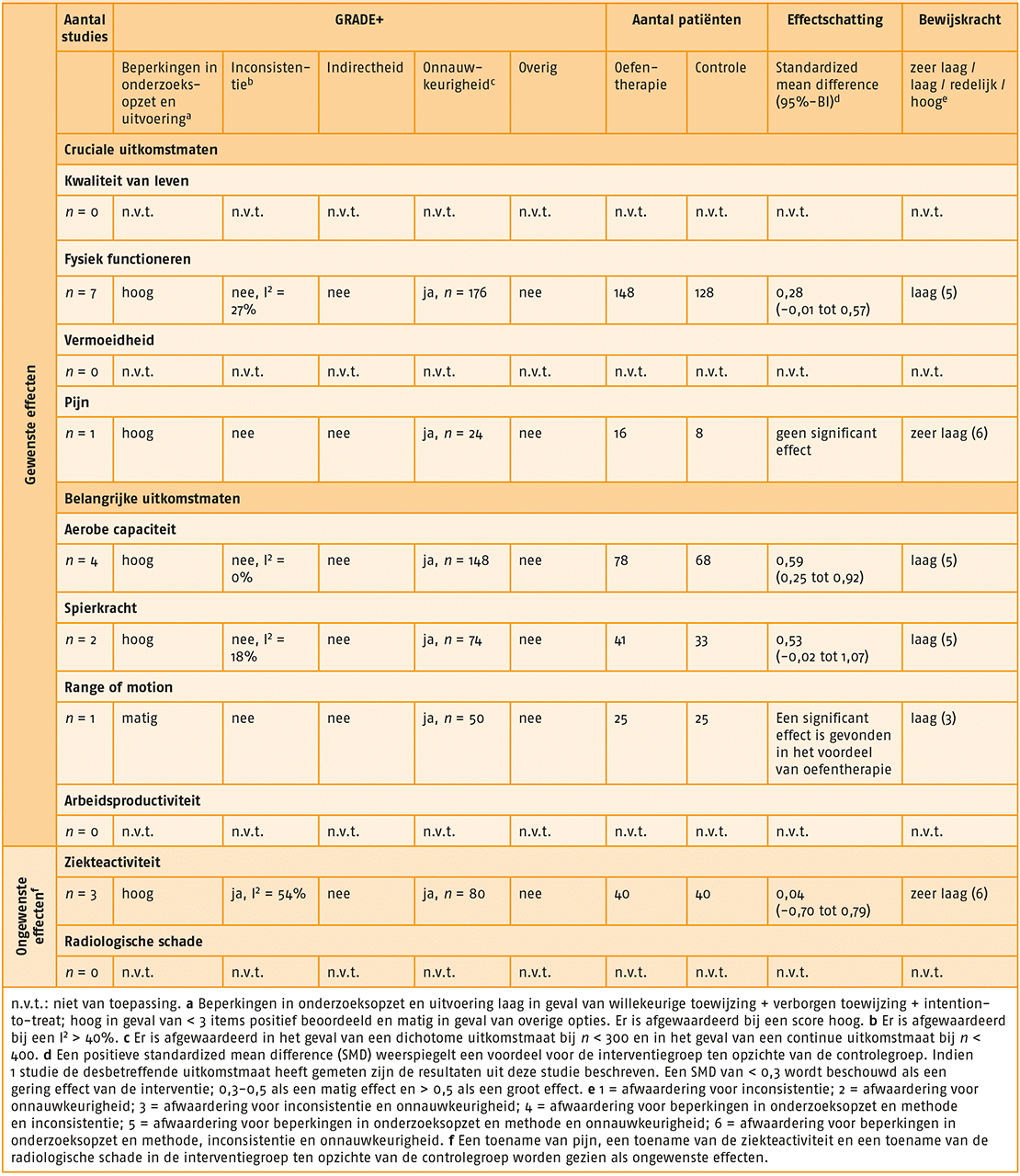
GRADE-profiel van oefentherapie met een frequentie van vier tot vijf keer per week.[link]
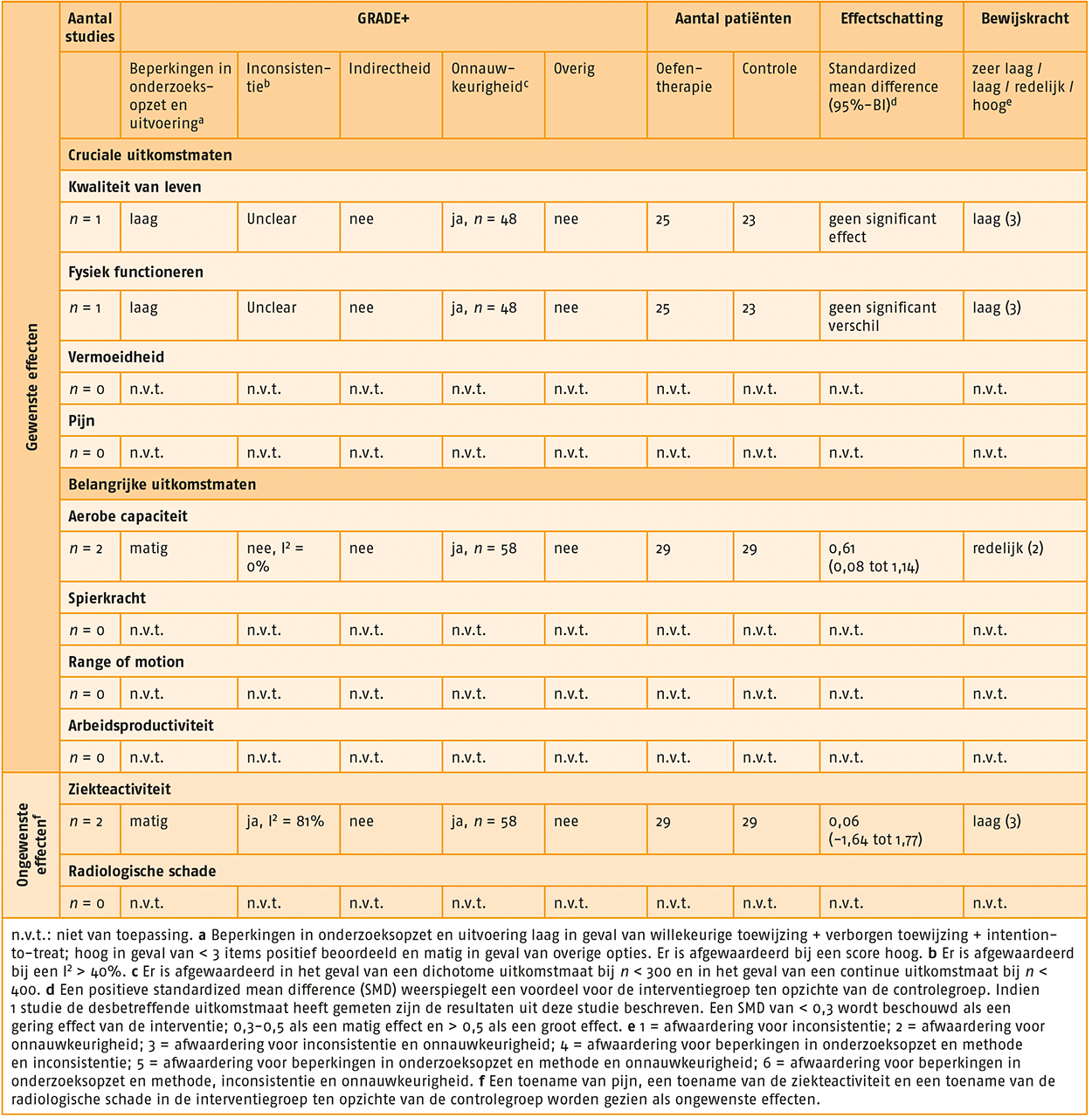
Van bewijs naar aanbeveling
Bij de formulering van de richting en de sterkte van de aanbeveling voor oefentherapie bij indicatie 1 heeft de werkgroep de volgende aanvullende overwegingen gemaakt.
Op basis van de omvang van de effectschattingen en de kwaliteit van bewijs is de werkgroep van mening dat een frequentie van twee keer per week begeleide oefentherapie de voorkeur verdient (bij indicatie 2), aangevuld met zelfstandig uitgevoerde oefeningen. Hierbij wordt aangetekend dat de begeleiding gedurende de behandelperiode afgebouwd dient te worden in overleg met de patiënt, waarbij het accent verschuift naar zelfstandig oefenen en bewegen. Op basis van de ACSM-richtlijnen [20] wordt hieraan toegevoegd dat spierkracht of functionele oefeningen en/of activiteiten bij voorkeur dagelijks, maar minimaal twee dagen per week geadviseerd worden en aerobe oefeningen en/of activiteiten bij voorkeur dagelijks, maar minimaal vijf dagen per week ten minste 30 minuten per keer, om tevens te voldoen aan de Beweegrichtlijnen van de Gezondheidsraad [21].
- Welke waarde patiënten aan een bepaalde frequentie hechten, en naar welke frequentie hun voorkeur naar uitgaat, zal waarschijnlijk van patiënt tot patiënt verschillen. De werkgroep schat in dat de meerderheid van de patiënten positief staat tegenover oefentherapie met een frequentie van twee keer per week.
- De eventuele kosten voor de patiënt zijn bij een frequentie van twee keer per week begeleide oefentherapie gunstig dan bij hogere frequenties (3-5x per week).
- De implementatie van oefentherapie met een frequentie van twee keer per week in de dagelijkse praktijk wordt door de werkgroep als aanvaardbaar en haalbaar ingeschat, omdat deze frequentie als meest aangewezen behandelfrequentie wordt beschouwd.
1. Baillet A, Payraud E, Niderprim VA, Nissen MJ, Allenet B, François P, et al. A dynamic exercise programme to improve patients’ disability in rheumatoid arthritis: a prospective randomized controlled trial. Rheumatology (Oxford). 2009 Apr;48(4):410-5.
2. Baslund B, Lyngberg K, Andersen V, Halkjaer Kristensen J, Hansen M, Klokker M, et al. Effect of 8 wk of bicycle training on the immune system of patients with rheumatoid arthritis. J Appl Physiol. 1993;75:1691-5.
3. Bearne LM, Scott DL, Hurley MV. Exercise can reverse quadriceps sensorimotor dysfunction that is associated with rheumatoid arthritis without exacerbating disease activity. Rheumatology (Oxford). 2002 Feb;41(2):157-66.
4. Bilberg A, Ahlmén M, Mannerkorpi K. Moderately intensive exercise in a temperate pool for patients with rheumatoid arthritis: a randomized controlled study. Rheumatology (Oxford). 2005 Apr;44(4):502-8.
5. Breedland I, van Scheppingen C, Leijsma M, Verheij-Jansen NP, van Weert E. Effects of a group-based exercise and educational program on physical performance and disease self-management in rheumatoid arthritis: a randomized controlled study. Phys Ther. 2011 Jun;91(6):879-93.
6. Da Silva KN, Teixeira LE, Imoto AM, Atallah AN, Peccin MS, Trevisani VF. Effectiveness of sensorimotor training in patients with rheumatoid arthritis: a randomized controlled trial. Rheumatol Int. 2013 Sep;33(9):2269-75.
7. de Jong Z, Munneke M, Zwinderman AH, Kroon HM, Jansen A, Ronday KH, et al. Is a long-term high-intensity exercise program effective and safe in patients with rheumatoid arthritis? Results of a randomized controlled trial. Arthritis Rheum. 2003;48(9):2415-24.
8. Flint-Wagner HG, Lisse J, Lohman TG, Going SB, Guido T, Cussler E, Gates D, Yocum DE. Assessment of a sixteen-week training program on strength, pain, and function in rheumatoid arthritis patients. J Clin Rheumatol. 2009 Jun;15(4):165-71,
9. Häkkinen A, Häkkinen K, Hannonen P. Effects of strength training on neuromuscular function and disease activity in patients with recent-onset inflammatory arthritis. Scand J Rheumatol. 1994;23(5):237-42.
10. Hansen TM, Hansen G, Langgaard AM, Rasmussen JO. Longterm physical training in rheumatoid arthritis. A randomized trial with different training programs and blinded observers. Scand J Rheumatol. 1993;22(3):107-12.
11. Harkcom TM, Lampman RM, Banwell BF, Castor CW. Therapeutic value of graded aerobic exercise training in rheumatoid arthritis. Arthr Rheum. 1985;28(1):32-9.
12. Lemmey AB, Marcora SM, Chester K, Wilson S, Casanova F, Maddison PJ. Effects of high-intensity resistance training in patients with rheumatoid arthritis: a randomized controlled trial. Arthritis Rheum. 2009 Dec 15;61(12):1726-34.
13. Lyngberg KK, Harreby M, Bentzen H, Frost B. Elderly rheumatoid arthritis on steroid treatment tolerate physical training without an increase in disease activity. Arch Phys Med Rehab. 1994;75:1189-95.
14. McMeeken J, Stillman B, Story I, Kent P, Smith J. The effects of knee extensor and flexor muscle training on the timed-up-and-go test in individuals with rheumatoid arthritis. Physiother Res Int. 1999;4(1):55-67.
15. Minor MA, Hewett JE, Webel RR, Anderson SK, Kay DR. Efficacy of physical conditioning exercise in patients with rheumatoid arthritis and osteoarthritis. Arthritis Rheum. 1989;32(11):1396-405.
16. Sanford-Smith S, Mackay-Lyons M, Nunes-Clement S. Therapeutic benefit of aquaerobics for individuals with rheumatoid arthritis. Physiotherapy Canada 1998;Winter:40–6.
17. Siqueira US, Orsini Valente LG, de Mello MT, Szejnfeld VL, Pinheiro MM. Effectiveness of aquatic exercises in women with rheumatoid arthritis: a randomized, controlled, 16-week intervention – the HydRA Trial. Am J Phys Med Rehabil. 2017 Mar;96(3):167-75.
18. Strasser B, Leeb G, Strehblow C, Schobersberger W, Haber P, Cauza E. The effects of strength and endurance training in patients with rheumatoid arthritis. Clin Rheumatol. 2011 May;30(5):623-32.
19. van den Ende CHM, Hazes JMW, Le Cessie S, Mulder WJ, Belfor DG, Breedveld FC, et al. Comparison of high and low intensity training in well controlled rheumatoid arthritis. Results of a randomized clinical trial. Ann Rheum Dis. 1996;55(11):798-805.
20. American College of Sports Medicine. Guidelines for Exercise Testing and Prescription. 10th edition. Lippincott William and Wilkins; 2017.
21. Beweegrichtlijnen 2017. Samenvatting. Den Haag: Gezondheidsraad; 2017. Beschikbaar via https://www.gezondheidsraad.nl/sites/default/files/grpublication/samenvatting_beweegrichtlijnen_2017_1.pdf
C.3.2 Intensiteit
Aanbeveling Streef naar de volgende minimale intensiteit:
- Spierkrachttraining: 60-80% van 1 repetition maximum (1RM; Borg-score 14-17) voor mensen die gewend zijn aan krachttraining. Pas de intensiteit aan naar 50-60% van 1RM (Borg-score 12-13) voor mensen die niet gewend zijn aan krachttraining. Streef naar twee tot vier sets van 8-15 herhalingen en 30-60 sec pauze tussen de sets.
- Aerobe training: > 60% van de maximale hartfrequentie (Borg-score 14-17) voor mensen die gewend zijn aan aerobe training. Pas de intensiteit aan naar 40-60% van de maximale hartfrequentie (Borg-score 12-13) voor mensen die niet gewend zijn aan aerobe training.
Zorg voor een geleidelijke opbouw in de intensiteit gedurende het programma. Volg hierin de volgende traiiningsprincipes.
Trainingsprincipes bij RA
- Begin de training met een warming-up en sluit af met een coolingdown.
- Bepaal de startintensiteit van de spierkrachttraining en monitor de intensiteit gedurende de behandeling met behulp van de submaximale krachttest.
- Bepaal de startintensiteit van de aerobe training en monitor de intensiteit gedurende de behandeling met behulp van hartfrequentie en/of Borg-score.
- Bouw de intensiteit van de training geleidelijk op tot het voor de patiënt maximaal haalbare niveau.
- Verlaag de intensiteit van de volgende training of las een extra hersteldag in, indien pijnklachten in het gewricht toenemen na de training en langer dan twee uur aanhouden.
- Start met aerobe oefeningen gedurende 10 minuten (of korter indien nodig) bij patiënten die ongetraind zijn en/of beperkt zijn door gewrichtspijn en -mobiliteit.
- Bied een alternatieve oefening aan waarbij dezelfde spiergroepen en energiesystemen worden gebruikt indien bij korter dan 10 minuten oefenen toename in gewrichtspijn optreedt.
- Pas de intensiteit van de krachttraining aan door het aantal sets, het aantal herhalingen en de pauze tussen de sets bij te stellen en pas de intensiteit van de aerobe training aan door de duur van de oefeningen, de duur van de sessie en de rustpauzes tussen de oefeningen bij te stellen.
Onderbouwing
Noot 16
Uitgangsvraag
Welke intensiteit van oefentherapie wordt aanbevolen bij patiënten met RA?
Conclusie vanuit de literatuurstudie
De effectiviteit van oefentherapie met een hoge intensiteit (met progressieve opbouw) versus oefentherapie met een lagere intensiteit op kwaliteit van leven, fysiek functioneren en vermoeidheid is onbekend, omdat er weinig studies over beschikbaar zijn en omdat in de studies die wel beschikbaar zijn effectschattingen niet zijn gerapporteerd. Bovendien is de kwaliteit van bewijs van de beschikbare studies laag.
Van bewijs naar aanbeveling
Op basis van het gebrek aan bruikbare effectschattingen en de lage kwaliteit van bewijs op het gebied van oefentherapie met een hoge intensiteit versus een lagere intensiteit is de werkgroep van mening dat er geen uitspraak gedaan kan worden over een voorkeur voor de ene, dan wel de andere intensiteit. Daarop is besloten de ACSM-richtlijnen te raadplegen. Gebaseerd op de ACSM-richtlijnen is door de werkgroep de minimale intensiteit van spierkrachttraining en aerobe training vastgesteld.
Aanbeveling voor de intensiteit van de oefentherapie
Streef naar de volgende minimale intensiteit:
- Spierkrachttraining: 60-80% van 1 repetition maximum (1RM; Borg-score 14-17) voor mensen die gewend zijn aan krachttraining. Pas de intensiteit aan naar 50-60% van 1RM (~Borg-score 12-13) voor mensen die niet gewend zijn aan krachttraining. Streef naar twee tot vier sets van 8-15 herhalingen en 30-60 sec pauze tussen de sets.
- Aerobe training: > 60% van de maximale hartfrequentie (~BORG-score 14-17) voor mensen die gewend zijn aan aerobe training. Pas de intensiteit aan naar 40-60% van de maximale hartfrequentie (~BORG-score 12-13) voor mensen die niet gewend zijn aan aerobe training.
Complete uitgangsvraag volgens PICO
Voor de beantwoording van deze uitgangsvraag is een gezamenlijke PICO uitgangsvraag geformuleerd voor de frequentie, intensiteit, type en duur van oefentherapie (zie noot 14).
Zoekstrategie
Er is een gezamenlijke zoekactie uitgevoerd voor de frequentie, intensiteit, type en duur van oefentherapie (zie noot 14).
Gevonden literatuur
De zoekactie van de literatuur leverde 1837 referenties op. Vier gerandomiseerde gecontroleerde onderzoeken
voldeden aan de inclusiecriteria voor de beantwoording van de uitgangsvraag met betrekking tot de intensiteit
van de oefentherapie.[1-4] De informatie uit deze studies is aangevuld met informatie uit de ACSM-richtlijn.[5]
Beschrijving studies
In vier studies werd een hoogintensief (dynamisch) oefenprogramma vergeleken met een oefenprogramma met een lagere intensiteit.[1-4] Hoe tot deze literatuur gekomen is staat beschreven in noot 14.
Effectiviteit en bewijskracht
De beoordeling van de onderzoeksopzet en uitvoering van de geselecteerde artikelen is opgenomen in de bijlage (opent in nieuw tabblad) van deze noot.
Hierna volgt per uitkomstmaat een beschrijving van de effectiviteit van oefentherapie in relatie tot de intensiteit ervan en de bewijskracht daarvoor. Zie ook het GRADE-profiel van de intensiteit van oefentherapie.
Gewenste effecten
Cruciale uitkomstmaten
- Uitkomstmaat ‘kwaliteit van leven’ (0 studies):
- Het effect en de bewijskracht van oefentherapie met een hoge intensiteit vergeleken met oefen- therapie met een lagere intensiteit op de kwaliteit van leven is onbekend.
- Uitkomstmaat ‘fysiek functioneren’ (3 studies):
- Het effect van oefentherapie met een hoge intensiteit vergeleken met oefentherapie met een lagere intensiteit op het fysiek functioneren is onbekend (SMD niet beschikbaar).
- De bewijskracht voor de uitkomstmaat ‘fysiek functioneren’ is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, gezien tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘vermoeidheid’ (0 studies):
- Het effect van oefentherapie met een hoge intensiteit vergeleken met oefentherapie met een lagere intensiteit op de vermoeidheid is onbekend.
- Uitkomstmaat ‘pijn’ (4 studies):
- Het effect van oefentherapie met een hoge intensiteit vergeleken met oefentherapie met een lagere intensiteit op de pijn is onbekend (SMD niet beschikbaar).
- De bewijskracht voor de uitkomstmaat ‘pijn’ is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, gezien tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
Belangrijke uitkomstmaten
- Uitkomstmaat ‘aerobe capaciteit’ (2 studies):
- Het effect en de bewijskracht van oefentherapie met een hoge intensiteit vergeleken met oefen- therapie met een lagere intensiteit op de aerobe capaciteit is onbekend (SMD niet beschikbaar).
- De bewijskracht voor de uitkomstmaat aerobe capaciteit is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, voor tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘spierkracht’ (4 studies):
- Het effect van oefentherapie met een hoge intensiteit vergeleken met oefentherapie met een lagere intensiteit op de spierkracht is onbekend (SMD niet beschikbaar).
- De bewijskracht voor de uitkomstmaat spierkracht is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, voor tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘range of motion’ (3 studies):
- Het effect van oefentherapie met een hoge intensiteit vergeleken met oefentherapie met een lagere intensiteit op de range of motion is onbekend (SMD niet beschikbaar).
- De bewijskracht voor de uitkomstmaat range of motion is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, voor tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘arbeidsproductiviteit’ (0 studies):
- Het effect van oefentherapie met een hoge intensiteit vergeleken met oefentherapie met een lagere intensiteit op de pijn is onbekend (SMD niet beschikbaar).
- De bewijskracht voor de uitkomstmaat ‘pijn’ is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, gezien tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
Ongewenste effecten
- Uitkomstmaat ‘ziekteactiviteit’ (4 studies):
- Het effect van oefentherapie met een hoge intensiteit vergeleken met oefentherapie met een lagere intensiteit op de ziekteactiviteit is onbekend (SMD niet beschikbaar).
- De bewijskracht voor de uitkomstmaat ziekteactiviteit is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, gezien tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘radiologische schade’ (1 studie):
- Het effect van oefentherapie met een hoge intensiteit vergeleken met oefentherapie met een lagere intensiteit op de radiologische schade is onbekend (SMD niet beschikbaar).
- De bewijskracht voor de uitkomstmaat ‘radiologische schade’ is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, gezien tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
GRADE-profiel van de intensiteit van de oefentherapie. [link]
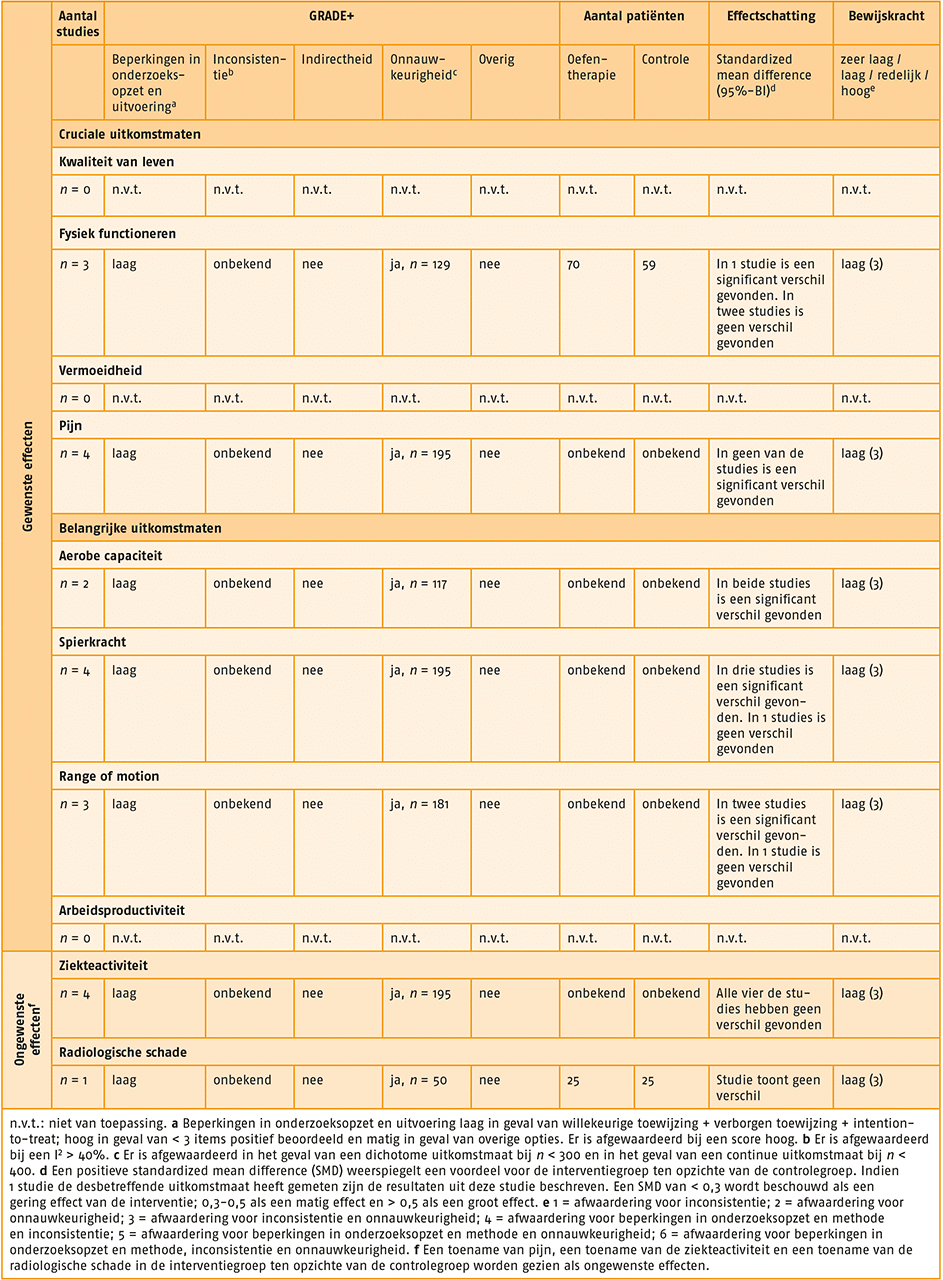
Van bewijs naar aanbeveling
Bij de formulering van de richting en de sterkte van de aanbeveling voor oefentherapie bij indicatie 1 heeft de werkgroep de volgende aanvullende overwegingen gemaakt.
- De werkgroep heeft geen voorkeur ten aanzien van de intensiteit van oefentherapie, omdat bruikbare effectschattingen hiervoor ontbreken. Daarom heeft de werkgroep op basis van de ACSM-richtlijnen de minimale intensiteit van spierkrachttraining en aerobe training vastgesteld.
- Welke waarde patiënten aan een bepaalde intensiteit van oefentherapie hechten, en naar welke intensiteit hun voorkeur uitgaat, zal waarschijnlijk van patiënt tot patiënt verschillen. De werkgroep schat in dat de meeste patiënten positief staan tegenover de gestelde minimale intensiteit van de oefentherapie, omdat met die intensiteit volgens de trainingsprincipes optimale behandelresultaten bereikt kunnen worden.
- Implementatie van oefentherapie met een minimale intensiteit in de dagelijkse praktijk wordt door de werkgroep als aanvaardbaar en haalbaar ingeschat, omdat deze als meest aangewezen behandelintensiteit wordt beschouwd.
1. Bostrom C, Harms-Ringdahl K, Karreskog H, Nordemar R. Effects of static and dynamic shoulder rotator exercises in women with rheumatoid arthritis: a randomised comparison of impairment, disability, handicap, and health. Scand J Rheumatol. 1998;27(4):281-90.
2. Ekdahl C, Andersson SI, Moritz U, Svensson B. Dynamic versus static training in patients with rheumatoid arthritis. Scand J Rheumatol. 1990;19(1):17-26.
3. van den Ende CHM, Hazes JMW, le Cessie S, Mulder WJ, Belfor DG, Breedveld FC, Dijkmans BA. Comparison of high and low intensity training in well controlled rheumatoid arthritis. Results of a randomized clinical trial. Ann Rheum Dis. 1996;55(11):798-805.
4. van den Ende CHM, Breedveld FC, le Cessie S, Dijkmans BAC, de Mug AW, Hazes JMW. Effect of intensive exercise on patients with active rheumatoid arthritis: a randomised clinical trial. Ann Rheum Dis. 2000;59:615-21.
5. American College of Sports Medicine. Guidelines for Exercise Testing and Prescription. 10th edition. Lippincott William and Wilkins; 2017.
C.3.3 Type
Aanbevelingen
- Bied oefentherapie aan in een combinatie van spierkrachttraining (kies voor oefeningen waarbij meerdere spiergroepen en meerdere gewrichten betrokken zijn) en aerobe training (kies voor activiteiten waarbij matig- tot hoogintensief getraind kan worden, zoals lopen, fietsen, zwemmen, roeien en oefenen op de crosstrainer).
NB Combineer bij spierkracht- en bij aerobe training functionele oefeningen (met bijvoorbeeld het eigen lichaamsgewicht) en oefeningen met apparaten. - Gebruik voor een optimaal behandelresultaat binnen één behandelsessie ten minste 75% van de behandeltijd voor één type training: spierkracht- of aerobe training. Instrueer de patiënt om het type training waar tijdens de behandelsessie minder tijd aan is besteed, zelfstandig uit te voeren.
- Gebruik functionele training: integreer in de oefentherapie activiteiten waarin de patiënt beperkt is (zoals lopen, traplopen, gaan zitten en opstaan uit een stoel, tillen of pakken van grote en kleine voorwerpen) door (onderdelen van) deze activiteiten te oefenen.
- Overweeg de oefentherapie aan te vullen met specifieke balans-, coördinatie- en/of neuromusculaire training wanneer sprake is van verstoringen op dit gebied.
- Overweeg de oefentherapie aan te vullen met actieve range-of-motion- of spierrekkingsoefeningen indien spierverkortingen en/of reversibele mobiliteitsbeperkingen van het gewricht het functioneren van de patiënt belemmeren.
Onderbouwing
Noot 17
Uitgangsvraag
Welk type oefentherapie wordt aanbevolen bij patiënten met RA?
Conclusie vanuit de literatuurstudie
Er zijn geen RCT’s gevonden waarin de effectiviteit van de verschillende typen oefentherapie rechtstreeks met elkaar zijn vergeleken. De aanbeveling voor het type oefentherapie is gebaseerd op de ACSM-richtlijn.[1]
Van bewijs naar aanbeveling
Niet van toepassing.
Aanbeveling voor het type oefentherapie
- Bied oefentherapie aan in een combinatie van spierkrachttraining (kies voor oefeningen waarbij meerdere spiergroepen en meerdere gewrichten betrokken zijn) en aerobe training (kies voor activiteiten waarbij matig- tot hoogintensief getraind kan worden, zoals lopen, fietsen, zwemmen, roeien en oefenen op de crosstrainer).
NB Combineer bij spierkracht- en bij aerobe training functionele oefeningen (met bijvoorbeeld het eigen lichaamsgewicht) en oefeningen met apparaten. - Gebruik voor een optimaal behandelresultaat binnen één behandelsessie ten minste 75% van de behandeltijd voor één type training: spierkracht- of aerobe training. Instrueer de patiënt om het type training waar tijdens de behandelsessie minder tijd aan is besteed, zelfstandig uit te voeren.
- Gebruik functionele training: integreer in de oefentherapie activiteiten waarin de patiënt beperkt is (zoals lopen, traplopen, gaan zitten en opstaan uit een stoel, tillen of pakken van grote en kleine voorwerpen) door (onderdelen van) deze activiteiten te oefenen.
- Overweeg de oefentherapie aan te vullen met specifieke balans-, coördinatie- en/of neuromusculaire training wanneer sprake is van verstoringen op dit gebied.
- Overweeg de oefentherapie aan te vullen met actieve range-of-motion- of spierrekkingsoefeningen indien spierverkortingen en/of reversibele mobiliteitsbeperkingen van het gewricht het functioneren van de patiënt belemmeren.
Complete uitgangsvraag volgens PICO
Voor de beantwoording van deze uitgangsvraag is een gezamenlijke PICO uitgangsvraag geformuleerd voor de frequentie, intensiteit, type en duur van oefentherapie (zie noot 14).
Zoekstrategie
Er is een gezamenlijke zoekactie uitgevoerd voor de frequentie, intensiteit, type en duur van oefentherapie (zie noot 14).
Gevonden literatuur
Er zijn geen gerandomiseerde gecontroleerde onderzoeken gevonden waarin het type oefentherapie rechtstreeks is onderzocht (zie noot 14). De aanbeveling voor het type oefentherapie is gebaseerd op de ACSM-richtlijn.[1]
Beschrijving studies
Niet van toepassing.
Effectiviteit en bewijskracht
Niet van toepassing.
Van bewijs naar aanbeveling
Niet van toepassing.
1. American College of Sports Medicine. Guidelines for Exercise Testing and Prescription. 10th edition. Lippincott William and Wilkins; 2017.
C.3.4 Duur
Uitgangsvraag
Welke duur van oefentherapie wordt aanbevolen bij patiënten met Reumatoïde Artritis (RA)?
De volgende sub-uitgangsvragen werden hierbij geformuleerd:
- Welke duur van oefentherapie wordt aanbevolen bij patiënten met RA met indicatie 1?
- Welke duur van oefentherapie wordt aanbevolen bij patiënten met RA met indicatie2?
- Welke duur van oefentherapie wordt aanbevolen bij patiënten met RA met indicatie 3?
Aanbevelingen
Streef naar een behandelperiode tussen de drie en de zes maanden voor indicatie 1 & 2.
Streef hierbij bij indicatie 1 naar maximaal drie tot zes keer begeleide oefentherapie (zie ook Module C.2.1 (opent in nieuw tabblad)). Voor verdere toelichting over indicatie 2, zie Module C.2.2 (opent in nieuw tabblad).
Bied langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie op indicatie (zie module B.4 Indicatiestelling (opent in nieuw tabblad)) aan bij patiënten met RA met ernstige functionele beperkingen in het dagelijks leven (indicatie 3), zolang de indicatie van toepassing blijft.
Toelichting Noot 18
Uitgangsvraag
Welke duur van oefentherapie wordt aanbevolen bij patiënten met RA?
Conclusie vanuit de literatuurstudie
De literatuur toont een groot effect van oefentherapie met een duur van drie tot zes maanden op de ‘kwaliteit van leven’ (lage kwaliteit van bewijs) en ‘pijn’ (redelijke kwaliteit van bewijs). De effectiviteit van oefentherapie met een duur van minder dan drie maanden en een duur van meer dan zes maanden op de kwaliteit van leven en pijn is onbekend. Op de uitkomstmaat ‘fysiek functioneren’ is er geen verschil in de effectiviteit tussen een duur van minder dan drie maanden, drie tot zes maanden en meer dan zes maanden oefentherapie.
Van bewijs naar aanbeveling
Op basis van de omvang van de effectschattingen en het kwaliteit van bewijs, die in het voordeel zijn van een duur van drie tot zes maanden, ten opzichte van een duur van minder dan drie maanden en een duur van meer dan zes maanden, is de werkgroep van mening dat een duur van drie tot zes maanden de voorkeur verdient (bij indicatie 2). Hieraan wordt door de werkgroep toegevoegd dat het streven is de behandelperiode aan te vullen met een of enkele follow-upsessies tegen het einde of na afronding van de behandelperiode om therapietrouw te bevorderen en om de patiënt te stimuleren tijdens en na de behandelperiode zelfstandig te blijven oefenen en bewegen.
Aanbeveling voor de duur van de oefentherapie
Streef naar een behandelperiode tussen de drie en de zes maanden. Vul de behandeling aan met een of enkele follow-upsessies. Deze hebben als doel de therapietrouw te bevorderen en kunnen worden ingepland op het moment dat de omvang van de begeleide oefentherapie is afgenomen en het zelfstandig oefenen en bewegen de boventoon voert. Stimuleer de patiënt om ook na de behandelperiode zelfstandig te blijven oefenen en bewegen.
Complete uitgangsvraag volgens PICO
Voor de beantwoording van deze uitgangsvraag is een gezamenlijke PICO uitgangsvraag geformuleerd voor de frequentie, intensiteit, type en duur van oefentherapie (zie noot 14).
Zoekstrategie
Er is een gezamenlijke zoekactie uitgevoerd voor de frequentie, intensiteit, type en duur van oefentherapie (zie noot 14).
Gevonden literatuur
Er zijn geen gerandomiseerde gecontroleerde onderzoeken gevonden waarbij de duur van de oefentherapie rechtstreeks is onderzocht. Om toch een aanbeveling te kunnen formuleren over de tijdsduur is een subgroepanalyse doorgevoerd met de geïncludeerde studies voor de uitgangsvraag over de effectiviteit van oefentherapie, om te bepalen welke duur het optimale resultaat oplevert (zie noot 14).
Beschrijving studies
Van de 19 geïncludeerde studies naar de effectiviteit van oefentherapie hadden zes studies een duur van minder dan drie maanden [1-3, 5, 14, 16 ], 11 studies een duur van drie tot zes maanden [4,6,8,9,11-13,15,17-19], en twee studies hadden een duur van meer dan zes maanden.[7,10] De karakteristieke van de studies worden beschreven in noot 10.
Effectiviteit en bewijskracht
De beoordeling van de onderzoeksopzet en uitvoering van de geselecteerde artikelen is opgenomen in de bijlage van deze noot.
Hierna volgt per uitkomstmaat een beschrijving van de effectiviteit van oefentherapie in relatie tot de duur ervan, en de bewijskracht daarvoor. Zie ook de GRADE-profielen van oefentherapie met een duur van minder dan drie maanden, met een duur van drie tot zes maanden, en met een duur van meer dan zes maanden.
Gewenste effecten
Cruciale uitkomstmaten
- Uitkomstmaat ‘kwaliteit van leven’:
- Het effect en de bewijskracht van oefentherapie met een duur van minder dan drie maanden (0 studies) en met een duur van meer dan zes maanden (0 studies) op de kwaliteit van leven is onbekend. Het effect van oefentherapie met een duur van drie tot zes maanden (3 studies) op de kwaliteit van leven is groot (SMD = 0,77; 95%-BI = -0,08-1,62).
- De bewijskracht voor de uitkomstmaat ‘kwaliteit van leven’ met een duur van drie tot zes maanden is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, gezien tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘fysiek functioneren’:
- Er bestaat een matig effect (SMD = 0,48; 95%-BI = 0,21-0,74) van oefentherapie met een duur van minder dan drie maanden (5 studies) op fysiek functioneren. Er bestaat eveneens een matig effect (SMD = 0,42; 95%-BI = 0,14-0,71) van oefentherapie met een duur van drie tot zes maanden (10 studies) op fysiek functioneren. Tevens bestaat er een matig effect (SMD = 0,42; 95%-BI = 0,19-0,65) van oefentherapie met een duur van meer dan zes maanden op fysiek functioneren (2 studies).
- De bewijskracht voor de uitkomstmaat ‘fysiek functioneren’ bij een duur van minder dan drie maanden is met één niveau verlaagd tot ‘redelijke kwaliteit van bewijs’, gezien het geringe aantal patiënten (onnauwkeurigheid). De bewijskracht voor de uitkomstmaat ‘fysiek functioneren’ bij een duur van drie tot zes maanden is met één niveau verlaagd tot ‘redelijke kwaliteit van bewijs’, gezien tegenstrijdige resultaten (inconsistentie). De bewijskracht voor de uitkomstmaat ‘fysiek functioneren’ bij een duur van meer dan zes maanden is met één niveau verlaagd tot ‘redelijke kwaliteit van bewijs’, gezien het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘vermoeidheid’:
- Het effect en de bewijskracht van oefentherapie met een duur van minder dan drie maanden, drie tot zes maanden en meer dan zes maanden op de vermoeidheid is onbekend (0 studies).
- Uitkomstmaat ‘pijn’:
- Het effect van oefentherapie met een duur van minder dan drie maanden (SMD niet beschikbaar) en met een duur van meer dan zes maanden (0 studies) op de pijn is onbekend. Er bestaat een groot effect (SMD = 0,82; 95%-BI = -0,45-1,19) van oefentherapie met een duur van drie tot zes maanden op de pijn (2 studies).
- De bewijskracht voor de uitkomstmaat ‘pijn’ voor de duur van minder dan drie maanden is met twee niveaus verlaagd tot ‘zeer lage kwaliteit van bewijs’, gezien de beperkingen in de onderzoeksopzet en de uitvoering, tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid). De bewijskracht voor de uitkomstmaat ‘pijn’ bij een duur van drie tot zes maanden is met één niveau verlaagd tot ‘redelijke kwaliteit van bewijs’, gezien het geringe aantal patiënten (onnauwkeurigheid).
Belangrijke uitkomstmaten
- Uitkomstmaat ‘aerobe capaciteit’:
- Er bestaat een matig effect (SMD = 0,46; 95%-BI = 0,06-0,86) van oefentherapie met een duur van minder dan drie maanden (3 studies) op de aerobe capaciteit. Er bestaat eveneens een matig effect (SMD = 0,49; 95%-BI = 0,23-0,75) van oefentherapie met een duur van drie tot zes maanden (6 studies) op fysiek functioneren. Het effect van oefentherapie met een duur van meer dan zes maanden op de aerobe capaciteit is onbekend (0 studies).
- De bewijskracht voor de uitkomstmaat ‘aerobe capaciteit’ bij een duur van minder dan drie maanden is met één niveau verlaagd tot ‘redelijke kwaliteit van bewijs’, gezien het geringe aantal patiënten (onnauwkeurigheid). De bewijskracht voor de uitkomstmaat ‘aerobe capaciteit’ bij een duur van drie tot zes maanden is met één niveau verlaagd tot ‘redelijke kwaliteit van bewijs’, gezien het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘spierkracht’:
- Er bestaat een matig effect (SMD = 0,48; 95%-BI = 0,21-0,74) van oefentherapie met een duur van minder dan drie maanden (5 studies) op ‘spierkracht’. Er bestaat eveneens een matig effect (SMD = 0,42; 95%-BI = 0,14-0,71) van oefentherapie met een duur van drie tot zes maanden (10 studies) op ‘spierkracht’. Tevens bestaat er een matig effect (SMD = 0,42; 95%-BI =0,19-0,65) van oefentherapie met een duur van meer dan zes maanden op ‘spierkracht’ (2 studies).
- De bewijskracht voor de uitkomstmaat ‘spierkracht’ bij een duur van minder dan drie maanden is met één niveau verlaagd tot ‘redelijke kwaliteit van bewijs’, gezien het geringe aantal patiënten (onnauwkeurigheid). De bewijskracht voor de uitkomstmaat ‘spierkracht’ bij een duur van drie tot zes maanden is met één niveau verlaagd tot ‘redelijke kwaliteit van bewijs’, gezien het geringe aantal patiënten (onnauwkeurigheid). De bewijskracht voor de uitkomstmaat ‘spierkracht’ bij een duur van meer dan zes maanden is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, gezien tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘range of motion’:
- De effectiviteit van oefentherapie met een duur van minder dan drie maanden op ‘range of motion’ is onbekend (0 studies). Er bestaat een groot effect (SMD = 0,59; 95%-BI = 0,17-1,01) van oefentherapie met een duur van drie tot zes maanden (2 studies) op ‘range of motion’.
- De effectiviteit van oefentherapie met een duur van meer dan zes maanden op ‘range of motion’ is onbekend (0 studies).
- De bewijskracht voor de uitkomstmaat ‘range of motion’ bij een duur van drie tot zes maanden is met één niveau verlaagd tot ‘redelijke kwaliteit van bewijs’, gezien het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘arbeidsproductiviteit’:
- De effectiviteit van oefentherapie met een duur van minder dan drie maanden, een duur van drie tot zes maanden, of met een duur van meer dan zes maanden op ‘arbeidsproductiviteit’ is onbekend (0 studies).
Ongewenste effecten
- Uitkomstmaat ‘ziekteactiviteit’:
- Er bestaat een gering effect (SMD = 0,24; 95%-BI = -0,57-1,06) van oefentherapie met een duur van minder dan drie maanden (4 studies) op de ‘ziekteactiviteit’. Er bestaat een matig effect (SMD = 0,43; 95%-BI = -0,01-0,87) van oefentherapie met een duur van drie tot zes maanden (3 studies) op ‘ziekteactiviteit’. Er bestaat een gering effect (SMD = 0,03; 95%-BI = -0,46-0,52) van oefentherapie met een duur van meer dan zes maanden (2 studies) op ‘ziekteactiviteit’.
- De bewijskracht voor de uitkomstmaat ‘ziekteactiviteit’ bij een duur van minder dan drie maanden is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, gezien tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid). De bewijskracht voor de uitkomstmaat ‘ziekteactiviteit’ bij een duur van drie tot zes maanden is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, gezien beperkingen in onderzoeksopzet en methode en het geringe aantal patiënten (onnauwkeurigheid). De bewijskracht voor de uitkomstmaat ‘ziekteactiviteit’ bij een duur van meer dan zes maanden is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, gezien tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘radiologische schade’:
- Het effect van oefentherapie met een duur van minder dan drie maanden en met een duur van drie tot zes maanden op ‘radiologische schade’ is onbekend (0 studies). Er bestaat een gering effect (SMD = 0,09; 95%-BI = -0,14-0,31) van oefentherapie met een duur van meer dan zes maanden op ‘radiologische schade’ (2 studies).
- De bewijskracht voor de uitkomstmaat ‘radiologische schade’ bij een duur van meer dan zes maanden is met een niveaus verlaagd tot ‘redelijke kwaliteit van bewijs’, gezien het geringe aantal patiënten (onnauwkeurigheid).
GRADE-profiel van oefentherapie met een duur van minder dan drie maanden.[link]
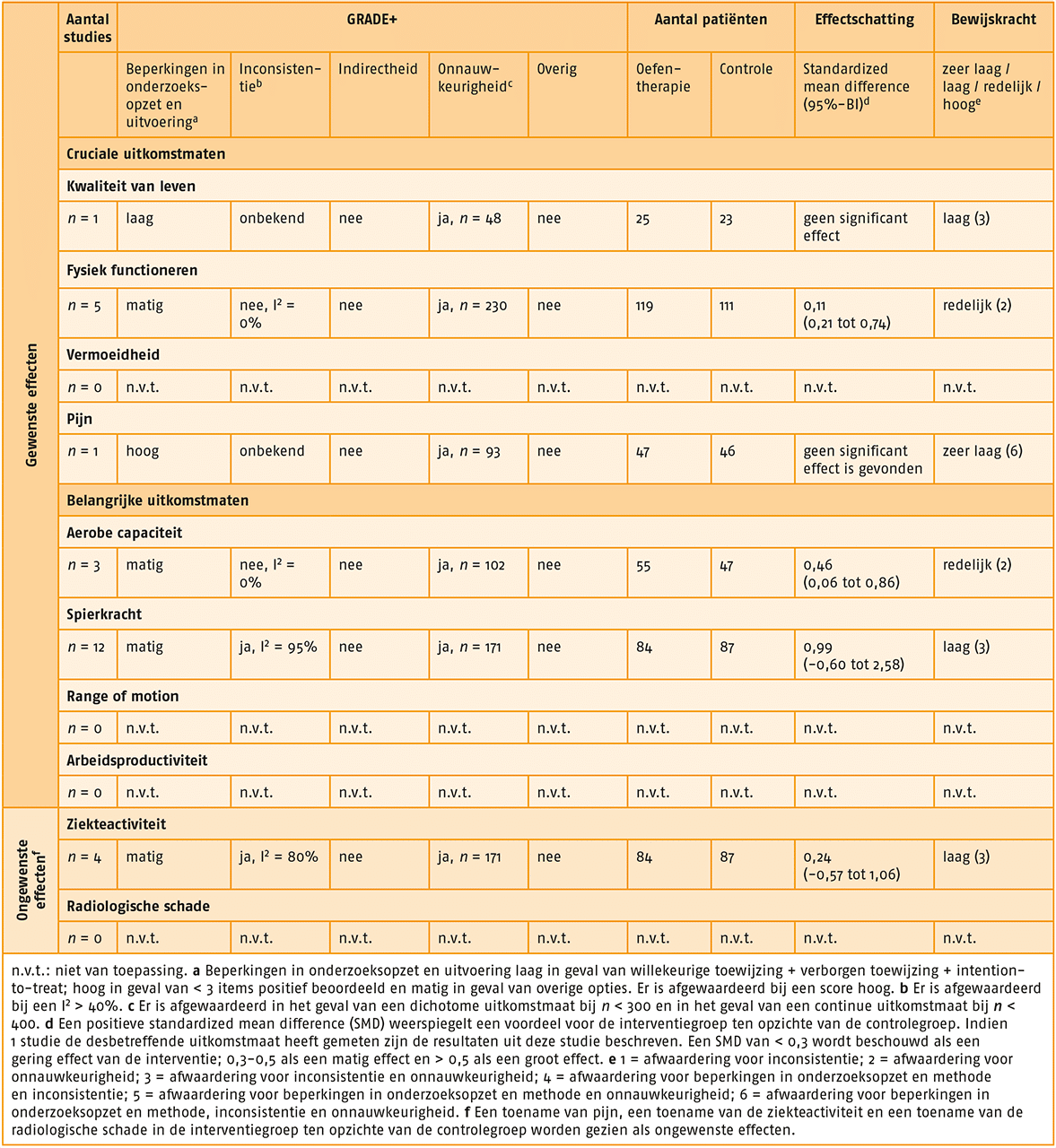
GRADE-profiel van oefentherapie met een duur van drie tot zes maanden.[link]
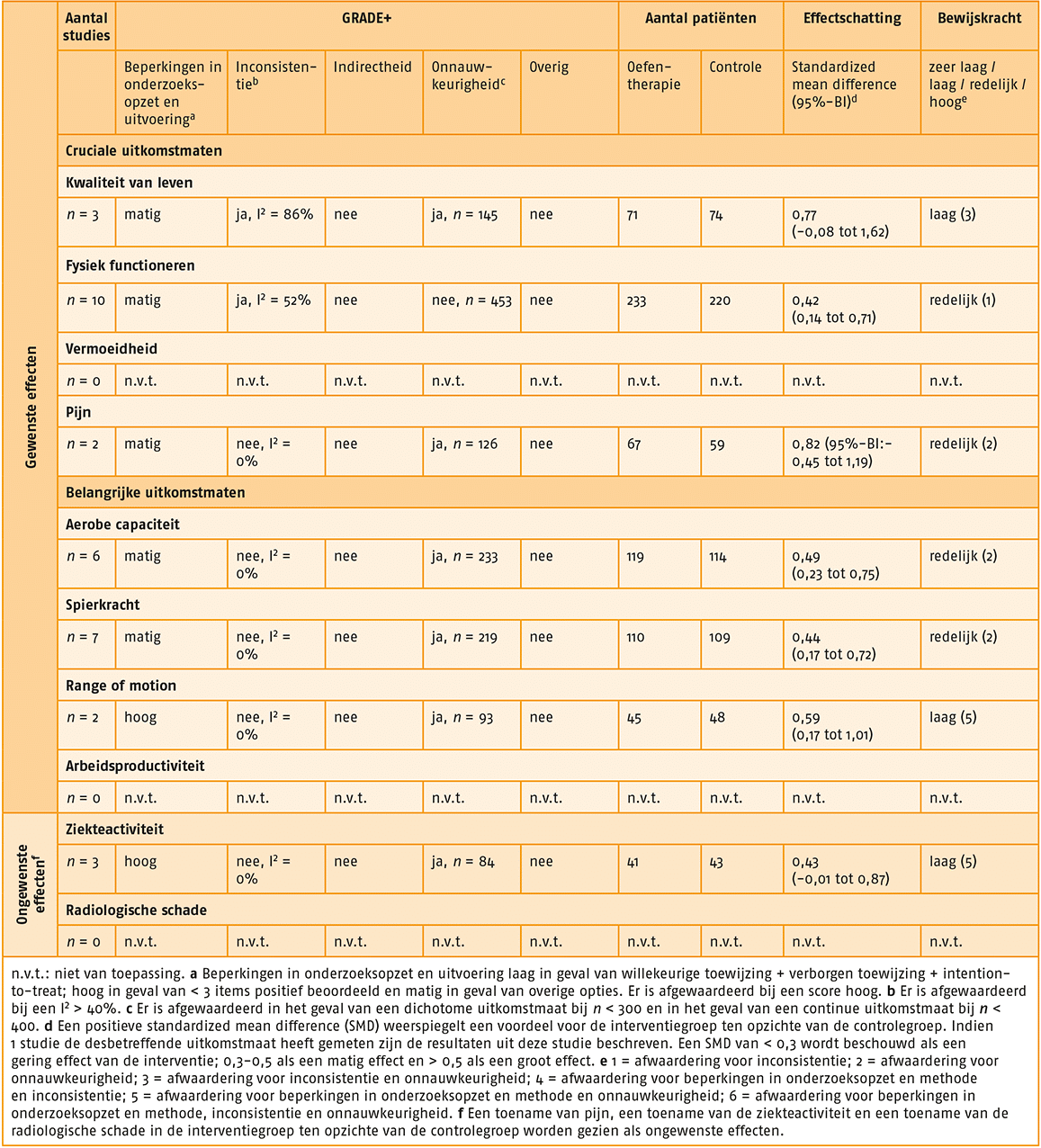
GRADE-profiel van oefentherapie met een duur van meer dan zes maanden.[link]
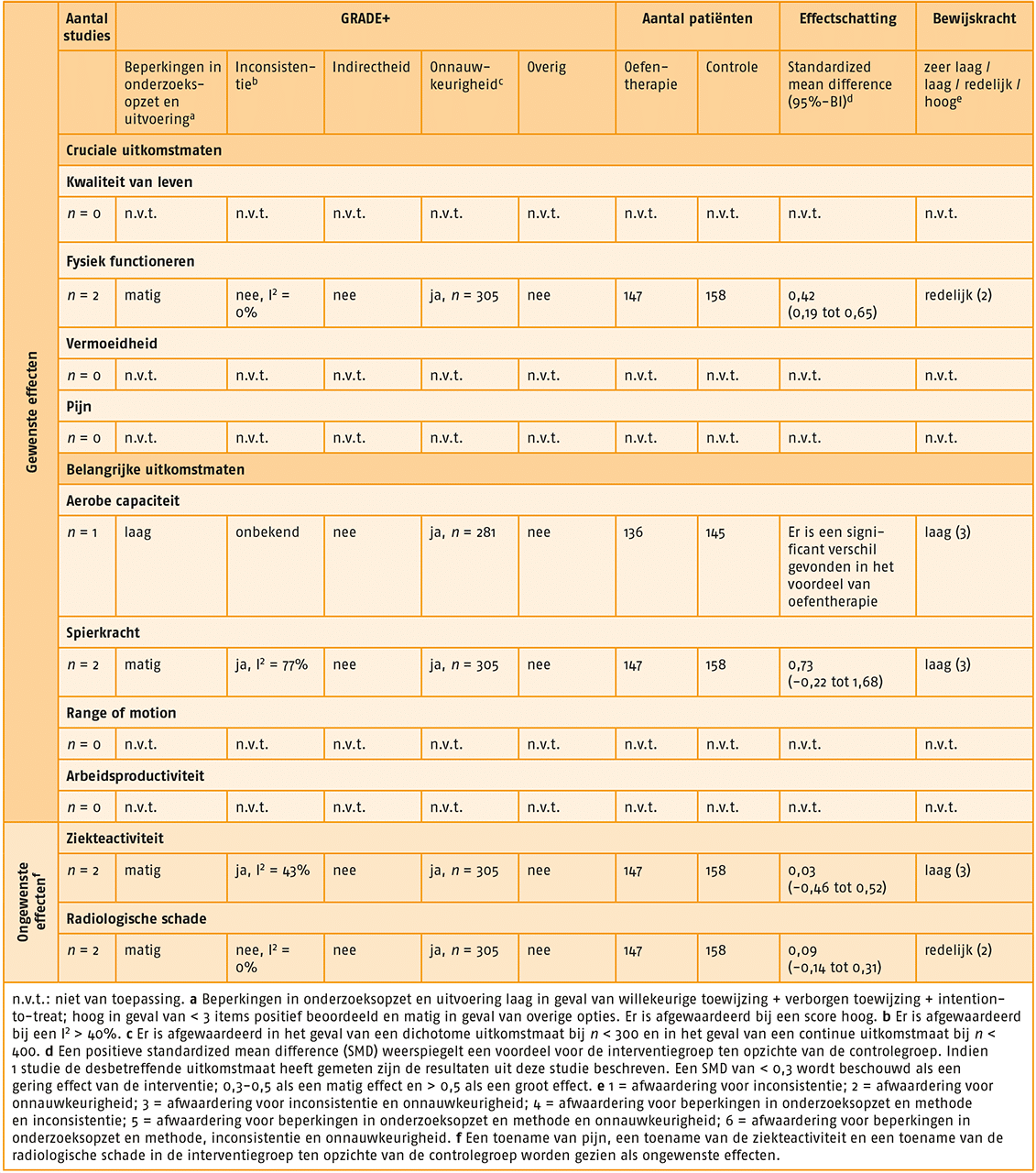
Van bewijs naar aanbeveling
Bij de formulering van de richting en de sterkte van de aanbeveling voor oefentherapie bij indicatie 1 heeft de werkgroep de volgende aanvullende overwegingen gemaakt.
- Op basis van de omvang van de effectschattingen en de kwaliteit van bewijs is de werkgroep van mening dat oefentherapie met een duur van drie tot zes maanden de voorkeur verdient. De werkgroep voegt hieraan toe dat het streven is de behandelperiode aan te vullen met een of enkele follow-upsessies tegen het einde of na afronding van de behandelperiode om therapietrouw te bevorderen en om de patiënt te stimuleren tijdens en na de behandelperiode zelfstandig te blijven oefenen en bewegen.
- Welke waarde patiënten aan een bepaalde tijdsduur hechten, en naar welke tijdsduur hun voorkeur uitgaat, zal waarschijnlijk van patiënt tot patiënt verschillen. De werkgroep schat in dat de meerderheid van de patiënten positief staat tegenover oefentherapie met een duur van drie tot zes maanden.
- De eventuele kosten voor de patiënt zijn bij een duur van drie tot zes maanden hoger dan bij een duur van minder dan drie maanden. De werkgroep is echter van mening dat dit kostenaspect wordt gecompenseerd doordat een langere tijdsduur een beter effect sorteert.
- De implementatie van oefentherapie met een duur van drie tot zes maanden in de dagelijkse praktijk wordt door de werkgroep als aanvaardbaar en haalbaar ingeschat, omdat deze duur als meest aangewezen optie wordt beschouwd.
Bronnen Noot 18
1. Baillet A, Payraud E, Niderprim VA, Nissen MJ, Allenet B, François P, Grange L, Casez P, Juvin R, Gaudin P. A dynamic exercise programme to improve patients’ disability in rheumatoid arthritis: a prospective randomized controlled trial. Rheumatology (Oxford). 2009 Apr;48(4):410-5.
2. Baslund B, Lyngberg K, Andersen V, Halkjaer Kristensen J, Hansen M, Klokker M, et al. Effect of 8 wk of bicycle training on the immune system of patients with rheumatoid arthritis. Journal of Applied Physiology 1993;75:1691-5.
3. Bearne LM, Scott DL, Hurley MV. Exercise can reverse quadriceps sensorimotor dysfunction that is associated with rheumatoid arthritis without exacerbating disease activity. Rheumatology (Oxford). 2002 Feb;41(2):157-66.
4. Bilberg A, Ahlmén M, Mannerkorpi K. Moderately intensive exercise in a temperate pool for patients with rheumatoid arthritis: a randomized controlled study. Rheumatology (Oxford). 2005 Apr;44(4):502-8.
5. Breedland I, van Scheppingen C, Leijsma M, Verheij-Jansen NP, van Weert E. Effects of a group-based exercise and educational program on physical performance and disease self-management in rheumatoid arthritis: a randomized controlled study. Phys Ther. 2011 Jun;91(6):879-93.
6. da Silva KN, Teixeira LE, Imoto AM, Atallah AN, Peccin MS, Trevisani VF. Effectiveness of sensorimotor training in patients with rheumatoid arthritis: a randomized controlled trial. Rheumatol Int. 2013 Sep;33(9):2269-75.
7. de Jong Z, Munneke M, Zwinderman AH, Kroon HM, Jansen A, Ronday KH, et al.Is a long-term high-intensity exercise program effective and safe in patients with rheumatoid arthritis? Results of a randomized controlled trial. Arthritis and Rheumatism 2003;48(9):2415-24.
8. Flint-Wagner HG, Lisse J, Lohman TG, Going SB, Guido T, Cussler E, Gates D, Yocum DE. Assessment of a sixteen-week training program on strength, pain, and function in rheumatoid arthritis patients. J Clin Rheumatol. 2009 Jun;15(4):165-71,
9. Häkkinen A, Häkkinen K, Hannonen P. Effects of strength training on neuromuscular function and disease activity in patients with recent-onset inflammatory arthritis. Scand J Rheumatol. 1994;23(5):237-42.
10. Hansen TM, Hansen G, Langgaard AM, Rasmussen JO. Longterm physical training in rheumatoid arthritis. A randomized trial with different training programs and blinded observers. Scandinavian Journal of Rheumatology 1993;22(3):107-12.
11. Harkcom TM, Lampman RM, Banwell BF, Castor CW. Therapeutic value of graded aerobic exercise training in rheumatoid arthritis. Arthritis and Rheumatism 1985;28(1):32-9.
12. Lemmey AB, Marcora SM, Chester K, Wilson S, Casanova F, Maddison PJ. Effects of high-intensity resistance training in patients with rheumatoid arthritis: a randomized controlled trial. Arthritis Rheum. 2009 Dec 15;61(12):1726-34.
13. Lyngberg KK, Harreby M, Bentzen H, Frost B. Elderly rheumatoid arthritis on steroid treatment tolerate physical training without an increase in disease activity. Archives of Physical Medicine and Rehabilitation 1994;75:1189-95.
14. McMeeken J, Stillman B, Story I, Kent P, Smith J. The effects of knee extensor and flexor muscle training on the timed-up-and-go test in individuals with rheumatoid arthritis. Physiother Res Int. 1999;4(1):55-67.
15. Minor MA, Hewett JE, Webel RR, Anderson SK, Kay DR. Efficacy of physical conditioning exercise in patients with rheumatoid arthritis and osteoarthritis. Arthritis and Rheumatism 1989;32(11):1396-405.
16. Sanford-Smith S, Mackay-Lyons M, Nunes-Clement S. Therapeutic benefit of aquaerobics for individuals with rheumatoid arthritis. Physiotherapy Canada 1998;Winter:40-6.
17. Siqueira US, Orsini Valente LG, de Mello MT, Szejnfeld VL, Pinheiro MM. Effectiveness of Aquatic Exercises in Women With Rheumatoid Arthritis: A Randomized, Controlled, 16-Week Intervention-The HydRA Trial. Am J Phys Med Rehabil. 2017 Mar;96(3):167-175.
18. Strasser B, Leeb G, Strehblow C, Schobersberger W, Haber P, Cauza E. The effects of strength and endurance training in patients with rheumatoid arthritis. Clin Rheumatol. 2011 May;30(5):623-32.
19. Van den Ende CHM, Hazes JMW, Le Cessie S, Mulder WJ, Belfor DG, Breedveld FC, Dijkmans BA. Comparison of high and low intensity training in well controlled rheumatoid arthritis. Results of a randomized clinical trial. Annals of the Rheumatic Diseases 1996;55(11):798-805.
Toelichting C.3.4-Indicatie 3
Aanleiding
De fysio- of oefentherapeut begeleidt de patiënt bij het proces van het voorkomen of verminderen van en/of het leren omgaan met beperkingen in activiteiten van het dagelijks leven en maatschappelijke participatie ten gevolge van (RA). De belangrijkste middelen om dit doel te bereiken zijn het geven van oefentherapie, voorlichting en advies .
In 2024 is de ‘Longstanding EXercise Therapy for people with Rheumatoid Arthritis’ (L-EXTRA)-studie naar de effecten van langdurige gesuperviseerde actieve oefentherapie gepubliceerd (3).
Naar aanleiding van deze L-EXTRA-studie is er door het Zorginstituut geconcludeerd dat langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie (≥ 52 weken) onder supervisie van een fysio- of oefentherapeut beschouwd kan worden als effectieve behandeling bij volwassen patiënten (≥ 18 jaar) met RA met ernstige functionele beperkingen in het dagelijks leven. Deze interventie voldoet bij de genoemde indicatie daarom aan ‘de stand van de wetenschap en praktijk’.
Naar aanleiding van dit onderzoek is de minister geadviseerd om, gelet op de weging van de vier pakketcriteria (de ‘stand van de wetenschap en praktijk’, kosteneffectiviteit, noodzakelijkheid en uitvoerbaarheid), langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie bij deze indicatie op te nemen in de basisverzekering. De minister is hiermee akkoord gegaan onder de voorwaarde dat onder andere de huidige KNGF-richtlijn Reumatoïde artritis (2018) wordt herzien op twee modules, namelijk B.4 ‘Indicatiestelling’ en C.2.3 ‘Indicatie 3: Oefentherapie met intensieve begeleiding’.
Naast de herziening van de bovengenoemd modules, geeft de L-EXTRA-studie ook nieuwe inzichten over de duur van de behandeling van patiënten met RA met ernstige functionele beperkingen. In de herziening van deze module zal specifiek worden ingegaan op de duur van langdurige gepersonaliseerde gesuperviseerde actieve fysio- of oefentherapie voor patiënten met RA met ernstige functionele beperkingen.
Rationale van de aanbeveling
De werkgroep heeft besloten om een sterke aanbeveling te formuleren voor gepersonaliseerde gesuperviseerde actieve oefentherapie bij patiënten met RA met ernstige functionele beperkingen (indicatie 3) voor de duur van ≥ 52 weken. Deze duur is geformuleerd op basis van de gevonden literatuur vanuit het systematische literatuuronderzoek in C.2.3, namelijk de L-EXTRA-studie. Deze L-EXTRA-studie laat zien dat bij patiënten met RA met ernstige functionele beperkingen langdurige (≥ 52 weken) gepersonaliseerde gesuperviseerde actieve oefentherapie geen (belangrijke) bijwerkingen geeft en resulteert in overwegend klinisch relevante effecten op de cruciale uitkomstmaten. De werkgroep benadrukt dat deze duur verlengd wordt, zolang er een indicatie bestaat voor de behandeling van deze patiënten (zie module B.4 ‘Indicatiestelling’). De werkgroep stelt dat deze duur van de interventie voor patiënten met RA met ernstige functionele beperkingen gewaardeerd wordt door patiënten en dat de overige criteria van het EtD-proces (economische overwegingen en kosteneffectiviteit, gelijkheid, aanvaarbaarheid en haalbaarheid) grotendeels als haalbaar en realistisch worden beschouwd.
Conclusies op basis van de literatuur
Voor het beantwoorden van deze uitgangsvraag is gebruikgemaakt van de beschreven duur vanuit de gevonden literatuur in het systematisch literatuuronderzoek, uitgewerkt in de module C.2.3 ‘Oefentherapie met intensieve begeleiding’ (opent in nieuw tabblad).
In deze module (C.2.3) is het effect van langdurige (≥ 52 weken) gepersonaliseerde gesuperviseerde actieve oefentherapie bij patiënten met RA met ernstige functionele beperkingen in het dagelijks leven geëvalueerd. De conclusie hiervan was dat bij patiënten met RA met ernstige functionele beperkingen langdurige gesuperviseerde actieve oefentherapie geen (belangrijke) bijwerkingen geeft en resulteert in klinisch relevante effecten op de cruciale uitkomsten: fysiek functioneren en fysieke kwaliteit van leven.
Deze bevindingen zijn tot stand gekomen op basis van een systematisch literatuuronderzoek, waarbij de beschreven effecten zijn gebaseerd op één studie, namelijk de L-EXTRA-studie (1). In onderstaand ‘Van bewijs naar aanbeveling – overwegingen’ wordt de beschreven duur voor deze studie toegelicht.
L-EXTRA-studie
De interventie bestond uit het vaststellen van gepersonaliseerde behandeldoelen en behandelmodaliteiten
(aerobe capaciteit, spierkrachttraining, flexibiliteit, gewricht range of motion en functioneel trainen van motorische vaardigheden, patiënteducatie en stimuleren van lichamelijke activiteit). Er werden 2 sessies per week gedurende de eerste 12 weken gehanteerd. Daarna moest de frequentie worden afgebouwd naar 1 keer per week (totaal 64 sessies), met 14 optionele sessies, afhankelijk van de behoeftes van de patiënt.
Er werden 394 deelnemers gescreend op de in- en exclusiecriteria. Tijdens de screening zijn 177 deelnemers (45%) afgevallen, waarvan 74 deelnemers omdat de functionele beperkingen niet ernstig genoeg waren en 19 deelnemers omdat de diagnose niet werd bevestigd door de reumatoloog. Er werden 217 patiënten gerandomiseerd in de interventiegroep en controlegroep. Na 1 uitvaller in beide groepen zaten er 109 patiënten in de interventiegroep en 106 in de controlegroep. De metingen waren bij 52 weken compleet van 105 patiënten in de interventiegroep en 99 in de controlegroep. In de ITT- analyse zitten 104 patiënten van de interventiegroep en 98 van de controlegroep, omdat in beide groepen van 1 patiënt de metingen niet voltooid waren binnen het vooraf gedefinieerde tijdsbestek van 6 weken. Van de 109 patiënten in de interventiegroep maakten 99 patiënten (91%) daadwerkelijk gebruik van de interventie in de eerste 52 weken. Het gemiddeld aantal sessies van deze 99 patiënten was 39. In de controlegroep maakten 70 patiënten (66%) gebruik van fysio- of oefentherapie. Tussen 52 en 104 weken maakten 74 van de 105 patiënten (70%) uit de interventiegroep, die op 52 weken nog in de studie zaten, gebruik van de interventie. Het gemiddeld aantal sessies van deze patiënten was 20 (SD 16). Het tijdstip van de 104 weken of eindmeting varieerde tussen de 80 en 122 weken ten opzichte van de baseline. Van de 99 patiënten die gebruikelijke zorg kregen en die op 52 weken nog in de studie zaten, maakten 61 patiënten (62%) gebruik van de interventie.
In de L-EXTRA-studie werd voorafgaand aan het onderzoek een aantal van 64-78 behandelingen in het eerste jaar (24 behandelingen in de eerste 12 weken en 40 in de volgende 40 weken en 14 optioneel in geval van progressie of exacerbatie van de problematiek) en 52 behandelingen in de daarna volgende jaren beoogd. Het gemiddeld aantal sessies lag echter lager in zowel het eerste als het tweede jaar. Een verklaring wordt gezocht in de COVID-19-pandemie. Door deze pandemie is de studie enige tijd geheel stilgelegd. Ook heeft de studie te lijden gehad onder maatregelen zoals quarantaine van patiënten en behandelaars, en terughoudendheid van deze groep patiënten met een kwetsbare gezondheid om de kans op besmetting te minimaliseren.
De effecten op de uitkomstmaten (52 weken) zijn beschreven in module C.3.2. Hieronder worden de effecten van langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie op de uitkomstmaten tussen de 52 en 104 weken gerapporteerd:
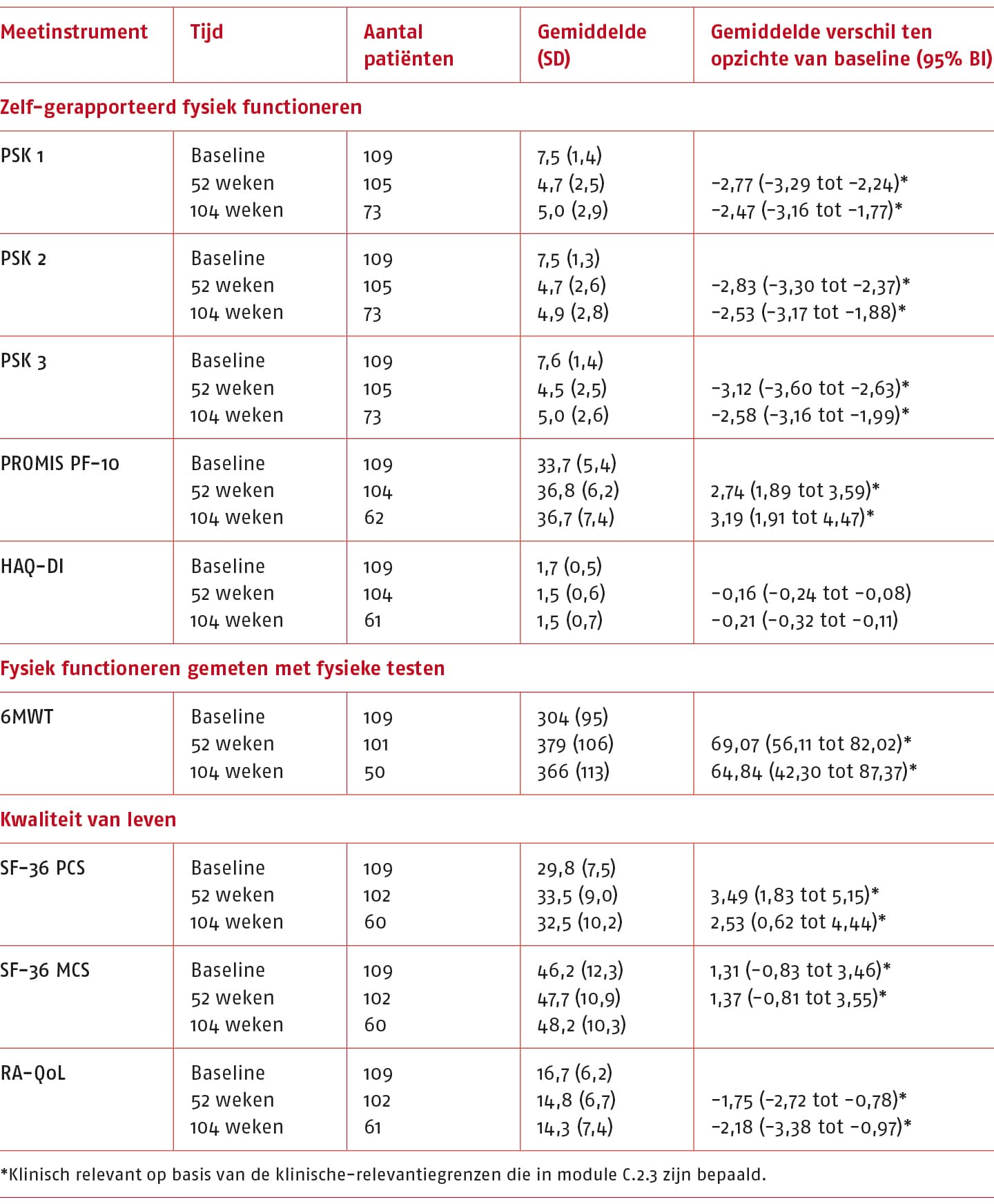
De resultaten op 104 weken (range 80-122) zijn voor alle uitkomsten in de interventiegroep significant beter dan op baseline. De scores tussen 52 en 104 weken blijven nagenoeg gelijk op alle uitkomstmaten, wat indiceert dat de effecten aanhouden als de patiënten in de interventiegroep de langdurige personaliseerde gesuperviseerde actieve oefentherapie voortzetten. Er zijn geen gegevens over het al dan niet aanhouden van het effect in de groep patiënten die de interventie niet voortzetten.

Van bewijs naar aanbeveling – overwegingen
Effecten en kwaliteit van bewijs
Het onderdeel van bewijs naar aanbeveling bevat een negental criteria.
In deze module is bij het beantwoorden van de uitgangsvraag geen bewijskracht vastgesteld. De bewijskracht van langdurige gepersonaliseerde, gesuperviseerde actieve oefentherapie is uitgewerkt in module C.2.3 ‘Oefentherapie met intensieve begeleiding’. Om die reden heeft de werkgroep geen gewenste effecten, ongewenste effecten, kwaliteit van bewijs en balans van gewenste en ongewenste effecten (vier van de negen criteria) geformuleerd.
1. Waarden en voorkeuren van patiënten
De werkgroep heeft de ervaring dat de patiënten grote waarde hechten aan langdurige, gepersonaliseerde gesuperviseerde actieve oefentherapie. De ervaring is dat patiënten met RA behoefte hebben aan langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie, gericht op de hulpvraag. De ervaring is dat RA-patiënten met ernstige functionele beperkingen ook na 52 weken een actieve hulpvraag hebben (of ontwikkelen) en daarbij ondersteuning wensen van de fysio- of oefentherapeut.
Deze ervaring wordt bevestigd door data vanuit de L-EXTRA-studie (Bijlage C.3.4-1 (opent in nieuw tabblad)). Hierin zien we dat het globaal waargenomen effect als 2 (mediaan (IQR: 2-3)) wordt beschreven, waarbij 1 een zeer sterk verbeterd en 7 een zeer sterk verslechterd effect betekent.
2. Economische overwegingen en kosteneffectiviteit
Voor fysio- en oefentherapeuten wordt de eis gesteld dat zij een verplichte scholing volgen om deze specifieke patiëntengroep te kunnen behandelen. De kosten die hiermee gepaard gaan, zijn wel een investering, echter de werkgroep ervaart deze als laag. De benodigde middelen voor het uitvoeren van langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie worden als verwaarloosbaar beoordeeld.
De maatschappelijke kosten zijn wat de werkgroep betreft onduidelijk. In de L-EXTRA-studie is ook een economische evaluatie uitgevoerd (2). In de module C.2.3 ‘Oefentherapie met intensieve begeleiding ’ zijn de resultaten van de onderzoekers beschreven. De werkgroep geeft aan dat het niet duidelijk is hoe deze maatschappelijke kosten uiteindelijk zullen zijn. Mogelijk neemt het aantal patiënten met RA met ernstige functionele beperkingen af ten gevolge van verbeterde behandeling (o.a. medicatie), en kan deze populatie meer participeren in de maatschappij. Dit zijn onzekere factoren.
3. Gelijkheid
De werkgroep verwacht dat het langdurig uitvoeren van de gepersonaliseerde gesuperviseerde actieve oefentherapie niet zal leiden tot een toename of afname van de gezondheidsgelijkheid. Hierbij wordt ervan uitgegaan dat de fysio- of oefentherapeutische zorg van patiënten met RA met ernstige functionele beperkingen al is opgenomen in het basispakket. Het wel of niet toepassen van deze interventie, binnen het basispakket, heeft (ook voor specifieke patiëntencategorieën) geen gevolgen.
4. Aanvaardbaarheid
De werkgroep verwacht dat het langdurig uitvoeren van gepersonaliseerde gesuperviseerde actieve oefentherapie door alle key stakeholders zal worden geaccepteerd. De middelen die van de therapeut geëist worden (tijd en trainingsinvestering), worden door de werkgroep als verwaarloosbaar beschouwd en wegen op tegen het mogen toepassen van deze interventie bij deze specifieke patiëntengroep.
De werkgroep benadrukt dat er een verantwoordelijkheid bij de fysio- of oefentherapeut en patiënt ligt dat als er geen indicatie meer is, de behandeling gestopt dient te worden. De werkgroep spreekt uit dat zij er vertrouwen in heeft dat dit wordt toegepast, mede gezien de afname van frequentie en aantal patiënten die deelnamen in de L-EXTRA-studie, en ook door het hedendaags fysio- en oefentherapeutisch handelen.
5. Haalbaarheid
De implementatie van langdurige gepersonaliseerde gesuperviseerde actieve oefentherapie wordt als realistisch beoordeeld.
Eventuele additionele overwegingen
Er zijn geen additionele overwegingen geformuleerd.
Aandachtspunten voor implementatie
Zie het onderdeel ‘haalbaarheid’.
Daarnaast worden er acties ingezet om het aantal behandelingen te monitoren. Jaarlijks zal het aantal unieke patiënten dat de behandeling declareert op jaarbasis gemonitord worden vanaf 2026 t.m 2030 en vergeleken worden met de te verwachtte patiënten aantallen in dit advies. Aanvullend zal ook het gemiddeld aantal behandelingen per patiënt en het verloop hiervan na pakketopname gemonitord worden.
De werkgroep is van mening dat de therapeut dicht bij de gehanteerde frequenties van de genoemde L-EXTRA -studie dient te blijven: Twee sessies per week gedurende de eerste 12 weken. Daarna moest de frequentie worden afgebouwd naar één keer per week (totaal 64 sessies), met 14 optionele sessies, afhankelijk van de behoeftes van de patiënt in de eerste twee jaren.
Kennislacunes
Er zijn geen kennislacunes geformuleerd.
Overige informatie C.3.4-Indicatie 3
Initiatiefnemers
Het initiatief voor deze modulaire herziening lag bij het Koninklijk Nederlands Genootschap Fysiotherapie (KNGF), in samenwerking met de Vereniging van Oefentherapeuten Cesar en Mensendieck (VvOCM).
Betrokkenheid van belanghebbenden (auteurs)
Voor het ontwikkelen van de richtlijnmodule is in 2024 een projectgroep samengesteld, bestaande uit een kerngroep en een multidisciplinaire werkgroep. De werkgroep bestaat uit vertegenwoordigers van alle primair betrokken professionals bij de zorg voor RA. De werkgroep werd ondersteund in de ontwikkeling door richtlijnadviseurs vanuit het KNGF en de VvOCM.
De rollen en taken van de belanghebbenden van de richtlijn worden beschreven in de KNGF-richtlijnenmethodiek (8).
Richtlijnadviseurs KNGF en VvOCM

Werkgroep

Belangen
Voorafgaand aan en bij afsluiting van het project hebben alle projectgroep leden een belangenverklaring ingevuld. De belangenverklaringen zijn beoordeeld door de richtlijnadviseurs en indien nodig (bij een ‘conflict of interest’) werden gedurende het richtlijnproject maatregelen getroffen (bijv. het niet participeren in het proces ‘van bewijs naar aanbeveling’ in de werk- of klankbordgroep) om (schijn van) oneigenlijke beïnvloeding door belangenverstrengeling zo veel mogelijk te voorkomen, conform de KNGF-richtlijnenmethodiek 2022. (9)
In de belangenverklaringen is een overzicht opgenomen met de affiliaties (de organisatie of instelling en plaats van werkzaamheden) van de leden van de projectgroep.

Autoriserende partijen
De volgende partijen hebben deze module geautoriseerd:
- Koninklijk Nederlands Genootschap Fysiotherapie (KNGF);
- Vereniging van Oefentherapeuten Cesar en Mensendieck (VvOCM);
- Nederlandse Vereniging voor Reumatologie (NVR);
- ReumaNederland;
- Vereniging voor Sportgeneeskunde (VSG);
- Nationale Vereniging Reumazorg Nederland.
De volgende partij heeft een verklaring van geen bezwaar afgegeven:
- Nederlands Huisartsen Genootschap (NHG).
Geldigheid en onderhoudsprocedure
Publicatiedatum:5 december 2024
Laatst beoordeeld:5 december 2024
Laatst geautoriseerd:5 december 2024
De eerstvolgende beoordeling op actualiteit vindt plaats in 2029.
Zie de KNGF-richtlijnenmethodiek voor informatie over het beleid wat betreft richtlijnenonderhoud.
Financiering
De ontwikkeling van deze module is gefinancierd door het KNGF.
Toepassing van de KNGF-richtlijnenmethodiek
De ontwikkeling van deze module heeft plaatsgevonden volgens de KNGF-richtlijnenmethodiek 2022. Deze methodiek is gebaseerd op het AGREE II-instrument en de AQUA-leidraad. Binnen de KNGF-richtlijnenmethodiek wordt gebruikgemaakt van GRADE voor de beoordeling van de bewijskracht en voor het proces van ‘evidence to decision’(18).
Bijlage C.3.4-Indicatie 3
Bronnen C.3.4-Indicatie 3
- Teuwen MMH, van Weely SFE, Vliet Vlieland TPM, van Wissen MAT, Peter WF, den Broeder AA, et al. Effectiveness of longstanding exercise therapy compared with usual care for people with rheumatoid arthritis and severe functional limitations: a randomised controlled trial. Ann Rheum Dis. 2024;83(4):437-45.
- Akl EA, Welch V, Pottie K, Eslava-Schmalbach J, Darzi A, Sola I, et al. GRADE equity guidelines 2: considering health equity in GRADE guideline development: equity extension of the guideline development checklist. J Clin Epidemiol. 2017;90:68-75.
- Zorginstituut Nederland. AQUA-Leidraad: Zorginstituut Nederland; 2021 [Available from: https://www.zorginzicht.nl/ontwikkeltools/ontwikkelen/aqua-leidraad (opent in nieuw tabblad).
- Koninklijk Nederlands Genootschap voor Fysiotherapie, Vreeken H, Van Doormaal MCM, Conijn D, Meerhoff G, Swart N. KNGF-richtlijnenmethodiek: ontwikkeling en implementatie van KNGF-richtlijnen, versie 3 Amersfoort: Koninklijk Nederlands Genootschap voor Fysiotherapie (KNGF); 2022 Richtlijnontwikkeling | Kennisplatform Fysiotherapie
C.3.5 Algemene factoren
Aanbevelingen
- Begeleid en motiveer de patiënt bij het bewegen wanneer bij RA-specifieke barrières, zoals pijn, stijfheid, vermoeidheid en angst (bijvoorbeeld angst om de ziekte te verergeren).
- Overweeg bij patiënten met handproblematiek een specifiek oefenprogramma voor de hand. De patiënt kan hiervoor worden doorverwezen naar een fysiotherapeut, een oefentherapeut of een ergotherapeut met specifieke deskundigheid op het gebied van de (reumatische) hand.
- Overweeg oefentherapie in het water in de beginfase van de behandeling bij ernstige pijnklachten tijdens het oefenen.
- Overweeg de MET-methode te gebruiken bij het inschatten van het inspanningsvermogen.
- Overweeg e-healthtoepassingen om de patiënt te ondersteunen in het zelfstandig (blijven) uitvoeren van oefeningen en/of om de mate van begeleiding te verminderen.
- Overweeg oefentherapie in groepsverband indien weinig individuele begeleiding nodig is.
Onderbouwing
Noot 19
Uitgangsvraag
Aan welke algemene factoren moet de oefentherapie bij patiënten met RA voldoen?
Deze uitgangsvraag is beantwoord door de algemene factoren waaraan oefentherapie bij patiënten met RA moet voldoen te beschrijven, gebaseerd op de ACSM-richtlijn.[1]
Voor de effectiviteit van oefentherapie bij patiënten met handproblematiek en de effectiviteit van oefentherapie in het water zijn literatuurstudies uitgevoerd.
Oefentherapie bij patiënten met handproblematiek
Conclusie vanuit de literatuurstudie
De literatuur toont een groot effect van handoefeningen op de uitkomstaat ‘fysiek functioneren’, met een lage kwaliteit van bewijs. Het effect van handoefeningen op de uitkomstmaten ‘kwaliteit van leven’, ‘vermoeidheid’ en ‘pijn’ is onbekend.
Van bewijs naar aanbeveling
Op basis van het effect van handoefeningen op fysiek functioneren en de beperkte ongewenste effecten (ziekteactiviteit neemt niet toe als gevolg van handoefeningen) en de hoge aanvaardbaarheid en haalbaarheid van handoefeningen is de werkgroep van mening dat handtherapie overwogen kan worden voor patiënten met handproblematiek.
Aanbeveling voor handoefeningen
Overweeg bij patiënten met handproblematiek een specifiek oefenprogramma voor de hand. De patiënt kan hiervoor worden doorverwezen naar een fysiotherapeut, een oefentherapeut of een ergotherapeut met specifieke deskundigheid op het gebied van de (reumatische) hand.
Oefentherapie op het droge versus oefentherapie in het water
Conclusie vanuit de literatuurstudie
De effectiviteit van oefentherapie op het droge versus oefentherapie in het water op de uitkomstmaten ‘kwaliteit van leven’, ‘fysiek functioneren’, ‘vermoeidheid’ en ‘pijn’ is onbekend.
Van bewijs naar aanbeveling
De literatuur geeft geen uitsluitsel over de effectiviteit van oefentherapie op het droge versus oefentherapie in het water. De werkgroep is van mening dat oefentherapie in het water overwogen kan worden bij ernstige pijnklachten in de beginfase van de behandeling, afhankelijk van de voorkeuren van de patiënt in een specifieke situatie.
Aanbeveling voor oefentherapie op het droge versus oefentherapie in het water
Overweeg oefentherapie in het water in de beginfase van de behandeling bij ernstige pijnklachten tijdens het oefenen.
Complete uitgangsvraag volgens PICO
Voor de beantwoording van deze uitgangsvraag is een gezamenlijke PICO uitgangsvraag geformuleerd voor de frequentie, intensiteit, type en duur van oefentherapie (zie noot 14).
Zoekstrategie
Er is een gezamenlijke zoekactie uitgevoerd voor de frequentie, intensiteit, type en duur van oefentherapie (zie noot 14).
Gevonden literatuur
De zoekactie van de literatuur leverde 1837 referenties op. Vier gerandomiseerde gecontroleerde onderzoeken voldeden aan de inclusiecriteria voor de beantwoording van de uitgangsvraag met betrekking tot de effectiviteit van oefentherapie bij patiënten met handproblematiek [2-5] en twee studies voldeden aan de inclusiecriteria met betrekking tot de effectiviteit van oefentherapie op het droge versus oefentherapie in het water.[6,7]
Oefentherapie bij patiënten met handproblematiek
Beschrijving studies
In vier studies is de effectiviteit van specifieke handoefeningen onderzocht [2-5], waarbij in één studie een vergelijking is gemaakt tussen isotonische en isometrische handoefeningen.[2]
Effectiviteit en bewijskracht
De beoordeling van de onderzoeksopzet en uitvoering van de geselecteerde artikelen is opgenomen in de bijlage (opent in nieuw tabblad) van deze noot.
Hierna volgt per uitkomstmaat een beschrijving van de effectiviteit van handoefeningen, en de bewijskracht daarvoor. Zie ook het GRADE-profiel van handoefeningen.
Gewenste effecten
Cruciale uitkomstmaten
- Uitkomstmaat ‘kwaliteit van leven’ (1 studie):
- Het effect van handoefeningen op de kwaliteit van leven is onbekend (SMD niet beschikbaar).
- De bewijskracht voor de uitkomstmaat ‘kwaliteit van leven’ is hoog; er heeft geen afwaardering plaatsgevonden.
- Uitkomstmaat ‘fysiek functioneren’ (3 studies):
- Er bestaat een groot effect (SMD = 0,61; 95%-BI = 0,04-1,18) van handoefeningen op fysiek functioneren.
- De bewijskracht voor de uitkomstmaat ‘fysiek functioneren’ is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, gezien beperkingen in de onderzoeksopzet en uitvoering en tegenstrijdige resultaten (inconsistentie).
- Uitkomstmaat ‘vermoeidheid’ (0 studies):
- het effect en de bewijskracht van handoefeningen op de vermoeidheid is onbekend.
- Uitkomstmaat ‘pijn’ (1 studie):
- Het effect van handoefeningen op de pijn is onbekend (SMD niet beschikbaar).
- De bewijskracht voor de uitkomstmaat ‘pijn’ is hoog; er heeft geen afwaardering plaatsgevonden.
Belangrijke uitkomstmaten
- Uitkomstmaat ‘aerobe capaciteit’ (0 studies):
- Het effect en de bewijskracht van handoefeningen op de aerobe capaciteit is onbekend.
- Uitkomstmaat ‘spierkracht’ (2 studies):
- Er bestaat een matig effect (SMD = 0,34; 95%-BI = -0,25-0,93) van handoefeningen op de spierkracht.
- De bewijskracht voor de uitkomstmaat spierkracht is met een niveau verlaagd tot ‘redelijke kwaliteit van bewijs’, gezien tegenstrijdige resultaten (inconsistentie).
- Uitkomstmaat ‘range of motion’ (2 studies):
- Er bestaat een gering effect (SMD = 0,09; 95%-BI = -0,08-0,26) van handoefeningen op de range of motion. De bewijskracht voor de uitkomstmaat range of motion is hoog.
- Uitkomstmaat ‘arbeidsproductiviteit’ (1 studie):
- Het effect van handoefeningen op de arbeidsproductiviteit is onbekend (SMD niet beschikbaar).
Ongewenste effecten
- Uitkomstmaat ‘ziekteactiviteit’ (1 studie):
- Het effect van handoefeningen op de ziekteactiviteit is onbekend (SMD niet beschikbaar).
- Uitkomstmaat ‘radiologische schade’ (0 studie):
- Het effect van handoefeningen op de radiologische schade is onbekend.
GRADE-profiel van handoefeningen. [link]
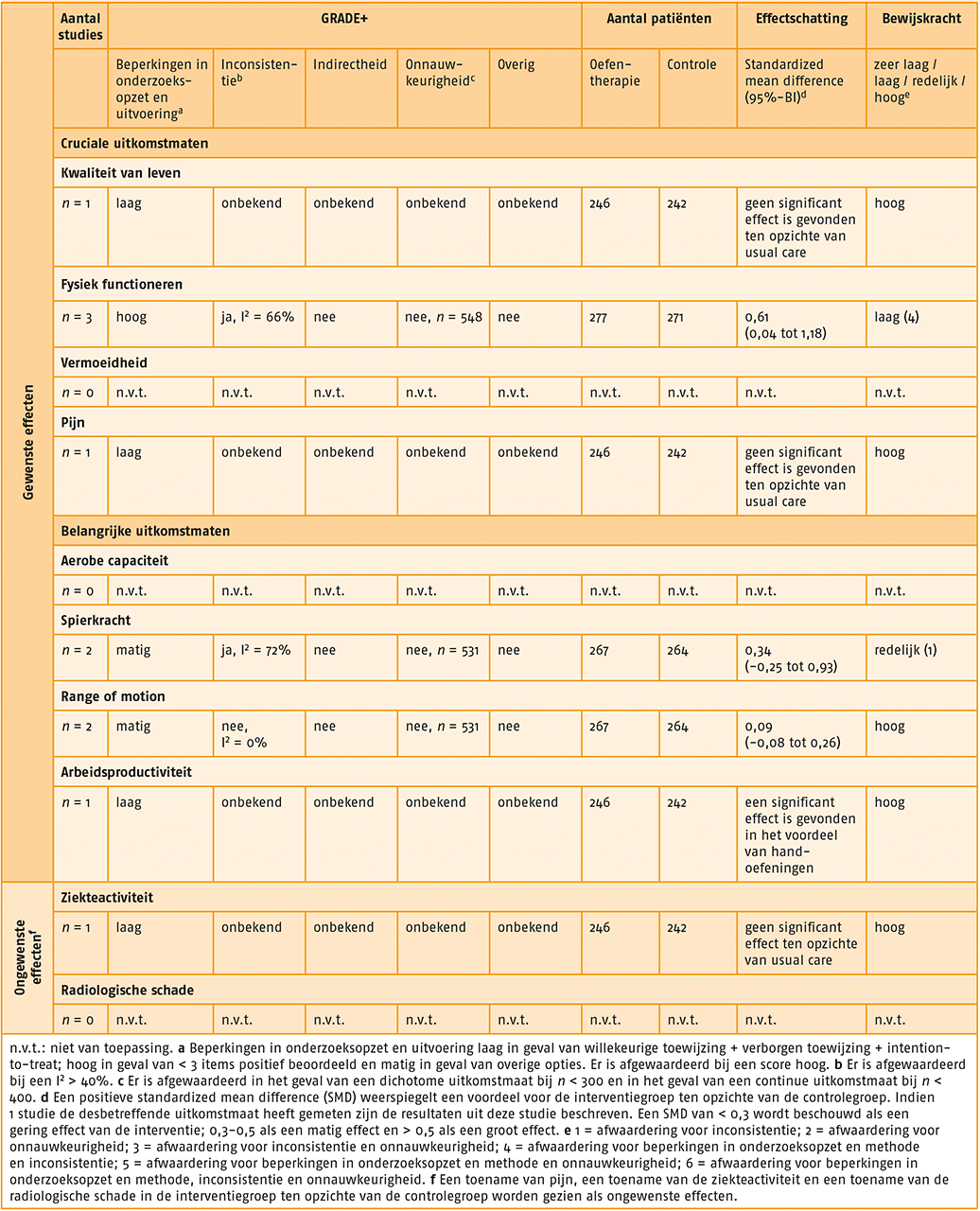
Van bewijs naar aanbeveling
Bij de formulering van de aanbeveling (richting en sterkte) voor oefentherapie bij indicatie 1 zijn de volgende aanvullende overwegingen gemaakt.
- De gewenste effecten van handtherapie op fysieke functioneren zijn aanwezig, terwijl de ongewenste effecten (zoals een toename van de ziekteactiviteit) zeldzaam lijkt. Alhoewel de effectschattingen van beperkte omvang zijn en er onzekerheid is over de waarschijnlijkheid van de effectschattingen, is de werkgroep van mening dat de gewenste effecten de ongewenste effecten overstijgen.
- Welke waarde patiënten aan handoefeningen hechten, zal waarschijnlijk van patiënt tot patiënt verschillen. De werkgroep schat in dat de meerderheid van de patiënten met handproblematiek positief staat tegenover handoefeningen.
- De implementatie van handoefeningen in de dagelijkse praktijk wordt door de werkgroep als aanvaardbaar en haalbaar ingeschat.
Oefentherapie op het droge versus oefentherapie in het water
Beschrijving studies
In twee studies is een vergelijking gemaakt tussen oefentherapie op het droge en oefentherapie in het water.[6,7]
Effectiviteit en bewijskracht
De beoordeling van de onderzoeksopzet en uitvoering van de geselecteerde artikelen is opgenomen in de bijlage (opent in nieuw tabblad) van deze noot.
Hierna volgt per uitkomstmaat een beschrijving van de effectiviteit van oefentherapie op het droge versus oefentherapie in het water, en de bewijskracht daarvoor. Zie ook het GRADE-profiel van oefentherapie op het droge versus oefentherapie op het droge.
Gewenste effecten
Cruciale uitkomstmaten
- Uitkomstmaat ‘kwaliteit van leven’ (0 studies):
- Het effect en de bewijskracht van oefentherapie op het droge versus oefentherapie in water op de kwaliteit van leven is onbekend.
- Uitkomstmaat ‘fysiek functioneren’ (2 studies):
- Het effect van oefentherapie op het droge versus oefentherapie in water op fysiek functioneren is onbekend (SMD niet beschikbaar).
- De bewijskracht voor de uitkomstmaat ‘fysiek functioneren’ is met twee niveaus verlaagd tot ‘Lage kwaliteit van bewijs’, gezien tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘vermoeidheid’ (0 studies):
- Het effect en de bewijskracht van oefentherapie op het droge versus oefentherapie in water op de vermoeidheid is onbekend.
- Uitkomstmaat ‘pijn’ (1 studie):
- Het effect en de bewijskracht van oefentherapie op het droge versus oefentherapie in water op de pijn is onbekend (0 studies).
Belangrijke uitkomstmaten
- Uitkomstmaat ‘aerobe capaciteit’ (1 studie):
- Het effect en de bewijskracht van oefentherapie in het water versus oefentherapie op het droge op de aerobe capaciteit is onbekend (SMD niet beschikbaar).
- Uitkomstmaat ‘spierkracht’ (2 studies):
- Het effect en de bewijskracht van oefentherapie in het water versus oefentherapie op het droge op de spierkracht is onbekend (SMD niet beschikbaar).
- Uitkomstmaat ‘range of motion’ (0 studies):
- Het effect en de bewijskracht van oefentherapie in het water versus oefentherapie op het droge op de range of motion is onbekend.
- Uitkomstmaat ‘arbeidsproductiviteit’ (0 studies):
- Het effect en de bewijskracht van oefentherapie in het water versus oefentherapie op het droge op de arbeidsproductiviteit is onbekend.
Ongewenste effecten
- Uitkomstmaat ‘ziekteactiviteit’ (2 studies):
- Het effect en de bewijskracht van oefentherapie in het water versus oefentherapie op het droge op de ziekteactiviteit is onbekend (SMD niet beschikbaar).
- Uitkomstmaat ‘radiologische schade’ (0 studie):
- Het effect en de bewijskracht van oefentherapie in het water versus oefentherapie op het droge op de arbeidsproductiviteit is onbekend.
GRADE-profiel van oefentherapie op het droge versus oefentherapie in het water. [link]
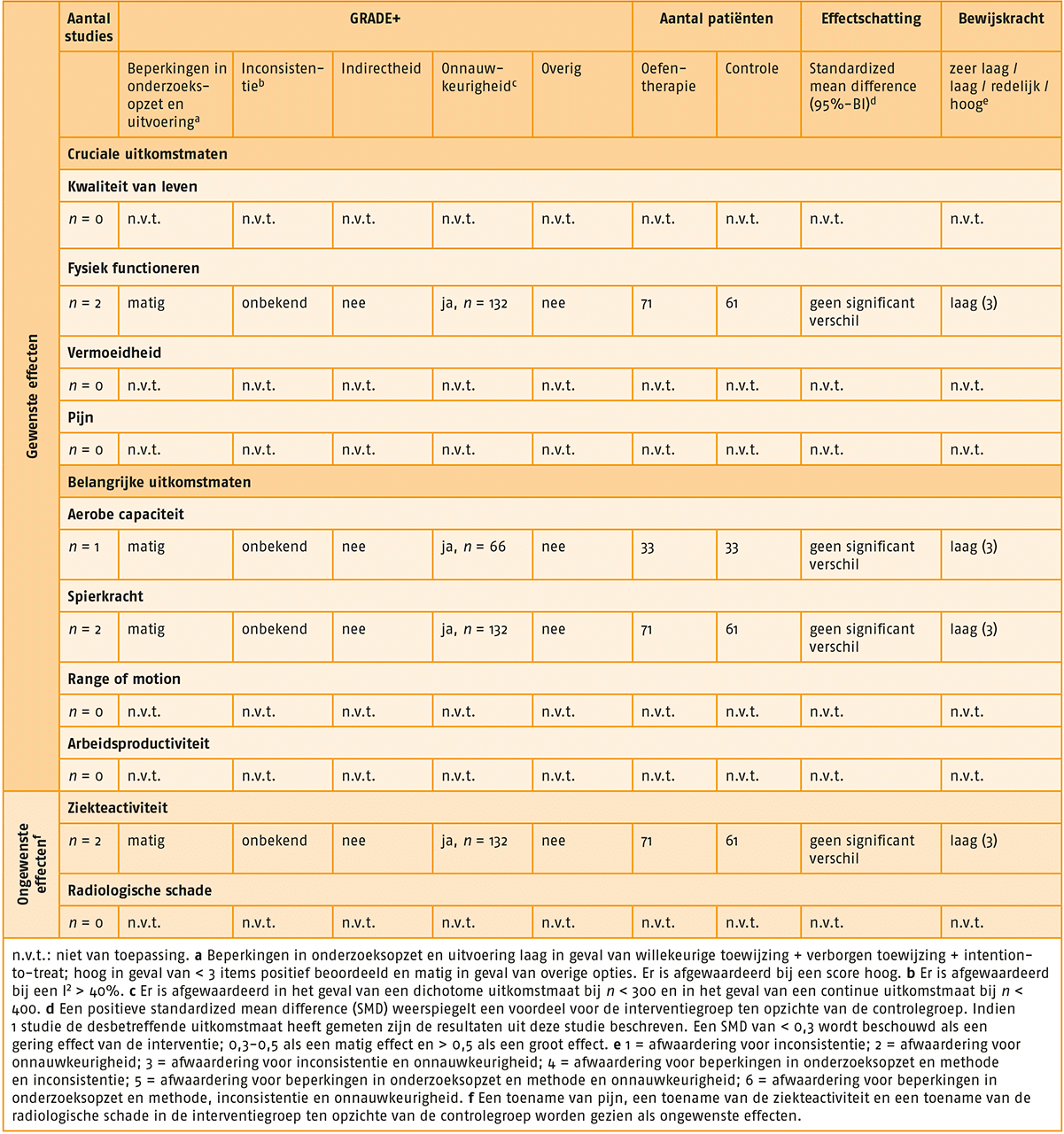
Van bewijs naar aanbeveling
Bij de formulering van de aanbeveling (richting en sterkte) voor oefentherapie bij indicatie 1 zijn aanvullende overwegingen gemaakt.
De gewenste effecten van oefentherapie op het droge versus oefentherapie in het water versus zijn niet aangetoond.
- Of de patiënt de voorkeur geeft aan oefentherapie op het droge of oefentherapie in het water zal waarschijnlijk van patiënt tot patiënt verschillen. De werkgroep schat in dat de meerderheid van de patiënten positief staat tegenover oefentherapie in water.
- De werkgroep schat in dat patiënten met ernstige klachten in de beginfase van de behandeling positief staan tegenover oefentherapie in water.
- De implementatie van oefentherapie in water bij patiënten met ernstige klachten in de beginfase van de behandeling in de dagelijkse praktijk wordt door de werkgroep als aanvaardbaar en haalbaar ingeschat.
1. American College of Sports Medicine. Guidelines for Exercise Testing and Prescription. 10th edition. Lippincott William and Wilkins; 2017.
2. Dogu B, Sirzai H, Yilmaz F, Polat B, Kuran B. Effects of isotonic and isometric hand exercises on pain, hand functions, dexterity and quality of life in women with rheumatoid arthritis. Rheumatol Int. 2013;33(10):2625-30.
3. Cima SR, Barone A, Porto JM, de Abreu DC. Strengthening exercises to improve hand strength and functionality in rheumatoid arthritis with hand deformities: a randomized, controlled trial. Rheumatol Int. 2013;33(3):725-32.
4. Lamb SE, Williamson EM, Heine PJ, Adams J, Dosanjh S, Dritsaki M, et al. Exercises to improve function of the rheumatoid hand (SARAH): a randomised controlled trial. Lancet. 2015;385(9966):421-9.
5. O’Brien AV, Jones P, Mullis R, Mulherin D, Dziedzic K. Conservative hand therapy treatments in rheumatoid arthritis-a randomized controlled trial. Rheumatology (Oxford). 2006;45(5):577-83.
6. Minor MA, Hewett JE, Webel RR, Anderson SK, Kay DR. Efficacy of physical conditioning exercise in patients with rheumatoid arthritis and osteoarthritis. Arthritis and Rheumatism 1989;32(11):1396-405.
7. Siqueira US, Orsini Valente LG, de Mello MT, Szejnfeld VL, Pinheiro MM. Effectiveness of aquatic exercises in women with rheumatoid arthritis: a randomized, controlled, 16-week intervention-the HydRA Trial. Am J Phys Med Rehabil. 2017 Mar;96(3):167-175.
C.3.6 Aanpassing oefentherapie vanwege comorbiditeit
De oefentherapie wordt aangepast indien comorbiditeit het fysiek functioneren belemmert. Voor deze aangepaste oefentherapie zijn, behalve kennis en vaardigheden met betrekking tot RA, ook specifieke kennis en vaardigheden vereist met betrekking tot de comorbiditeit(en) van de individuele patiënt. Hierbij geldt de algemene stelregel ‘onbekwaam is onbevoegd’. Indien de behandelend therapeut onvoldoende kennis en vaardigheden heeft over de aanwezige comorbiditeit wordt de patiënt doorverwezen naar een therapeut die in dit opzicht wel voldoende kennis heeft.
Onderbouwing
Noot 20
Uitgangsvraag
Welke aanpassingen binnen de oefentherapie worden aanbevolen voor patiënten met RA indien er sprake is van een of meer vormen van comorbiditeit die invloed hebben op het fysiek functioneren?
Deze vraag is beantwoord door de aanpassingen binnen de oefentherapie te beschrijven. Hierbij is (wetenschappelijke) literatuur gebruikt.
Voor aanpassing van de oefentherapie in het geval van comorbiditeit die het dagelijks functioneren belemmert, dient de therapeut over voldoende kennis en vaardigheden te beschikken om de patiënt met die comorbiditeit te kunnen behandelen. Is dit niet het geval, dan dient de therapeut de patiënt te verwijzen naar een therapeut die deze kennis en vaardigheden wel heeft. Voor het aanpassen van de oefentherapie dient de therapeut kennis en ervaring te hebben met de i3-S strategie voor het aanpassen van de oefentherapie in geval van de aanwezigheid van comorbiditeit naast de indexziekte.[1] Deze strategie is eerdere toegepast bij het aanpassen van de oefentherapie bij de aanwezigheid van comorbiditeit naast de index ziekte knieartrose [2] en borstkanker.[3]
1. Dekker J, de Rooij M, van der Leeden M. Exercise and comorbidity: the i3-S strategy for developing comorbidity-related adaptations to exercise therapy. Disabil Rehabil. 2016;38(9):905-9.
2. de Rooij M, van der Leeden M, Avezaat E, Häkkinen A, Klaver R, Maas T, et al. Development of comorbidity-adapted exercise protocols for patients with knee osteoarthritis. Clin Interv Aging. 2014 May 14;9:829-42.
3. van der Leeden M, Huijsmans RJ, Geleijn E, de Rooij M, Konings IR, Buffart LM, et al. Tailoring exercise interventions to comorbidities and treatment-induced adverse effects in patients with early stage breast cancer undergoing chemotherapy: a framework to support clinical decisions. Disabil Rehabil. 2018 Feb;40(4):486-96.
C.4 Niet-oefentherapeutische interventies
In de fysio- of oefentherapeutische behandeling van patiënten met RA staan voorlichting en advies, en oefentherapie centraal. De toepassing van andere, niet-oefentherapeutische interventies wordt afgeraden.
Aanbeveling Bied de volgende interventies níet aan bij patiënten met RA:
- laagvermogen lasertherapie;
- elektrostimulatie (waaronder TENS);
- ultrageluid;
- massage;
- thermotherapie;
- medisch tapen;
- dry needling.
Aanbeveling Bied de passieve mobilisatie van gewrichten en spieren bij voorkeur níet aan bij patiënten met RA. Overweeg kortdurende passieve mobilisatie van een aangedaan gewricht ter ondersteuning van oefentherapie uitsluitend bij patiënten zonder actieve ontstekingen om de gewrichtsmobiliteit te vergroten.
NB Passieve mobilisaties zijn gecontra-indiceerd bij cervicale problematiek.
Onderbouwing
Noot 21
Uitgangsvraag
Worden niet-oefentherapeutische interventies, al dan niet in aanvulling op de oefentherapeutische interventie, aanbevolen bij patiënten met RA?
Conclusie vanuit de literatuurstudie
De zoekactie naar literatuur van voldoende methodologische kwaliteit heeft geen literatuur opgeleverd voor de effectiviteit van massage, thermotherapie, medisch tapen, passieve mobilisaties en dry needling. De geïncludeerde literatuur over laagvermogen lasertherapie, elektrostimulatie (waaronder TENS) en ultrageluid bevatte veelal effectschattingen van onbekende omvang (omdat de effectmaat niet was gerapporteerd). De kwaliteit van het beschikbare bewijs was zeer laag.
Van bewijs naar aanbeveling
Op basis van het gebrek aan wetenschappelijke onderbouwing voor niet-oefentherapeutische interventies bij patiënten met RA, het gebrek aan wetenschappelijke onderbouwing voor niet-oefentherapeutische interventies voor andere aandoeningen en de algemene tendens binnen de fysiotherapie gericht op een actieve aanpak is de werkgroep van mening dat laagvermogen-lasertherapie, elektrostimulatie (waaronder TENS), ultrageluid, massage, thermotherapie, medisch tapen en dry needling sterk afgeraden kunnen worden (‘bied bij voorkeur niet aan’). De werkgroep is van mening dat passieve mobilisatie bij voorkeur niet aangeboden dient te worden. Passieve mobilisatie kan worden overwogen, ter ondersteuning van de oefentherapie, uitsluitend als kortdurende interventie ten behoeve van het vergroten van de gewrichtsmobiliteit, bij patiënten zonder actieve ontstekingen.
Aanbeveling voor niet-oefentherapeutische interventies bij patiënten met RA
Bied de volgende interventies níet aan bij patiënten met RA:
- laagvermogen lasertherapie
- elektrostimulatie (waaronder TENS)
- ultrageluid
- massage
- thermotherapie
- medisch tapen
- dry needling
Bied de passieve mobilisatie van gewrichten en spieren bij voorkeur níet aan bij patiënten met RA. Overweeg kortdurende passieve mobilisatie van een aangedaan gewricht ter ondersteuning van oefentherapie uitsluitend bij patiënten zonder actieve ontstekingen om de gewrichtsmobiliteit te vergroten.
NB Passieve mobilisaties zijn gecontra-indiceerd bij cervicale problematiek.
Volledige uitgangsvraag volgens PICO
Welke niet-oefentherapeutische interventies (I), vergeleken met geen oefentherapie (C), worden wel en welke worden niet aanbevolen al dan niet als aanvulling op de oefentherapeutische interventie bij patiënten met RA (P) ter verbetering van de kwaliteit van leven, fysiek functioneren, pijn, vermoeidheid, aerobe capaciteit, spierkracht, range of motion, ziekte activiteit, radiologische schade en arbeidsproductiviteit (O)?
Zoekstrategie
Er is door het KNGF op 3 maart 2017 een zoekactie uitgevoerd naar samenvattingen van de literatuur (i.e. systematische literatuurstudie) en gerandomiseerde gecontroleerde onderzoeken naar niet-oefentherapeutische interventies bij patiënten met RA. De zoektermen voor oefentherapie zijn opgenomen in de bijlage (opent in nieuw tabblad) van deze noot. De selectiecriteria voor inclusie zijn weergegeven in de volgende tabel.
Selectiecriteria systematische literatuurstudie niet-oefentherapeutische interventies.
| Type studie | RCT’s |
|---|---|
| Type patiënt | volwassenen met de diagnose reumatoïde artritis volgens de ARA or ACR/EULAR classificatiecriteria |
| Type interventie | elke vorm van: – passieve mobilisatie – massage – thermotherapie – het toedienen van elektrische stimulatie – het toedienen van elektrische stimulatie middels TENS – het toedienen van elektromagnetische energie – het toedienen van mechanische energie (ultrageluid) – medical taping – dry needling |
| Type vergelijking | geen interventie of usual care |
| Type uitkomst | cruciale uitkomstmaten: kwaliteit van leven, fysiek functioneren, pijn*, vermoeidheid belangrijke uitkomstmaten: aerobe capaciteit, spierkracht, range of motion, ziekteactiviteit*, radiologische schade*, arbeidsproductiviteit |
| Type tijdslijn | direct na de interventie |
De zoekactie van de literatuur leverde 82 referenties op voor laagvermogen lasertherapie, 82 referenties voor ultrageluid, 82 referenties voor elektrische stimulatie, 82 referenties voor transcutaneous electrical nerve stimulation (TENS), 65 referenties voor massage, 179 referenties voor thermotherapie, 38 referenties voor medisch tapen en 100 referenties voor passieve mobilisatie. Na screening van titel en abstract zijn zeven artikelen geïncludeerd voor laagvermogen-lasertherapie [3-5, 7-10], één artikel voor ultrageluid [6], één artikel voor elektrostimulatie [1] en één artikel voor TENS [2]. De flowcharts van de systematische literatuurstudies van de niet-oefentherapeutische interventies zijn op te vragen bij de auteurs van deze richtlijn. Op basis van de selectiecriteria konden er geen artikelen worden geïncludeerd die de effectiviteit van massage, thermotherapie, medisch tapen en passieve mobilisatie onderzochten.
Beschrijving studies
Laagvermogen-lasertherapie
De duur varieerde van drie dagen tot tien weken met een frequentie van twee keer per week tot dagelijks.
Elektrostimulatie
De duur was tien weken, met een frequentie die variërende van 1 uur tot drie uur per dag.
TENS
De studie naar TENS had een duur van in totaal 20 minuten.
Ultrageluid (elektromechanische therapie)
De duur was drie weken met een frequentie van vijf keer per week.
Effectiviteit en bewijskracht
De beoordeling van de onderzoeksopzet en uitvoering van de geselecteerde artikelen is opgenomen in de bijlage (opent in nieuw tabblad) van deze noot.
Hierna volgt per uitkomstmaat een beschrijving van de effectiviteit van niet-oefentherapeutische interventies, en de bewijskracht daarvoor.
Laagvermogen-lasertherapie
Gewenste effecten
Cruciale uitkomstmaten
- Uitkomstmaten ‘kwaliteit van leven’ en ‘vermoeidheid’ (0 studies):
- Het effect en de bewijskracht van laagvermogen-lasertherapie op de kwaliteit van leven en vermoeidheid bij patiënten met RA, vergeleken met geen interventie of de gebruikelijke zorg is onbekend.
- Uitkomstmaat ‘fysiek functioneren’ (3 studies):
- Het effect van laagvermogen-lasertherapie op fysiek functioneren bij patiënten met RA, vergeleken met geen interventie of de gebruikelijke zorg is gering (SMD = 0,20; 95%-BI = -0,14-0,55).
- De bewijskracht voor de uitkomstmaat ‘fysiek functioneren’ is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, gezien beperkingen in de onderzoeksopzet en uitvoering en het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘pijn’ (3 studies):
- Het effect van laagvermogen-lasertherapie op pijn bij patiënten met RA, vergeleken met geen interventie of de gebruikelijke zorg is groot (SMD = 0,92; 95%-BI = -0,74-2,57).
- De bewijskracht voor de uitkomstmaat ‘pijn’ is met drie niveaus verlaagd tot ‘zeer lage kwaliteit van bewijs’, gezien beperkingen in de onderzoeksopzet en uitvoering, tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
Belangrijke uitkomstmaten
- Uitkomstmaat ‘range of motion’ (1 studie):
- Het effect van laagvermogen-lasertherapie op de range of motion bij patiënten met RA, vergeleken met geen interventie of de gebruikelijke zorg is onbekend (SMD niet beschikbaar).
- De bewijskracht voor de uitkomstmaat range of motion is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, gezien tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaten ‘aerobe capaciteit’, ‘spierkracht’ en ‘arbeidsproductiviteit’ (0 studies):
- Het effect en de bewijskracht van laagvermogen-lasertherapie op deze uitkomstmaten is onbekend.
Ongewenste effecten
- Uitkomstmaat ‘ziekteactiviteit’ (4 studies):
- Het effect van laagvermogen-lasertherapie op de ziekteactiviteit bij patiënten met RA, vergeleken met geen interventie of de gebruikelijke zorg is matig (SMD = 0,41; 95%-BI = -0,07-0,88).
- De bewijskracht voor de uitkomstmaat ‘ziekteactiviteit’ is met drie niveaus verlaagd tot ‘zeer lage kwaliteit van bewijs’, gezien beperkingen in de onderzoeksopzet en uitvoering, tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘radiologische schade’ (1 studie):
- Het effect van laagvermogen-lasertherapie op de radiologische schade bij patiënten met RA, vergeleken met geen interventie of de gebruikelijke zorg is onbekend (SMD niet beschikbaar).
- De bewijskracht voor de uitkomstmaat ‘radiologische schade’ is met drie niveaus verlaagd tot ‘zeer lage kwaliteit van bewijs’, gezien beperkingen in de onderzoeksopzet en uitvoering, tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
Het GRADE-profiel van laagvermogen-lasertherapie. staat in de volgende tabel.
GRADE-profiel van laagvermogen-lasertherapie.
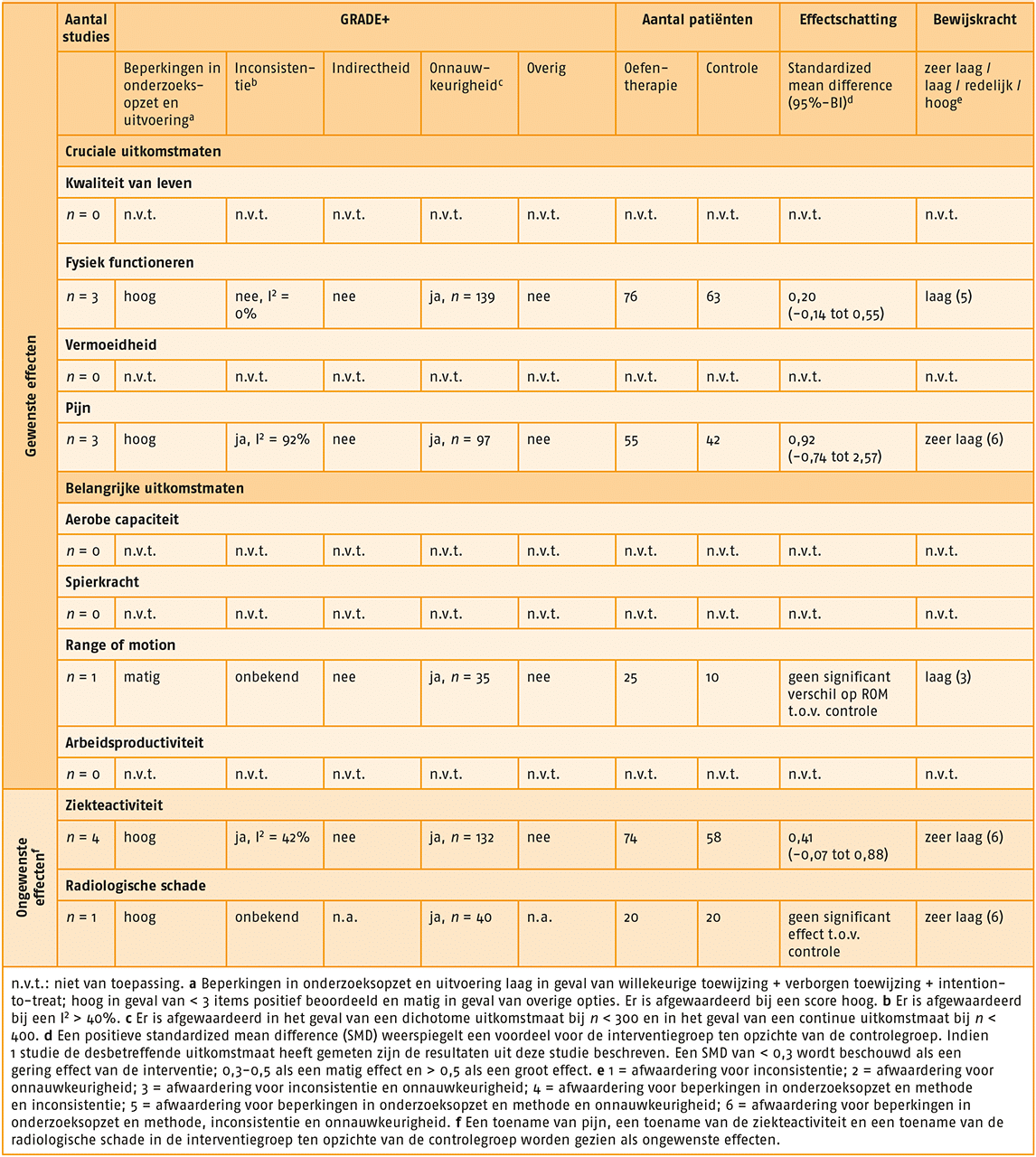
Elektrische stimulatie
Gewenste effecten
Cruciale uitkomstmaten
- Uitkomstmaten ‘kwaliteit van leven’, ‘fysiek functioneren’, ‘vermoeidheid’ en ‘pijn’ (0 studies):
- Het effect en de bewijskracht van elektrostimulatie op ‘kwaliteit van leven’, ‘fysiek functioneren’, ‘vermoeidheid’ en ‘pijn’ bij patiënten met RA is onbekend.
Belangrijke uitkomstmaten
- Uitkomstmaat ‘spierkracht’ (1 studie):
- Het effect van elektrische stimulatie op spierkracht bij patiënten met RA, vergeleken met geen interventie of de gebruikelijke zorg is onbekend (SMD niet beschikbaar).
- De bewijskracht voor de uitkomstmaat ‘spierkracht’ is met drie niveaus verlaagd tot ‘zeer lage kwaliteit van bewijs’, gezien beperkingen in de onderzoeksopzet en uitvoering, tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaten ‘aerobe capaciteit’, ‘range of motion’, ‘arbeidsproductiviteit’, ‘ziekteactiviteit’ en ‘radiologische schade’ (0 studies):
- Het effect en de bewijskracht van elektrische stimulatie op deze uitkomstmaten is onbekend.
Het GRADE-profiel van elektrische stimulatie staat in de volgende tabel.
GRADE-profiel van elektrische stimulatie.
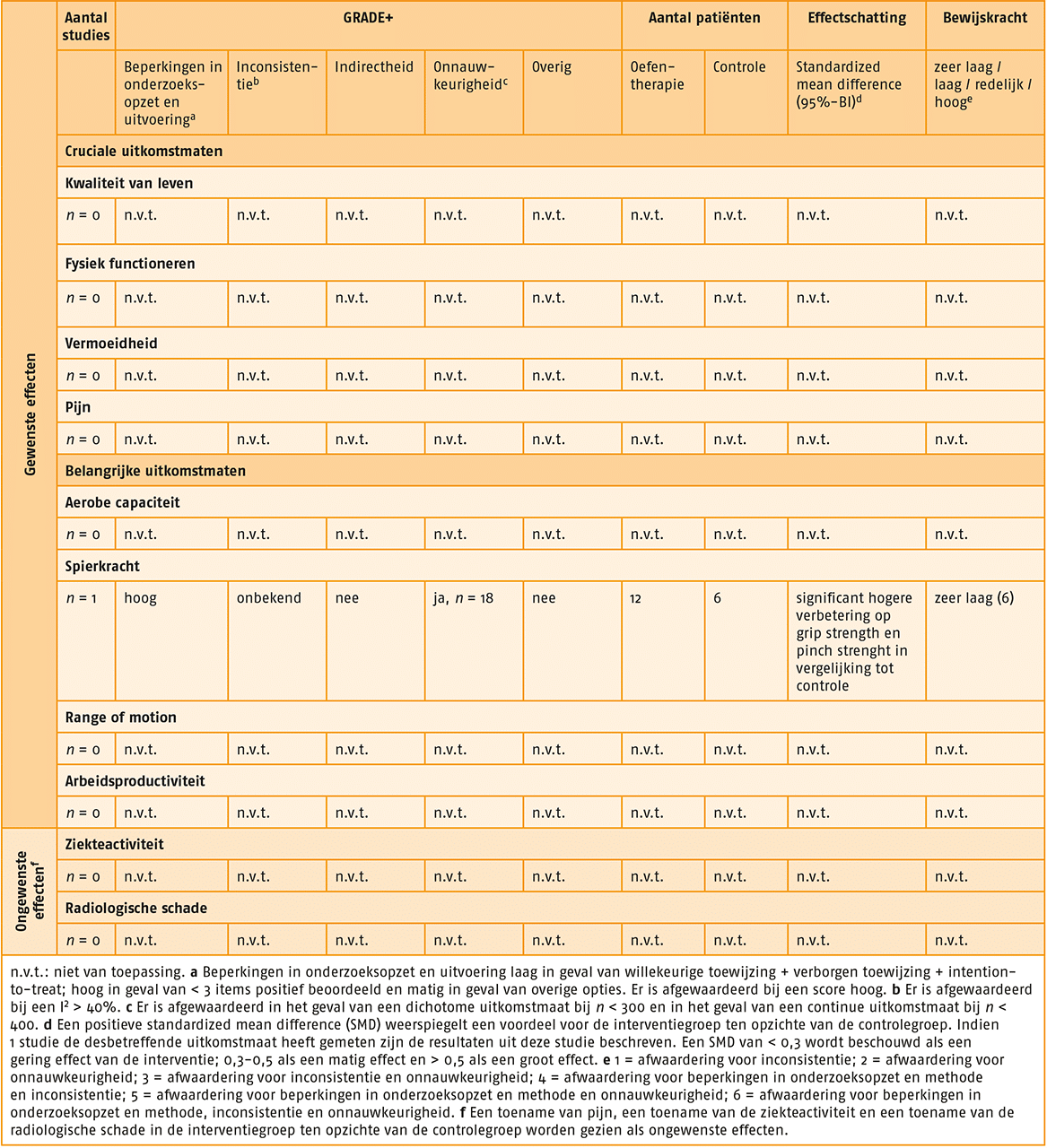
Transcutaneous electrical nerve stimulation (TENS)
Gewenste effecten
Cruciale uitkomstmaten
- Uitkomstmaten ‘kwaliteit van leven’ en ‘fysiek functioneren’ (0 studies):
- Het effect en de bewijskracht van TENS op de uitkomstmaten ‘kwaliteit van leven’ en ‘fysiek functioneren’ bij patiënten met RA is onbekend.
- Uitkomstmaat ‘vermoeidheid’ (1 studie):
- Het effect van TENS op ‘vermoeidheid’ bij patiënten met RA, vergeleken met geen interventie of de gebruikelijke zorg is onbekend (SMD niet beschikbaar).
- De bewijskracht voor de uitkomstmaat ‘vermoeidheid’ is met drie niveaus verlaagd tot ‘zeer lage kwaliteit van bewijs’ gezien beperkingen in de onderzoeksopzet en uitvoering, tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten. (onnauwkeurigheid).
- Uitkomstmaat ‘pijn’ (1 studie):
- Het effect van TENS op pijn bij patiënten met RA, vergeleken met geen interventie of de gebruikelijke zorg is onbekend (SMD niet beschikbaar).
- De bewijskracht voor de uitkomstmaat ‘pijn’ is met drie niveaus verlaagd tot ‘zeer lage kwaliteit van bewijs’, gezien beperkingen in de onderzoeksopzet en uitvoering, tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
Belangrijke uitkomstmaten
- Uitkomstmaten ‘aerobe capaciteit’, ‘spierkracht’, ‘range of motion’, ‘arbeidsproductiviteit’, ‘ziekteactiviteit’ en ‘radiologische schade’ (0 studies):
- Het effect en de bewijskracht van TENS op deze uitkomstmaten is onbekend.
Het GRADE-profiel van TENS staat in de volgende tabel.
GRADE-profiel van TENS.
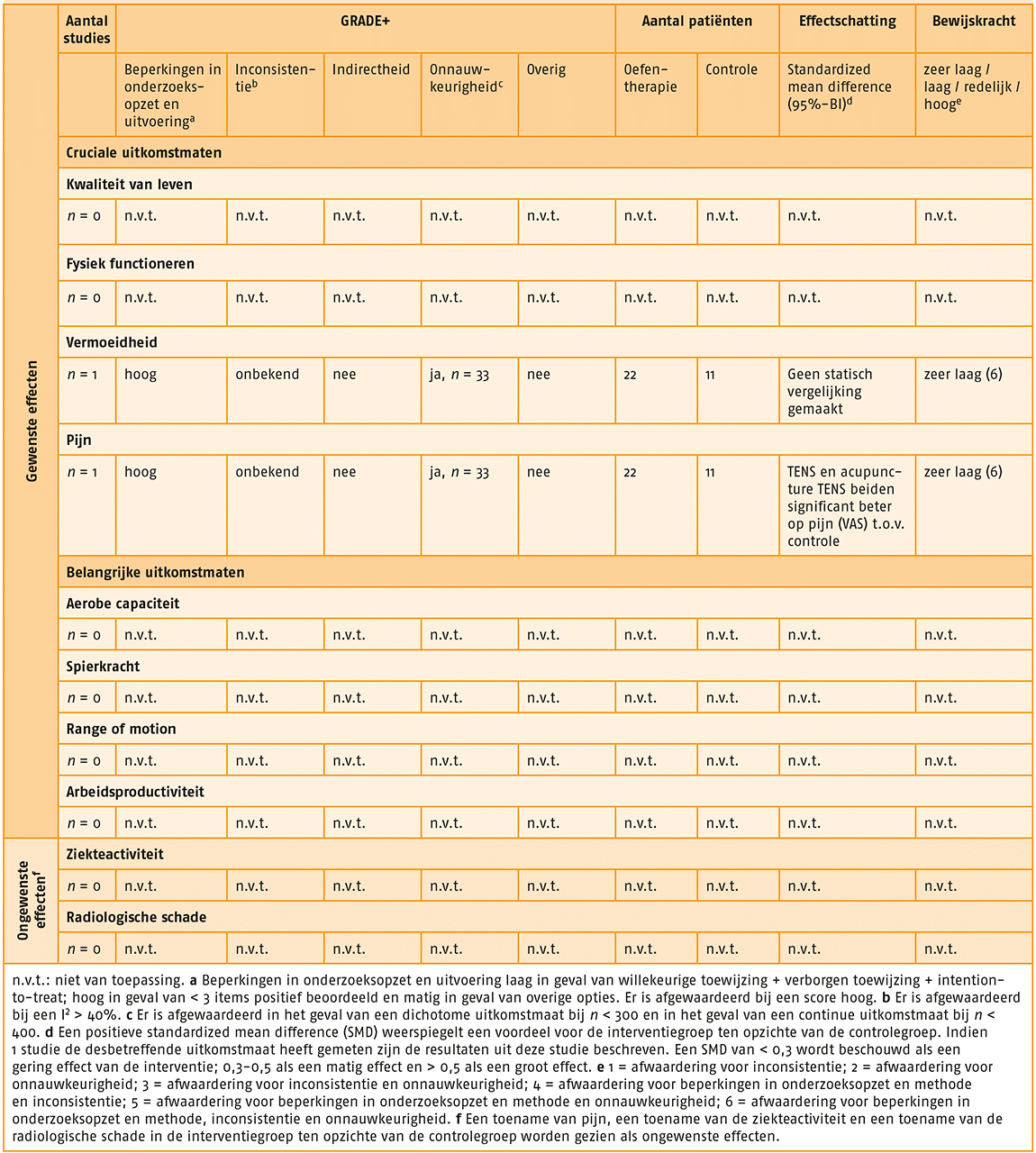
Ultrageluid
Gewenste effecten
Cruciale uitkomstmaten
- Uitkomstmaat ‘kwaliteit van leven’ (0 studies):
- Het effect en de bewijskracht van ultrageluid op de kwaliteit van leven bij patiënten met RA, vergeleken met geen interventie of de gebruikelijke zorg is onbekend.
- Uitkomstmaat ‘fysiek functioneren’ (1 studie):
- Het effect van ultrageluid op het fysiek functioneren bij patiënten met RA, vergeleken met geen interventie of de gebruikelijke zorg is onbekend (SMD niet beschikbaar).
- De bewijskracht voor de uitkomstmaat ‘fysiek functioneren’ is met drie niveaus verlaagd tot ‘zeer lage kwaliteit van bewijs’, gezien beperkingen in de onderzoeksopzet en uitvoering, tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten. (onnauwkeurigheid).
- Uitkomstmaat ‘pijn’ (1 studie):
- Het effect van ultrageluid op de pijn bij patiënten met RA, vergeleken met geen interventie of de gebruikelijke zorg is onbekend (SMD niet beschikbaar).
- De bewijskracht voor de uitkomstmaat ‘pijn’ is met drie niveaus verlaagd tot ‘zeer lage kwaliteit van bewijs’, gezien beperkingen in de onderzoeksopzet en uitvoering, tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
Belangrijke uitkomstmaten
- Uitkomstmaat ‘spierkracht’ (1 studie):
- Het effect van ultrageluid op de spierkracht bij patiënten met RA, vergeleken met geen interventie of de gebruikelijke zorg is onbekend (SMD niet beschikbaar).
- De bewijskracht voor de uitkomstmaat ‘spierkracht’ is met drie niveaus verlaagd tot ‘zeer lage kwaliteit van bewijs’, gezien de beperkingen in de onderzoeksopzet en de uitvoering, tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘range of motion’ (1 studie):
- Het effect van ultrageluid op de range of motion bij patiënten met RA, vergeleken met geen interventie of de gebruikelijke zorg is onbekend (SMD niet beschikbaar).
- De bewijskracht voor de uitkomstmaat ‘range of motion’ is met drie niveaus verlaagd tot ‘zeer lage kwaliteit van bewijs’, gezien de beperkingen in de onderzoeksopzet en de uitvoering, tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaten ‘aerobe capaciteit’, ‘arbeidsproductiviteit’, ‘ziekteactiviteit’ en ‘radiologische schade’ (0 studies):
- Het effect en de bewijskracht van ultrageluid op deze uitkomstmaten is onbekend.
In de volgende tabel staat het GRADE-profiel van mechanische eniergie (ultrageluid).
GRADE-profiel van elektromechanische energie (ultrageluid).
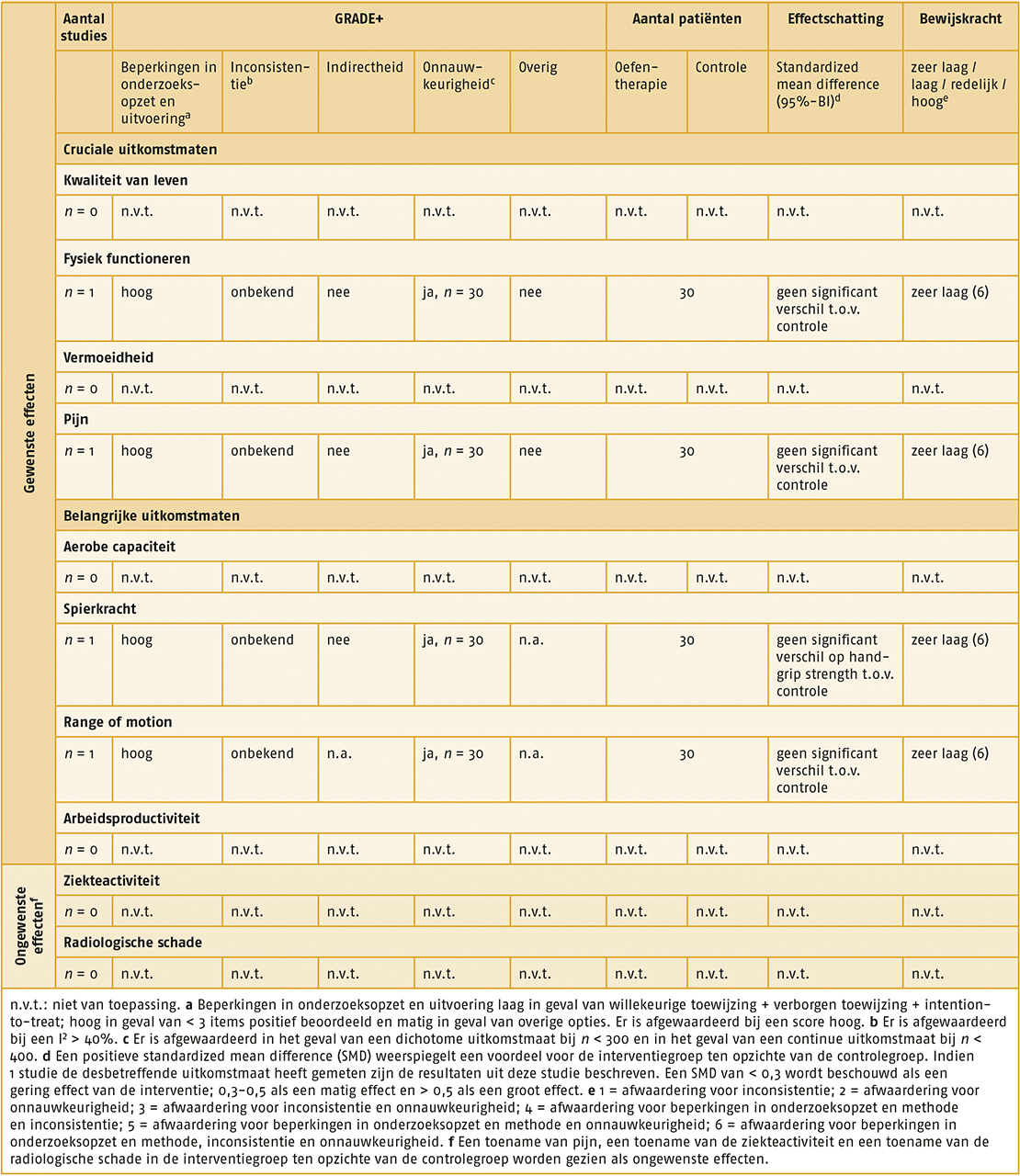
Van bewijs naar aanbeveling
Bij de formulering van de richting en sterkte van de aanbeveling voor niet-oefentherapeutische interventies heeft de werkgroep de volgende aanvullende overwegingen gemaakt. Zie ook het beoordelingsformulier van bewijs naar aanbeveling voor niet-oefentherapeutische interventies in de bijlage (opent in nieuw tabblad) van deze noot.
- Op basis van het gebrek aan wetenschappelijke literatuur en de lage bewijskracht en lage kwaliteit van het beschikbare bewijs wordt door de werkgroep vastgesteld dat de gewenste en de (mogelijke) ongewenste effecten gelijk zijn. Wel is de werkgroep van mening dat passieve mobilisatie overwogen kan worden ter ondersteuning van de oefentherapie, uitsluitend als kortdurende interventie om de gewrichtsmobiliteit te vergroten bij patiënten zonder actieve ontstekingen.
- Welke waarde patiënten hechten aan niet-oefentherapeutische interventies en naar welke niet-oefentherapeutische interventie hun voorkeur uitgaat, zal van patiënt tot patiënt verschillen. De werkgroep schat in dat de meerderheid van de patiënten niet positief staat tegenover niet-oefentherapeutische interventies, vanwege het gebrek aan effectiviteit ervan .
- De kosten van de niet-oefentherapeutische interventies voor de patiënt zijn afhankelijk van de vigerende overheidsbepalingen ten aanzien van ziektekosten (zie Rijksoverheid.nl), In een aantal gevallen zijn er voor de fysiotherapeut kosten verbonden aan de toepassing van niet-oefentherapeutische interventies, doordat materiaal en/of apparatuur moet worden aangeschaft en er omdat er scholing nodig kan zijn.
- Er zijn geen studies beschikbaar naar de kosteneffectiviteit van de niet-oefentherapeutische interventies.
- De implementatie van de niet-oefentherapeutische interventies in de dagelijkse praktijk wordt door de werkgroep als onaanvaardbaar en onhaalbaar ingeschat, omdat de interventies niet als meest aangewezen behandeloptie worden beschouwd en er mogelijk specifieke middelen voor vereist zijn.
1. Oldham JA, Stanley JK. Rehabilitation of atrophied muscle in the rheumatoid arthritic hand: a comparison of two methods of electrical stimulation. J Hand Surg Br. 1989;14(3):294-7.
2. Langley GB, Sheppeard H, Johnson M, Wigley RD. The analgesic effects of transcutaneous electrical nerve stimulation and placebo in chronic pain patients. A double-blind non-crossover comparison. Rheumatol Int. 1984;4(3):119-23.
3. Bliddal H, Hellesen C, Ditlevsen P, Asselberghs J, Lyager L. Soft-laser therapy of rheumatoid arthritis. Scand J Rheumatol. 1987;16(4):225-8.
4. Goats GC, Flett E, Hunter JA, Stirling A. Low Intensity Laser and Phototherapy for Rheumatoid Arthritis. Physiotherapy, May 1996, vol82, no 5.
5. Hall J, Clarke AK, Elvins DM, Ring EF. Low level laser therapy is ineffective in the management of rheumatoid arthritic finger joints. Br J Rheumatol. 1994;33(2):142-7.
6. Hawkes J, Care G, Dixon JS, Bird HA, Wright VA. Comparison of three different treatments for rheumatoid arthritis of the hands. Physiotherapy Practice 2 1986;2: 155-60,
7. Johannsen F, Hauschild B, Remvig L, Johnsen V, Petersen M, Bieler T. Low energy laser therapy in rheumatoid arthritis. Scand J Rheumatol. 1994;23(3):145-7.
8. Meireles SM, Jones A, Natour J. Low-level laser therapy on hands of patients with rheumatoid arthritis. Clin Rheumatol. 2011;30(1):147-8.
9. Palmgren N, Jensen GF, Kaae K, Windelin M, Colov HC. Low-power laser therapy in rheumatoid arthritis. Lasers Med Sci. 1989 Sep;4(3):193-6.
10. Walker JW, Somlyo AV, Goldman YE, Somlyo AP, Trentham DR. Kinetics of smooth and skeletal muscle activation by laser pulse photolysis of caged inositol 1,4,5-trisphosphate. Nature. 1987;327(6119):249-52.
C.5 Gedragsmatige interventies ter bevordering van lichamelijke activiteit
Aanbeveling Bied bij patiënten die onvoldoende lichamelijk actief zijn gedragsmatige interventies aan ter bevordering van de mate van lichamelijke activiteit.
Toevoeging Houd bij het bevorderen van lichamelijke activiteit rekening met de volgende principes van gedragsverandering:
- Houd rekening met de fase van gedragsverandering waarin de patiënt zich bevindt.
- Formuleer haalbare doelen in samenspraak met de patiënt.
- Geef de instructies zodanig dat de patiënt deze begrijpt en weet wat hij moet of kan doen.
- Zorg voor voldoende variatie tijdens de oefensessies.
- Integreer individuele oefeningen en lichamelijke activiteiten in het dagelijks leven en leer de patiënt de individuele oefeningen en lichamelijke activiteiten te integreren in het dagelijks leven om de effectiviteit van de oefentherapie te vergroten.
- Zorg dat de patiënt onafhankelijk wordt van de therapeutische ondersteuning.
- Help de patiënt terugval in het oude (inactieve) beweeggedrag te voorkomen.
- Informeer de patiënt over vorderingen en leer de patiënt zijn vorderingen ook zelf te monitoren.
- Betrek de omgeving van de patiënt (partner, kinderen, vrienden etc.) bij de behandeling ter ondersteuning van de veranderingen in het beweeggedrag van de patiënt.
- Moedig bij de patiënt het vertrouwen in eigen kunnen aan.
- Evalueer met de patiënt wat effectief is en wat niet effectief is.
- Help de patiënt om eigen doelen te blijven nastreven.
- Leer de patiënt omgaan met negatieve emoties en stress die het behalen van gestelde doelen kunnen belemmeren.
Onderbouwing
Noot 22
Uitgangsvraag
Worden (gedragsmatige) interventies ter bevordering van de mate van lichaamsbeweging met supervisie van een fysio- of oefentherapeut aanbevolen bij patiënten met RA?
Conclusie vanuit de literatuurstudie
De literatuur toont een groot effect van gedragsmatige interventies ter bevordering van lichamelijke activiteit op de mate van lichaamsbeweging (van matige tot hoge intensiteit) vergeleken met geen interventie of de gebruikelijke zorg, met een hoge kwaliteit van bewijs. Tevens toont de literatuur een groot effect van gedragsmatige interventies ter bevordering van lichamelijke activiteit op de mate van lichaamsbeweging (van lage intensiteit) vergeleken met geen interventie of de gebruikelijke zorg, met een redelijke kwaliteit van bewijs. Het effect van gedragsmatige interventies ter bevordering van lichamelijke activiteit op de mate van sedentair gedrag, vergeleken met geen interventie of de gebruikelijke zorg, is onbekend.
Van bewijs naar aanbeveling
Op basis van de gewenste effecten van gedragsmatige interventies ter bevordering van de mate van lichamelijke activiteit, de waarschijnlijkheid op kosteneffectiviteit en de hoge aanvaardbaarheid en haalbaarheid is de werkgroep van mening dat gedragsmatige interventies ter bevordering van de mate van lichamelijke activiteit sterk aanbevolen kunnen worden bij patiënten die onvoldoende lichamelijk actief zijn (‘bied gedragsmatige interventies ter bevordering van de mate van lichamelijke activiteit aan’).
Aanbeveling
Bied bij patiënten die onvoldoende lichamelijk actief zijn gedragsmatige interventies aan ter bevordering van de mate van lichamelijke activiteit.
Complete uitgangsvraag volgens PICO
Worden (gedragsmatige) interventies ter bevordering van de mate van lichaamsbeweging met
supervisie van een fysiotherapeut (I) vergeleken met geen interventie (C) aanbevolen bij patiënten met RA (P) ter verbetering van de mate van lichaamsbeweging (hoge tot matige intensiteit en lage intensiteit), en sedentair gedrag (O)?
Zoekstrategie
Er is door het KNGF op 3 maart 2017 een zoekactie uitgevoerd naar samenvatting van de literatuur (i.e. systematische literatuurstudie) en gerandomiseerde gecontroleerde onderzoeken naar het promoten van lichaamsbeweging door fysiotherapeuten bij patiënten met RA. De zoektermen voor oefentherapie zijn opgenomen in de bijlage van deze noot. De selectiecriteria voor inclusie zijn weergegeven in de volgende tabel.
Selectiecriteria systematische literatuurstudie gedragsmatige interventies ter bevordering van lichamelijke activiteit.
| Type studie | RCT’s |
|---|---|
| Type patiënt | volwassenen met de diagnose reumatoïde artritis volgens de ARA or ACR/EULAR classificatiecriteria |
| Type interventie | promotie van lichaamsbeweging (elke vorm van beweging) door een fysiotherapeut |
| Type vergelijking | geen interventie of usual care |
| Type uitkomst | cruciale uitkomstmaten: kwaliteit van leven, fysiek functioneren, pijn*, vermoeidheid belangrijke uitkomstmaten: aerobe capaciteit, spierkracht, range of motion, ziekteactiviteit*, radiologische schade*, arbeidsproductiviteit |
| Type tijdslijn | langetermijn-follow-up |
Gevonden literatuur
De zoekactie van de literatuur leverde 1837 referenties op. Hierin werd één systematische review [1] geïdentificeerd waarin vijf gerandomiseerde gecontroleerde onderzoeken waren geïncludeerd. Deze systematische review behaalde 6 van de 11 punten op de AMSTAR checklist. Gezien de lage kwaliteit van deze review is besloten de zoekactie opnieuw te doen. In totaal werken 24 potentiële studies gevonden waarvan uiteindelijk zes gerandomiseerde gecontroleerde onderzoeken voldeden aan onze inclusiecriteria.
De flowchart van de systematische literatuurstudie(s) naar gedragsmatige interventies ter bevordering van lichamelijke activiteit is opgenomen in de bijlage (opent in nieuw tabblad) van deze noot.[2-7]
Beschrijving studies
De duur van de interventies varieerde van vijf weken tot 12 maanden waarbij er vier studies een relatief kort programma hadden (5 tot 16 weken) en twee studies een lang programma (1 jaar). In twee studies werd motivational interviewing toegepast gecombineerd met telefonische of SMS-reminders. In drie studies werd gepersonaliseerde coaching toegepast waarvan in studie via een online platform. In één studie werden educatieve groepssessie georganiseerd.
Alle studies waren gericht op gedragsverandering waarbij de volgende principes werden gehanteerd:
- Houd rekening met de fase van gedragsverandering waarin de patiënt zich bevindt.
- Formuleer haalbare doelen in samenspraak met de patiënt.
- Zorg voor goede instructies waarbij de patiënt weet en begrijp wat hij of zij moet doen of kan doen.
- Zorg voor voldoende variatie tijdens de oefensessies.
- Integreer individuele oefeningen en lichamelijke activiteiten in het dagelijks leven.
- Zorg dat de patiënt onafhankelijk wordt van de fysiotherapeutische ondersteuning.
- Help voorkomen dat de patiënt terugvalt in het oude (inactieve) beweeggedrag.
- Informeer de patiënt over vorderingen en leer de patiënt dit ook zelf te monitoren.
- Betrek de omgeving van de patiënt (partner, kinderen, vrienden etc.) bij de ondersteuning van de beweeggedragsverandering door de patiënt.
- Moedig bij de patiënt het geloof in eigen kunnen aan.
- Evalueer met de patiënt wat er wel en niet goed is gegaan.
- Help de patiënt om goed te blijven focussen op eigen doelen en zich niet af te laten leiden door anderen.
- Leer de patiënt omgaan met negatieve emoties en stress die belemmerend kunnen werken bij het behalen van de gestelde doelen.
- Leer de patiënt dat integratie van individuele oefeningen en/of lichamelijke activiteiten in het dagelijks leven een goede manier is om gedragsverandering te blijven volhouden.
Effectiviteit en bewijskracht
De beoordeling van de onderzoeksopzet en uitvoering van de geselecteerde artikelen is opgenomen in de bijlage (opent in nieuw tabblad) van deze noot.
Hierna volgt per uitkomstmaat een beschrijving van de effectiviteit van gedragsmatige interventies ter bevordering van lichamelijke activiteit, en de bewijskracht daarvoor.
Zie ook het GRADE-profiel van gedragsmatige interventies ter bevordering van lichamelijke activiteit.
Gewenste effecten
Cruciale uitk omstmaten
- Uitkomstmaat ‘mate van lichaamsbeweging van matige tot hoge intensiteit’ (4 studies):
- Er bestaat een verhoogde waarschijnlijkheid dat gedragsmatige interventies ter bevordering van lichamelijke activiteit leiden tot een hogere mate van lichaamsbeweging van matige tot hoge intensiteit, vergeleken met geen interventie (odds ratio = 1,90; 95%-BI = 1,19-3,05).
- De bewijskracht voor de uitkomstmaat ‘mate van lichaamsbeweging van matige tot hoge intensiteit’ is hoog; er heeft geen afwaardering plaatsgevonden.
- Uitkomstmaat ‘mate van lichaamsbeweging van lage intensiteit’ (3 studies):
- Er bestaat een groot effect (SMD = 0,57; 95%-BI = 0,23-0,91) van gedragsmatige interventies op de mate van lichaamsbeweging van lage intensiteit.
- De bewijskracht voor de uitkomstmaat ‘mate van lichaamsbeweging van lage intensiteit’ is met één niveau verlaagd tot ‘redelijke kwaliteit van bewijs’, gezien het geringe aantal patiënten (onnauwkeurigheid).
- Uitkomstmaat ‘sedentair gedrag’ (1 studie):
- Het effect van gedragsmatige interventies op sedentair gedrag is onbekend (SMD niet beschikbaar).
- De bewijskracht voor de uitkomstmaat ‘sedentair gedrag’ is met twee niveaus verlaagd tot ‘lage kwaliteit van bewijs’, gezien tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (onnauwkeurigheid).
GRADE-profiel van gedragsmatige interventies ter bevordering van lichamelijke activiteit. [link]
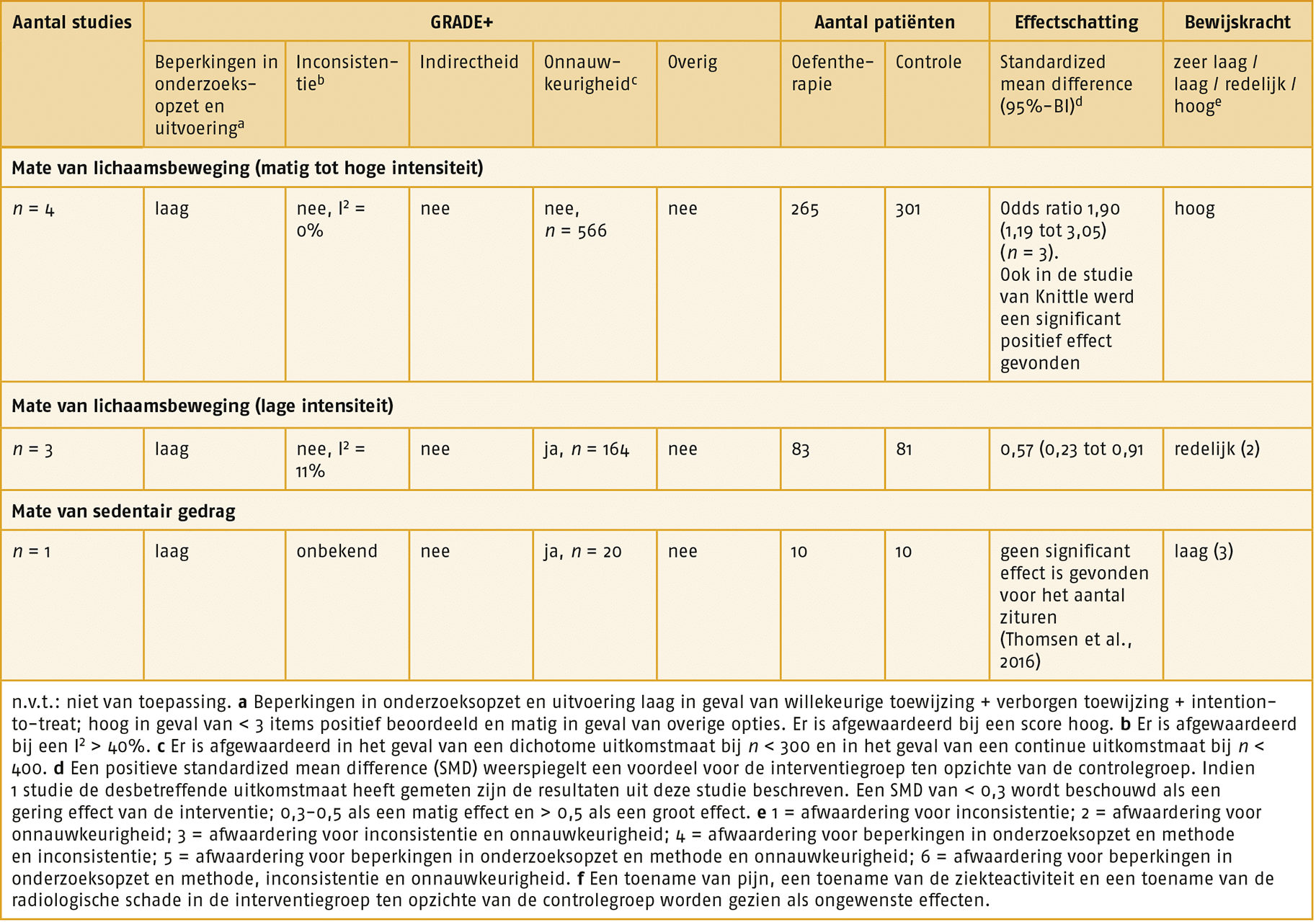
Van bewijs naar aanbeveling
Bij de formulering van de richting en de sterkte van de aanbeveling voor gedragsmatige interventies ter bevordering van lichamelijke activiteit heeft de werkgroep de volgende aanvullende overwegingen gemaakt. Zie ook het beoordelingsformulier van bewijs naar aanbeveling voor gedragsmatige interventies ter bevordering van lichamelijke activiteit in de bijlage (opent in nieuw tabblad) bij deze noot.
- De gewenste effecten (verbetering van de mate van lichaamsbeweging en sedentair gedrag) van een gedragsmatige interventie ter bevordering van de mate van lichamelijke activiteit zijn aanwezig. Er zijn geen ongewenste effecten gemeten.
- Welke waarde patiënten hechten aan gedragsmatige interventies ter bevordering van de lichamelijke activiteit, en naar welke interventie hun voorkeur uitgaat, zal waarschijnlijk van patiënt tot patiënt verschillen.
- De werkgroep schat in dat de meerderheid van de patiënten er positief tegenover staat, vanwege de gunstige effecten ervan.
- De kosten voor de patiënt zijn afhankelijk van de vigerende overheidsbepalingen ten aanzien van ziektekosten (zie Rijksoverheid.nl). De kosten van gedragsmatige interventies ter bevordering van de lichamelijke activiteit voor de fysiotherapeut en de patiënt zijn onbekend, maar de werkgroep schat in dat deze kosten niet substantieel zijn.
- Een interventie (van 12 maanden) ter bevordering van de lichaamsbeweging blijkt wel kosteneffectief te zijn vanuit het perspectief van de patiënt, maar niet vanuit sociaal-maatschappelijk perspectief, uitgezonderd als patiënten veel beperkingen in activiteiten hebben.[8]
- De implementatie van de interventie in de dagelijkse praktijk wordt door de werkgroep als aanvaardbaar en haalbaar ingeschat, omdat de interventie als meest aangewezen behandeloptie wordt beschouwd en er geen specifieke middelen voor vereist zijn.
1. Larkin L, Gallagher S, Cramp F, Brand C, Fraser A, Kennedy N. Behaviour change interventions to promote physical activity in rheumatoid arthritis: a systematic review. Rheumatol Int. 2015;35(10):1631-40.
2. Brodin N, Eurenius E, Jensen I, Nisell R, Opava CH. Coaching patients with early rheumatoid arthritis to healthy physical activity: a multicenter, randomized, controlled study. Arthritis Rheum. 2008;59(3):325-31.
3. Feldthusen C, Dean E, Forsblad-d’Elia H, Mannerkorpi K. Effects of person-centered physical therapy on fatigue-related variables in persons with rheumatoid arthritis: a randomized controlled trial. Arch Phys Med Rehabil. 2016 Jan;97(1):26-36.
4. Knittle K, de Gucht V, Hurkmans E, Peeters A, Ronday K, Maes S, et al. Targeting motivation and self-regulation to increase physical activity among patients with rheumatoid arthritis: a randomised controlled trial. Clin Rheumatol. 2015;34(2):231-8.
5. Mayoux-Benhamou A, Giraudet-Le Quintrec JS, Ravaud P, Champion K, Dernis E, Zerkak D, Roy C, Kahan A, Revel M, Dougados M. Influence of patient education on exercise compliance in rheumatoid arthritis: a prospective 12-month randomized controlled trial. J Rheumatol. 2008 Feb;35(2):216-23.
6. Thomsen T, Aadahl M, Beyer N, Hetland ML, Loppenthin K, Midtgaard J, et al. Motivational counselling and SMS-reminders for reduction of daily sitting time in patients with rheumatoid arthritis: a descriptive randomised controlled feasibility study. BMC Musculoskelet Disord. 2016;17(1):434.
7. van den Berg MH, Ronday HK, Peeters AJ, le Cessie S, van der Giesen FJ, Breedveld FC, et al. Using internet technology to deliver a home-based physical activity intervention for patients with rheumatoid arthritis: a randomized controlled trial. Arthritis Rheum. 2006 Dec 15;55(6):935-45.
8. Brodin N, Lohela-Karlsson M, Swardh E, Opava CH. Cost-effectiveness of a one-year coaching program for healthy physical activity in early rheumatoid arthritis. Disabil Rehabil. 2015;37(9):757-62.
C.6 Afsluiting van de behandeling
De behandeling wordt afgesloten wanneer:
- de hulpvraag is beantwoord en de behandeldoelen zijn bereikt, en/of
- er bij tussenevaluaties geen of onvoldoende therapeutisch effect is bereikt en/of
- er sprake is van contra-indicaties voor oefentherapie en/of
- de therapietrouw onvoldoende is, ondanks diverse pogingen om deze te verbeteren.
De therapeut adviseert de patiënt over het in stand houden van behaalde doelstellingen. Daarbij kan de therapeut de patiënt onder andere informatie en advies geven over het handhaven van adequaat beweeggedrag in het dagelijks leven.
De afsluiting vindt plaats volgens de vigerende richtlijnen van het KNGF (opent in nieuw tabblad) en de VvOCM (opent in nieuw tabblad) over dossiervoering respectievelijk verslaglegging (opent in nieuw tabblad).

