Diagnostisch proces
Inleiding
Tijdens het eerste consult inventariseert de fysiotherapeut de reden van verwijzing en bepaalt hij of de patiënt in aanmerking komt voor fysiotherapeutische behandeling op basis van de anamnese en het lichamelijk onderzoek. Uitgangspunt is de hulpvraag van de patiënt, inclusief de belangrijkste klachten van de patiënt. Met behulp van vier screeningsvragen bepaalt de fysiotherapeut de uiteindelijke indicatie voor behandeling (zie paragraaf B.5).
Voor meer informatie over samen beslissen, zie module ‘A.8 Samen beslissen (opent in nieuw tabblad)‘ en module ‘C.8 De keuze voor de behandeling (opent in nieuw tabblad)‘.
Met behulp van de verwijsgegevens, de anamnese en het lichamelijk onderzoek gaat de fysiotherapeut na of er een indicatie bestaat voor fysiotherapie. Uitgangspunt is de hulpvraag van de patiënt, inclusief de belangrijkste klachten. De fysiotherapeut onderzoekt welke stoornissen in functie, beperkingen in activiteiten en participatieproblemen bij de patiënt op de voorgrond staan, wat de prognose van de aandoening is, mede in het licht van relevante comorbiditeiten, en wat de informatiebehoefte is van de patiënt. Op basis van bovenstaande wordt bepaald of de patiënt in aanmerking komt voor fysiotherapeutische behandeling.
B.1 Anamnese
Op basis van de anamnese tracht de fysiotherapeut inzicht te krijgen in:
- de hulpvraag van de patiënt;
- de aanwezigheid, aard en ernst van de klachten en de bevorderende en belemmerende factoren voor herstel ten aanzien van het gezondheidsprobleem van de patiënt;
- het vroegere en huidige functioneren (= bewegingsgedrag) van de patiënt in het algemeen dagelijks leven (ADL) en werkgerelateerd (met behulp van de Walking Impairment Questionnaire [WIQ]);
- welke kennis en inzichten de patiënt heeft over zijn aandoening;
- de behoefte aan informatie/voorlichting (met behulp van de Vragenlijst Informatiebehoefte [bijlage 2]);
- de aanwezigheid van relevante risicofactoren of comorbiditeiten (met behulp van de Cumulative Illness Rating Scale [CIRS]);
- de aanwezigheid van rode en/of gele vlaggen (screening ‘pluis/niet-pluis’);
- de kwaliteit van leven van de patiënt (met behulp van de EuroQol 5D [EQ-5D]);
- de motivatie van de patiënt;
- de wenselijkheid om, in overleg met de patiënt, de partner/mantelzorger te betrekken bij de voorlichting en het opstellen van het behandelplan.
De fysiotherapeut stelt tevens vast of er mogelijk andere aandoeningen zijn die een grotere behandelprioriteit hebben dan sPAV, doordat deze aandoeningen een grotere beperking opleveren voor de patiënt dan sPAV.
Indien er sprake is van een of meerdere rode vlaggen informeert de fysiotherapeut de patiënt over deze bevindingen. De fysiotherapeut brengt ook de verwijzer hiervan op de hoogte, na overleg met de patiënt. De fysiotherapeut adviseert de patiënt om contact op te nemen met de huisarts of behandelend specialist.
Meetinstrumenten
De meetinstrumenten die van toepassing kunnen zijn bij patiënten met SPAV zijn op systematische wijze gekoppeld aan de gezondheidsdomeinen van de ICF. In figuur 1 staat een overzicht van de
aanbevolen meetinstrumenten.
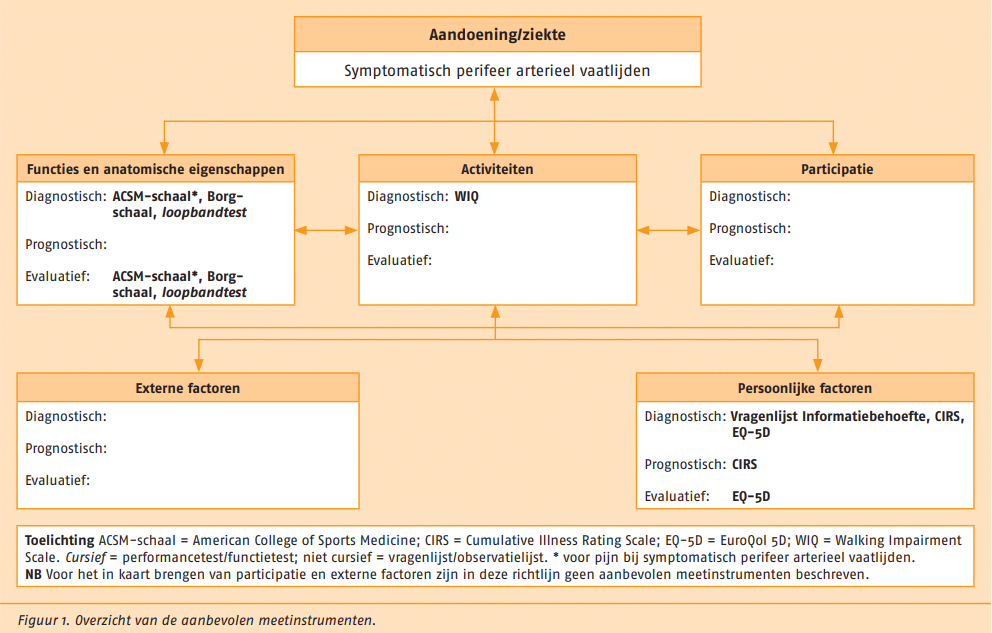
Deze instrumenten kunnen worden toegepast wanneer daar in de praktijk aanleiding toe is. De optionele meetinstrumenten staan in de Verantwoording en toelichting. Al deze meetinstrumenten zijn beschikbaar via www.meetinstrumentenzorg.nl (opent in nieuw tabblad).
Op basis van de anamnese tracht de fysiotherapeut inzicht te krijgen in:
- de hulpvraag van de patiënt;
- de aanwezigheid, aard en ernst van de klachten en de bevorderende en belemmerende factoren voor herstel ten aanzien van het gezondheidsprobleem van de patiënt;
- het vroegere en huidige functioneren (= bewegingsgedrag) van de patiënt in het algemeen dagelijks leven (ADL) en werkgerelateerd (met behulp van de Walking Impairment Questionnaire [WIQ]);
- welke kennis en welk inzicht de patiënt heeft over zijn aandoening;
- de behoefte aan informatie/voorlichting (met behulp van de Vragenlijst Informatiebehoefte);
- de aanwezigheid van relevante risicofactoren of comorbiditeiten (met behulp van de Cumulative Illness Rating Scale [CIRS]);
- de aanwezigheid van rode en/of gele vlaggen (screening ‘pluis/niet-pluis’44);
- de kwaliteit van leven van de patiënt (met behulp van de EuroQol 5D [EQ-5D]);
- de motivatie van de patiënt;
- de wenselijkheid om, in overleg met de patiënt, de partner/mantelzorger te betrekken bij de voorlichting en het opstellen van het behandelplan.
De fysiotherapeut stelt tevens vast of er mogelijk andere aandoeningen zijn die een grotere behandelprioriteit hebben dan sPAV, doordat deze aandoeningen een grotere beperking opleveren voor de patiënt dan sPAV.
Indien er sprake is van een of meerdere rode vlaggen informeert de fysiotherapeut de patiënt over deze bevindingen. De fysiotherapeut brengt ook de verwijzer hiervan op de hoogte, na overleg met de patiënt. De fysiotherapeut adviseert de patiënt om contact op te nemen met de huisarts of behandelend specialist.
Meetinstrumenten
De meetinstrumenten die van toepassing kunnen zijn bij patiënten
met SPAV zijn op systematische wijze gekoppeld aan de gezondheidsdomeinen van de ICF. In figuur 1a staan de aanbevolen meetinstrumenten, in figuur 1b de optionele meetinstrumenten.
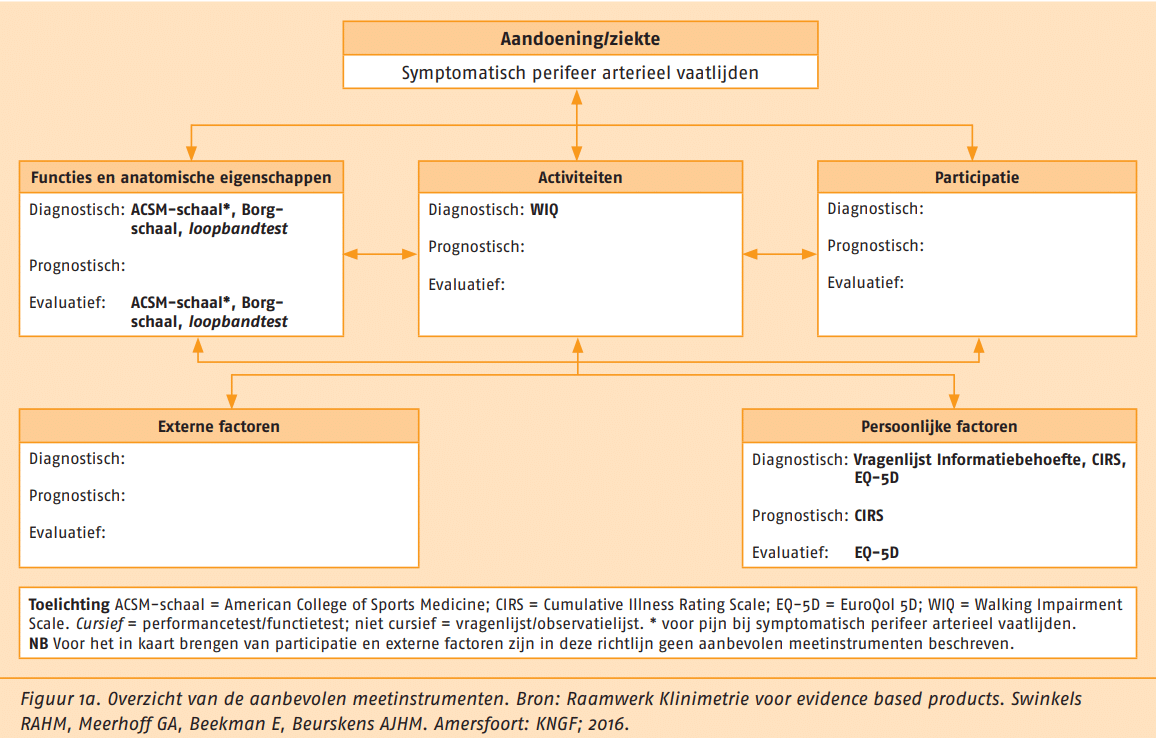
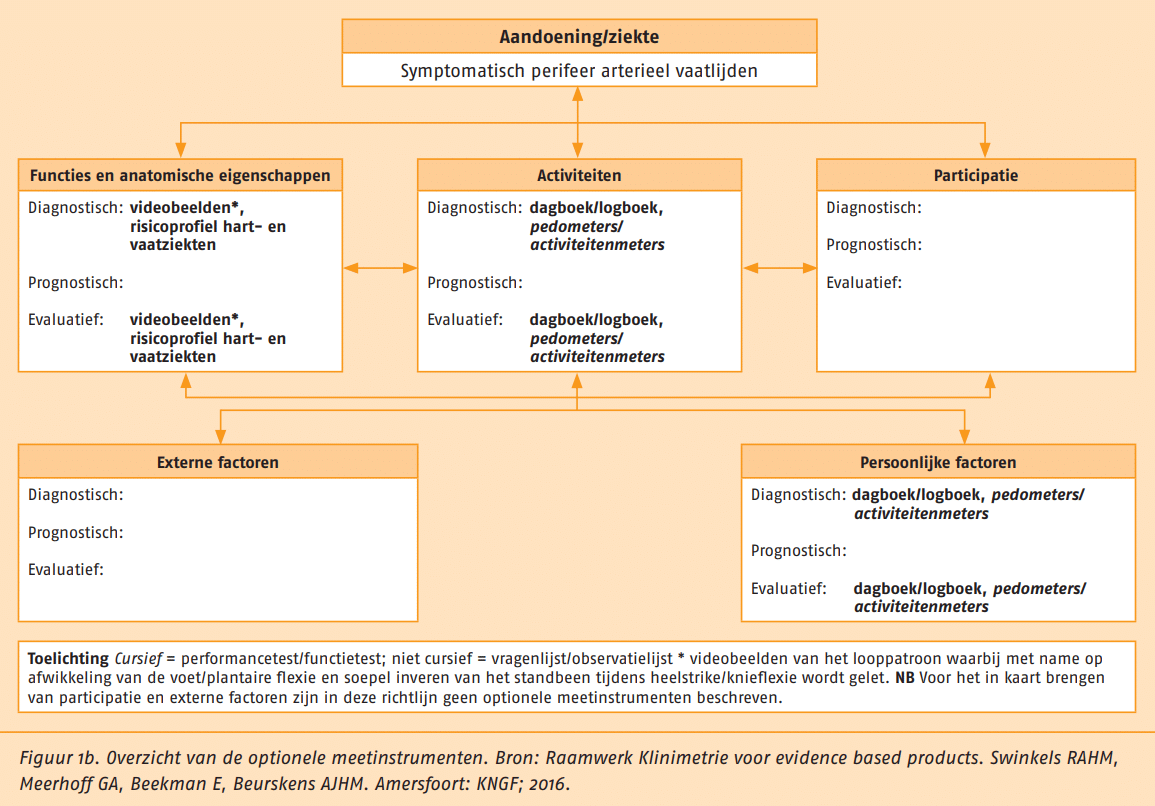
Instrumenten uit beide sets kunnen worden toegepast wanneer daar in de praktijk aanleiding toe is. Al deze meetinstrumenten zijn beschikbaar via www.meetinstrumentenzorg.nl (opent in nieuw tabblad).
B.2 Lichamelijk onderzoek
Het lichamelijk onderzoek bestaat uit:
Inspectie en palpatie (paragraaf B.2.1)
Functieonderzoek (paragraaf B.2.2)
Aanvullend functieonderzoek (paragraaf B.2.3)
B.2.1 Inspectie en palpatie
De fysiotherapeut let specifiek op tekenen van acute verslechtering van de symptomen van sPAV en de belastbaarheid van de patiënt aan de hand van:
- huiddefecten die zijn ontstaan tussen het tijdstip van verwijzing en het moment van de intake;
- opvallend kleur- of temperatuurverschil tussen het linker- en rechterbeen, ontstaan tussen het tijdstip van verwijzing en het moment van de intake;
- enkeloedeem beiderzijds als mogelijke aanwijzing voor hartfalen (zie de KNGF-richtlijn Hartrevalidatie (opent in nieuw tabblad));
- standsafwijkingen van de benen;
- tekenen van acute ischemie (pijn, gevoelsstoornissen, spierzwakte, kleur).
Hoewel palpatie tot de basisvaardigheden van de fysiotherapeut behoort, zijn gegevens die worden verkregen door middel van palpatie niet eenduidig te interpreteren.
De fysiotherapeut let specifiek op tekenen van acute verslechtering van de symptomen van sPAV en de belastbaarheid van de patiënt aan de hand van:
- huiddefecten die zijn ontstaan tussen het tijdstip van verwijzing en het moment van de intake;
- opvallend kleur- of temperatuurverschil tussen het linker- en rechterbeen, ontstaan tussen het tijdstip van verwijzing en het moment van de intake;
- enkeloedeem beiderzijds als mogelijke aanwijzing voor hartfalen: zie de KNGF-richtlijn Hartrevalidatie (opent in nieuw tabblad)45;
- standsafwijkingen van de benen;
- tekenen van acute ischemie (pijn, gevoelsstoornissen, spierzwakte, kleur).
Hoewel palpatie tot de basisvaardigheden van de fysiotherapeut behoort, zijn gegevens die worden verkregen door middel van palpatie niet eenduidig te interpreteren. Afwezigheid van pulsaties is niet altijd het gevolg van vaatlijden, terwijl aanwezigheid van pulsaties vaatlijden/arteriële obstructie niet uitsluit. Daarom is op basis van consensus binnen de werkgroep besloten palpatie niet expliciet als diagnostisch instrument te vermelden in de Praktijkrichtlijn.
B.2.2 Functieonderzoek
Ter evaluatie van het functioneren van de patiënt voert de fysiotherapeut een functieonderzoek uit. Het functieonderzoek bij patiënten met sPAV omvat:
- een loopbandtest;
- het meten van dagelijkse inspanningspatronen;
- vaststellen van de ernst van de pijn;
- evalueren van het looppatroon.
Loopbandtest
De functionele loopafstand (de afstand waarbij de patiënt zou willen stoppen) en de maximale loopafstand (de afstand waarbij de patiënt moet stoppen) worden gemeten met behulp van een loopbandtest (loopsnelheid 3,2 km/uur, toename hellingshoek met 2% elke twee minuten beginnend bij 0%, tot maximaal 10%, duur van de test maximaal 30 minuten).
Het resultaat van de loopbandtest geeft een indicatie van de ernst van de aandoening. Het is aan te bevelen om voorafgaand aan de loopbandtest een proeftest uit te voeren om de patiënt vertrouwd te maken met de procedure van de testafname, het protocol en de uitvoering van de test.
Na afname van de loopbandtest wordt de loopafstand vastgelegd. Tevens wordt gelet op signalen die de loopafstand van de patiënt kunnen beperken:
- lokalisatie van de pijn;
- ernst van de pijn;
- uitputting;
- pijn op de borst;
- benauwdheid;
- angst.
De werkgroep formuleerde de volgende samenvattende aanbevelingen:
(1) Loopbandtest
De loopbandtest is een zinvol meetinstrument voor het vaststellen van de functionele en maximale loopafstanden, als indicatie van de ernst van de klachten bij patiënten met sPAV.
(2) Loopbandtest met toenemende belasting
Een loopbandtest met toenemende belasting is een betrouwbaarder meetinstrument om de ernst van de klachten te bepalen bij patiënten met sPAV dan de loopbandtest met een constante belasting.
Meten van dagelijkse inspanningspatronen
Om de dagelijkse functionele activiteit van de patiënt goed in te schatten, kunnen een dagboek, observaties en elektronische meetsystemen gebruikt worden.
Vaststellen van de ernst van de pijn
De ernst van de pijn wordt tijdens de loopbandtest en de looptraining gemeten met de schaal van het American College of Sports Medicine (ACSM-schaal) voor pijn bij sPAV.
De werkgroep formuleerde de volgende samenvattende aanbeveling:
(3) ACSM-schaal voor pijn
De werkgroep is van mening dat de ACSM-schaal voor pijn (vierpuntsschaal) bij sPAV een zinvol meetinstrument is voor het scoren van de pijn tijdens het lopen bij patiënten met sPAV.
Evaluatie van het looppatroon
De fysiotherapeut signaleert afwijkingen in het looppatroon en beoordeelt de oorzaken van deze afwijkingen, eventueel door gebruik te maken van videobeelden. Bij patiënten met sPAV zijn er met name afwijkingen waar te nemen bij de afwikkeling van de voet en het soepel inveren van het standbeen aan het begin van de standfase (tijdens heelstrike).
De werkgroep formuleerde de volgende samenvattende aanbeveling:
(4) Evaluatie van het looppatroon
De werkgroep is van mening dat, als specifieke veranderingen in het looppatroon de patiënt belemmeren in het lopen, evaluatie van het looppatroon vooral gericht moet zijn op het vaststellen van afwijkingen bij het afwikkelen van de voet en inveren van het standbeen tijdens de heelstrike van de standfase.
Doel van het functieonderzoek is evaluatie van het functioneren van de patiënt. Het functieonderzoek bij patiënten met sPAV omvat:
- een loopbandtest;
- het meten van dagelijkse inspanningspatronen;
- vaststellen van de ernst van de pijn;
- evalueren van het looppatroon.
Indien nodig besluit de fysiotherapeut aanvullend functieonderzoek te verrichten.
NB. Het afnemen van een inspanningstest
Bij patiënten met sPAV kan het inspanningsvermogen verminderd zijn door een verminderd aeroob uithoudingsvermogen en/of door lokale beperkingen ten gevolge van de arteriële obstructie.
Toch beveelt de werkgroep niet aan om een inspanningstest af te nemen als onderdeel van het functieonderzoek. Dit is een wijziging ten opzichte van de ‘KNGF-richtlijn Claudicatio intermittens’ uit 2003.46 Het afnemen van een maximale inspanningstest door de fysiotherapeut is niet aangewezen, omdat patiënten met sPAV een hoogrisicogroep vormen voor het optreden van complicaties. Op grond hiervan is, op basis van consensus binnen de werkgroep, besloten een inspanningstest niet als diagnostisch instrument op te nemen in de Praktijkrichtlijn.
Een submaximale inspanningstest kan wél worden uitgevoerd om het inspanningsvermogen objectief vast te stellen bij aanvang van of gedurende de behandelreeks. Op basis van de resultaten van deze test kunnen de opgestelde fysiotherapeutische behandeldoelen bijgesteld worden.
Loopbandtest
Bij patiënten met sPAV treden er tijdens het lopen klachten op als pijn, kramp of vermoeidheid in het been die veroorzaakt worden door ischemie.24 Deze klachten kunnen leiden tot een afname van de loopafstand.
De loopbandtest wordt uitgevoerd om op objectieve wijze de maximale loopafstand vast te stellen. Tijdens de loopbandtest worden de functionele loopafstand (afstand waarbij de patiënt zou willen stoppen) en de maximale loopafstand (de afstand waarbij de patiënt moet stoppen) gemeten. Deze metingen geven een indicatie van de ernst van de aandoening. Omdat de hulpvraag van de patiënt centraal staat, worden de resultaten van de test afgezet tegen de loopafstand die nodig is voor ADL, arbeidsgerelateerde en huishoudelijke activiteiten, vrije tijdsbesteding en de Nederlandse Norm Gezond Bewegen (NNGB).
Kruidenier et al. onderzochten de betrouwbaarheid en validiteit van de meting van de functionele loopafstand en vergeleken deze met de betrouwbaarheid en validiteit van metingen van de pijnvrije (afgelegde afstand op het moment dat de pijn begint) en de maximaleloopafstand bij patiënten met claudicatio intermittens die looptraining kregen.47 Uit dit onderzoek bleek dat het meten van de functionele loopafstand betrouwbaar en valide is en sterk correleert met de functionele beperkingen van de patiënt. Tevens bleek dat de functionele loopafstand mogelijk beter overeenkomt met de daadwerkelijke functionele beperkingen van patiënten dan de pijnvrije en maximale loopafstanden.47
Omdat patiënten in het dagelijks leven waarschijnlijk niet stoppen met lopen bij de eerste pijn, is de werkgroep van mening dat het meten van de functionele loopafstand meer aangewezen is voor de bepaling van de ernst van de aandoening en beter aansluit bij de hulpvraag van de patiënt dan het meten van de pijnvrije loopafstand.
Het is aan te bevelen om voorafgaand aan de loopbandtest, op een andere dag, een proeftest uit te voeren. Tijdens deze proeftest kan de patiënt vertrouwd raken met de loopband en de testprocedure. De betrouwbaarheid van de loopbandtest neemt door het uitvoeren van een proeftest toe.48 Tijdens deze proeftest kan de fysiotherapeut tevens de optimale loopsnelheid voor de patiënt bepalen, om deze vervolgens tijdens de fysiotherapeutische behandeling te hanteren.
De loopbandtest biedt tevens mogelijkheid voor het meten van bloeddruk, zuurstofsaturatie en subjectieve pijnbeleving ACSM-vierpuntsschaal van de American College of Sports Medicine.49Tijdens de loopbandtest is de fysiotherapeut alert op tekenen van cardiale overbelasting, zoals pijn of een drukkend gevoel op de borst, mogelijk met uitstraling naar de (linker)arm en (linker)kaak, ernstige vermoeidheid of kortademigheid die niet in relatie staat tot de geleverde inspanning, flauwvallen, duizeligheid en/of vegetatieve reacties (misselijkheid, transpiratie, bleekheid).45
Bij vrouwen dient de fysiotherapeut extra alert te zijn, omdat cardiale problemen zich bij hen vaak op een meer aspecifieke manier presenteren. Ook kan pijn in de benen optreden zonder vasculaire oorzaak,49 maar op neurogene of orthopedische gronden.
In deze richtlijn wordt niet nader ingegaan op het onderkennen van klachten op andere dan cardiale of vasculaire gronden.
Uitvoering van de loopbandtest
De loopbandtest dient te worden afgenomen met oplopende intensiteit door de hellingshoek tijdens de test in stappen te verhogen met als doel de klachten te provoceren. De loopsnelheid dient ingesteld te worden op 3,2 km/uur. Er wordt gestart met een hellingshoek van 0%. Vervolgens wordt de hellingshoek progressief verhoogd: elke 2 minuten met 2% tot maximaal 10%.50 De duur van de test bedraagt maximaal 30 minuten.
Uit onderzoek is gebleken dat de loopbandtest een betrouwbaar instrument is voor het vaststellen van de pijnvrije en maximale loopafstand.50,51 Nicolaï et al. onderzochten de betrouwbaarheid van verschillende protocollen voor de loopbandtest.51 In hun meta-regressieanalyse, die was gebaseerd op acht studies, vergeleken zij loopbandtesten voor de bepaling van de pijnvrije en maximale loopafstand met een constante belasting en loopbandtesten met een toenemende (‘graded’) belasting. Zij concludeerden dat een loopbandtest met een toenemende belasting de hoogste betrouwbaarheid geniet voor de bepaling van de maximale loopafstand. Bij gebruik van een loopbandtest met een constante belasting (bijvoorbeeld om praktische redenen), is een test met een hellingshoek van 12% betrouwbaarder dan een test met een hellingshoek van 0% of 10%.51 Voor de bepaling van de pijnvrije loopafstand vonden zij geen verschillen in betrouwbaarheid tussen loopbandtesten met een constante en toenemende belasting.51
Conclusies
Loopbandtest (niveau 1)
- Het is aangetoond dat de loopbandtest een zinvol meetinstrument is voor het vaststellen van de functionele en maximale loopafstanden, als indicatie van de ernst van de klachten bij patiënten met sPAV.
Kwaliteit van de gevonden artikelen: A1 (Nicolaï et al., 200951), B (Gardner et al., 199150).
Loopbandtest met toenemende belasting (niveau 1)
- Het is aangetoond dat een loopbandtest met een toenemende belasting een betrouwbaarder meetinstrument is om de ernst van de klachten te bepalen bij patiënten met sPAV dan een loopbandtest met een constante belasting.
Kwaliteit van het gevonden artikel: A1 (Nicolaï et al., 200951).
Overige overwegingen
De loopbandtest kan ook worden gebruikt voor een subjectieve inschatting van het inspanningsvermogen. Tijdens het uitvoeren van de loopbandtest wordt gelet op de wijze waarop de patiënt omgaat met zijn klachten. Bij een inadequate pijntolerantie zal de patiënt uit angst voor (de schadelijke gevolgen van) pijn de inspanning eerder afbreken. De patiënt stopt de inspanning bij een beginnende pijn, graad 1 of 2 op de ACSM-schaal.49 Dan is er weinig verschil tussen de functionele en de maximale loopafstand.
Naast inadequaat pijngedrag kan bij de patiënt ook angst voor inspanning bestaan. Deze angst kan verlammend werken op het lichamelijk prestatievermogen, zoals bekend is bij hartpatiënten.45,52 De angst voor inspanning wordt geëvalueerd aan de hand van de anamnese en observatie tijdens de loopbandtest en de gegeven trainingen. De patiënt zal een lichte belasting als zwaar ervaren. Dit zal blijken uit een hoge score op de Borg Rating of Perceived Exertion Scale (RPE-schaal) of de ACSM-schaal voor pijn, terwijl dit niet lijkt overeen te komen met de objectieve belastingsverschijnselen.
Ten slotte moeten de resultaten van de loopbandtest gekoppeld worden aan de vereiste hoeveelheid trainingsarbeid ter preventie van hart- en vaatziekten. De behandeling is mede gericht op een positieve beïnvloeding van de risicofactoren voor atherosclerose. Om dit te bereiken moet de patiënt dagelijks 30 minuten kunnen bewegen met een matige intensiteit conform de NNGB (≥ 3 à 4 MET’s).53 Een hoger energieverbruik (langere trainingsduur) heeft waarschijnlijk een beter effect op de risicofactoren voor atherosclerose, met name overgewicht/obesitas, zoals gebleken is uit een studie bij patiënten met coronarialijden.45,54
De loopbandtest kan door een fysiotherapeut worden uitgevoerd als de verwijzer de patiënt tot een dergelijke inspanning in staat acht. Indien de cardiale belastbaarheid van de patiënt verandert gedurende de behandelperiode, overlegt de fysiotherapeut met de verwijzer over een cardiologische screening.
De Zes-minuten wandeltest (6MWT)
Naast de loopbandtest met oplopende intensiteit wordt ook wel de gestandaardiseerde Zes-minuten wandeltest gebruikt.49 Deze test is echter niet gevalideerd voor deze patiëntengroep. Daarom heeft de werkgroep besloten om in deze richtlijn de Zes-minuten wandeltest niet als diagnostisch instrument aan te bevelen.
Op basis van bovenstaande formuleerde de werkgroep de volgende samenvattende aanbevelingen:
(1) Loopbandtest
De loopbandtest is een zinvol meetinstrument voor het vaststellen van de functionele en maximale loopafstanden, als indicatie van de ernst van de klachten bij patiënten met sPAV.
(2) Loopbandtest met toenemende belasting
Een loopbandtest met toenemende belasting is een betrouwbaarder meetinstrument om de ernst van de klachten te bepalen bij patiënten met sPAV dan de loopbandtest met een constante belasting.
Meten van dagelijkse inspanningspatronen
Om de dagelijkse functionele activiteit van de patiënt goed in te schatten, kunnen dagboekjes, observaties en elektronische meetsystemen gebruikt worden. Pedometers en driedimensionale activiteitenmeters zijn nog volop in ontwikkeling en worden tot nog toe vooral in wetenschappelijk onderzoek gebruikt. Er zijn high en lowtech activiteitenmeters, waarbij steeds meer toepassingen aan smartphones en horloges gekoppeld kunnen worden.
Op dit moment acht de werkgroep het nog niet mogelijk om al een voorkeur voor een bepaald meetsysteem uit te spreken.
Vaststellen van de ernst van de pijn (ACSM-schaal)
Tijdens de loopbandtest en de looptraining kan de ACSM-schaal voor pijn bij sPAV gebruikt worden.49 Deze subjectieve schaal meet de ernst van de pijn en loopt van graad 1 t/m 4.
Op basis van bovenstaande formuleerde de werkgroep de volgende samenvattende aanbeveling:
(3) ACSM-schaal voor pijn
De werkgroep is van mening dat de ACSM-schaal voor pijn (vierpuntsschaal) bij sPAV een zinvol meetinstrument is voor het scoren van de pijn tijdens het lopen bij patiënten met sPAV.
Evaluatie van het looppatroon
Bij patiënten met sPAV treden tijdens het lopen specifieke veranderingen op in het looppatroon. Vaak is sprake van een verminderde afwikkeling van de voet (verminderde plantaire flexie) aan het einde van de standfase en de afwezigheid van knieflexie in de vroege standfase.55-60 Dit leidt tot een afname van de loopsnelheid en een verminderde staplengte bij deze patiënten.57De volgende veranderingen in het looppatroon zijn kenmerkend voor personen met sPAV:
- de afzet aan de aangedane zijde is minder krachtig: er is geen (actieve) hielheffing;
- knieflexie in de vroege standfase ontbreekt: vaak is sprake van extensie of hyperextensie in de vroege standfase;
- de afwikkeling van de voet is verminderd;
- tijdens hielcontact is de dorsale flexie verminderd;
- het eerste grondcontact vindt plaats met de gehele voet;
- de stapfrequentie is lager.
Deze aanpassingen zijn compensatiemechanismen die optreden om PAV-klachten te vermijden of te verminderen en zijn kenmerkend voor het passieve gaan.61 Op den duur kunnen deze compensatiemechanismen de patiënt echter hinderen bij het lopen.
De fysiotherapeut signaleert afwijkingen in het looppatroon en beoordeelt de oorzaken van deze afwijkingen, eventueel door gebruik te maken van videobeelden. Bij patiënten met sPAV zijn met name afwijkingen waar te nemen bij de afwikkeling van de voet en het soepel inveren van het standbeen bij het begin van de standfase (tijdens heelstrike).
Afhankelijk van de behoefte van de patiënt en de expertise van de fysiotherapeut kan besloten worden tijdens de behandeling aandacht te besteden aan het verbeteren van het looppatroon.
Op basis van bovenstaande formuleerde de werkgroep de volgende samenvattende aanbeveling:
(4) Evaluatie van het looppatroon
De werkgroep is van mening dat, als specifieke veranderingen in het looppatroon de patiënt belemmeren in het lopen, evaluatie van het looppatroon vooral gericht moet zijn op het vaststellen van afwijkingen bij het afwikkelen van de voet en inveren van het standbeen tijdens de heelstrike van de standfase.
B.2.3 Aanvullend functieonderzoek
De uitgebreidheid van het functieonderzoek hangt af van de ernst van het gezondheidsprobleem zoals uit de anamnese naar voren is gekomen. Eventueel aanvullend functieonderzoek kan bestaan uit:
- vaststellen van de spierkracht;
- mobiliteitsonderzoek;
- evaluatie van coördinatie/stabiliteit;
- sensibiliteitsonderzoek (in geval van diabetes mellitus).
De uitslag van de testen wordt met de patiënt besproken. Hierbij dient de nadruk te liggen op het benoemen van de punten die wél goed gingen. De minder goede punten komen in het behandelplan aan de orde.
De uitgebreidheid van het functieonderzoek hangt af van de ernst van het gezondheidsprobleem. Eventueel aanvullend onderzoek omvat sensibiliteitsonderzoek met 10-grams Semmes Weinstein monofilamenten (bij diabetes mellitus), spierkracht, mobiliteit en coördinatie/stabiliteit.62
Het afnemen van dergelijke functieonderzoeken behoort tot de basisvaardigheden van de fysiotherapeut. Hierop wordt in deze richtlijn dan ook niet nader ingegaan.
B.3 Differentiaaldiagnostiek
In de differentiaaldiagnose van sPAV staan de volgende aandoeningen centraal:
- lumbale wervelkanaalstenose (neurogene claudicatio)
- diabetische neuropathie
- artrose
- varices en chronische veneuze insufficiëntie
- chronisch compartimentsyndroom
- bakercyste
Er dient opgemerkt te worden dat bij sommige patiënten de verschillende aandoeningen ook in combinatie kunnen voorkomen. Daarnaast is er sprake van overlap in de klachtenpresentatie van de verschillende ziektebeelden.
De fysiotherapeut stelt vast of een of meerdere van deze aandoeningen bij de patiënt aanwezig zijn. Na de differentiaaldiagnostiek kan de fysiotherapeut bepalen welk probleem primair ten grondslag ligt aan de beperkingen in de loopfunctie of de trainbaarheid en welke interventie gewenst is.
De manier waarop de genoemde aandoeningen zich tijdens de behandeling kunnen voordoen als sPAV is beschreven in de Verantwoording van deze paragraaf.
Andere aandoeningen kunnen klachten geven die sterk lijken op de klachten ten gevolge van sPAV. Na de differentiaaldiagnostiek kan de fysiotherapeut bepalen welk probleem primair ten grondslag ligt aan de beperkingen in de loopfunctie of de trainbaarheid en welke interventie gewenst is. Tevens dient opgemerkt te worden dat de verschillende aandoeningen ook samen kunnen voorkomen bij sommige patiënten.
Differentiaaldiagnostisch kan worden gedacht aan: lumbale wervelkanaalstenose (neurogene claudicatio), diabetische neuropathie, artrose, varices en chronische veneuze insufficiëntie, chronisch compartimentsyndroom en een bakercyste.
B.4.1 Lumbale wervelkanaalstenose: neurogene claudicatio
Lumbale wervelkanaalstenose wordt veroorzaakt door een of meerdere vernauwing(en) in en rondom het wervelkanaal.63 Deze vernauwingen zijn meestal het gevolg van degeneratieve veranderingen van de benige en weke delen van de wervelkolom. Bij patiënten met een dergelijke vernauwing ontstaat tijdens het lopen pijn; bij sommige patiënten ontstaan ook neurologische prikkelings- en uitvalsverschijnselen, soms in beide benen.63 Deze klachten verdwijnen echter niet bij stilstaan, zoals bij sPAV, maar door een houdingsverandering (bijvoorbeeld door de rug te buigen, te gaan zitten of te bukken). Een ander verschil met sPAV is dat patiënten met neurogene claudicatio bergop lopen soms als minder pijnlijk ervaren dan vlak lopen.64 De fysiotherapeut let op de volgende symptomen en verschijnselen:
- de pijn en eventuele uitvalsverschijnselen volgen een dermatomaal patroon;
- neurologische uitval (sensibiliteit, kracht, reflexen);
- de klachten nemen toe bij extensie en/of nemen af bij flexie van de lumbale wervelkolom.
Bij een vermoeden van neurogene claudicatio is het wenselijk met de verwijzer te overleggen over het te volgen beleid.
B.4.2 Diabetische neuropathie
Diabetische neuropathie kenmerkt zich door de aanwezigheid van symptomen en/of tekenen van perifere neuropathie bij patiënten met diabetes mellitus, na uitsluiting van andere oorzaken.65 Diabetische neuropathie wordt ingedeeld in verschillende stadia, die richting geven aan de diagnostiek en behandeling.65
De fysiotherapeut stelt vast of:
- de pijn en eventuele uitvalsverschijnselen optreden volgens een diffuus patroon;
- de pijn en eventuele uitvalsverschijnselen optreden in rust;
- neurologische uitval (niet-segmentale samenhang) aanwezig is (sensibiliteit, kracht, reflexen).
B.4.3 Artrose
Artrose kenmerkt zich door een langzaam en wisselend progressief verlies van gewrichtskraakbeen. Symptomen zijn pijn, stijfheid en, op den duur, een achteruitgang in het dagelijks functioneren; deze achteruitgang ontstaat vermoedelijk vooral door een gebrek aan beweging.66 De pijn treedt aanvankelijk op bij aanvang van de beweging en bij langdurig belasten. De pijn neemt vaak toe naarmate de dag vordert. In latere fasen is er ook pijn in rust en nachtelijke pijn.66 Daarnaast kan er sprake zijn van een verminderde beweeglijkheid in de gewrichten, verminderde spierkracht, instabiliteit van de gewrichten en crepitaties.66
B.4.4 Varices en chronische veneuze insufficiëntie
Het gelijktijdig aanwezig zijn van varices of, in een later stadium, chronische veneuze insufficiëntie kan het klachtenbeeld van sPAV negatief beïnvloeden. De klachten bestaan uit pijn, een vermoeid, zwaar of gespannen gevoel in de benen, vooral ter plaatse van de varices of in de kuit(en). Deze klachten nemen vaak gedurende de dag toe en verergeren na staan of lang stilzitten, vooral in een warme omgeving. Activatie van de spierpomp door beweging of het hoog leggen van de benen kan de klachten verminderen. Bij enkelvoudige veneuze insufficiëntie kan pitting oedeem optreden.
De fysiotherapeut stelt vast of:
- de klachten verminderen door beweging of het hoog leggen van het been;
- de patiënt huidafwijkingen heeft of (in de loop van de dag) last krijgt van dikke voeten.
Als varices of chronische veneuze insufficiëntie het succesvol uitvoeren van oefentherapie in de weg staat, rapporteert de fysiotherapeut dit aan de verwijzer.
B.4.5 Inspanningsgebonden chronisch compartimentsyndroom
Het inspanningsgebonden chronisch compartimentsyndroom kan zich in verschillende, door fascie omgeven spiergroepen manifesteren.67 De klachten bestaan uit zwelling en soms functiebeperking in de aangedane spierloges van meestal het onderbeen of de onderarmen bij inspanning.67 Tijdens inspanning ontstaat er een acute of chronisch progressieve toename van de druk in het compartiment, waardoor de circulatie en de functie van de weefsels in de hierdoor ontstane ‘afgesloten’ ruimte worden verstoord.67 Hierdoor ervaart de patiënt een inspanningsgebonden pijn in het betreffende compartiment die gepaard gaat met functieverlies van de betrokken spiergroep, waardoor uiteindelijk de inspanningen moeten worden gestaakt.67
B.4.6 Bakercyste
De bakercyste betreft een meestal niet-pijnlijke, fluctuerende zwelling in de knieholte. De cyste ontstaat waarschijnlijk doordat een in de knieholte aanwezige bursa vanuit het kniegewricht wordt gevuld als gevolg van een overproductie van synoviale vloeistof.68
Deze overproductie kan veroorzaakt worden door een al dan niet symptomatische intra-articulaire aandoening zoals artrose, reumatoïde artritis of een meniscusletsel.68 De bakercyste zal in wisselende mate aanwezig blijven zolang de onderliggende oorzaak niet is weggenomen.68 De cyste kan een strak gevoel geven in de knieholte en het gebruik van de knie, bijvoorbeeld bij flexie, belemmeren. Bij intensieve belasting van de knie, zoals tijdens lang lopen, kunnen de klachten toenemen.
B.4 Comorbiditeit
Patiënten kunnen naast sPAV nog andere aandoeningen hebben die een beperking opleveren bij het lopen of de trainbaarheid. Aandoeningen die van invloed kunnen zijn op de loopfunctie of de trainbaarheid, zijn:
- diabetes mellitus;
- chronisch obstructieve longziekten (COPD);
- hartfalen;
- angina pectoris;
- cerebrovasculair accident (CVA);
- artrose;
- klachten van wervelkolom/SI-gewricht/heupgewricht/kniegewricht, voet(en).
De fysiotherapeut dient de training op deze specifieke comorbiditeiten af te stemmen. Als de fysiotherapeut op basis van zijn ervaringen en vaardigheden bemerkt dat het trainingsresultaat minder is dan verwacht bij de individuele patiënt, vermeldt hij de mogelijke invloed van deze aandoeningen in de rapportage aan de verwijzer.
De invloed van de genoemde aandoeningen op de behandeling staat in de Verantwoording en toelichting.
Patiënten kunnen naast sPAV nog andere aandoeningen hebben die een beperking opleveren voor de loopfunctie of trainbaarheid. De training dient op deze specifieke comorbiditeiten te worden aangepast. Er bestaat echter nog geen evidentie over de optimale fysiotherapeutische behandeling bij patiënten met één of meerdere comorbiditeiten.
Veel voorkomende comorbiditeiten bij sPAV zijn diabetes mellitus, COPD, hartfalen, angina pectoris, cerebrovasculair accident (CVA), artrose en klachten van wervelkolom, SI-gewricht, heupgewricht, kniegewricht en voet.
Als de fysiotherapeut inschat dat de aanwezige comorbiditeit een belemmering oplevert voor het succesvol uitvoeren van de behandeling, wordt dit gerapporteerd aan de verwijzer.
B.4.1 Diabetes mellitus
De trainbaarheid van patiënten die tevens diabetes mellitus hebben, zal zeker aan het begin van de training beperkt zijn. Voor het bereiken van trainingseffecten is een goed hormonaal evenwicht met een goed functionerend anabool metabolisme nodig.69 De fysiotherapeut dient hiermee rekening te houden in het trainingsprogramma. Zie de KNGF-standaard Beweeginterventie diabetes mellitus type 2 (opent in nieuw tabblad) voor aanbevelingen over de fysiotherapeutische behandeling bij patiënten met diabetes mellitus.69
B.4.2 COPD
Chronisch obstructieve longziekten (COPD (opent in nieuw tabblad)) is een groep vermijdbare en behandelbare aandoeningen met significante extrapulmonale effecten, die kunnen bijdragen tot de ernst van COPD bij de individuele patiënt.70 De pulmonale component van COPD wordt gekenmerkt door luchtwegobstructie die niet volledig reversibel is. De luchtwegobstructie is progressief en geassocieerd met een abnormale inflammatoire respons van de longen op schadelijke partikels of gassen. Bij patiënten met COPD is de fysieke activiteit in het dagelijks leven significant verminderd in vergelijking met die van gezonde ouderen.71
Ongeveer 16 tot 19% van de patiënten met sPAV heeft tevens COPD.39,72,73 De combinatie van sPAV en COPD kan invloed hebben op de mate waarin de patiënt trainbaar is. De fysiotherapeut dient hiermee rekening te houden en kan andere (gecombineerde) trainingsvormen toepassen. Zie de KNGF-richtlijn COPD (opent in nieuw tabblad) voor aanbevelingen voor de fysiotherapeutische behandeling bij patiënten met COPD.71
B.4.3 Hartfalen
Enkeloedeem beiderzijds kan wijzen op chronisch hartfalen. Overige symptomen en verschijnselen bij hartfalen zijn: kortademigheid en/of vermoeidheid bij inspanning of zelfs in rust, mogelijk ook ’s nachts, en gewichtstoename. De combinatie van sPAV en hartfalen kan de trainbaarheid van de patiënt beïnvloeden. Zie de KNGF-richtlijn Hartrevalidatie (opent in nieuw tabblad) voor aanbevelingen over de fysiotherapeutische behandeling bij patiënten met hartfalen.45
B.4.4 Angina pectoris
Angina pectoris, ofwel pijn op de borst, wordt veroorzaakt door een vernauwing van de kransslagaders, waardoor een deel van de hartspier te weinig zuurstof krijgt. De klachten bij patiënten met angina pectoris treden vaak op wanneer de hartspier meer zuurstof nodig heeft, zoals tijdens lichamelijke inspanning of bij de overgang van een warme naar een koude omgeving. Tijdens deze provocerende momenten ervaren patiënten een beklemmende, drukkende of benauwende pijn op de borst, mogelijk met uitstraling naar andere delen van het lichaam zoals de onderkaak, hals, schouderbladen of (linker)arm. Bij stabiele angina pectoris verdwijnen de klachten vaak enkele minuten na het staken van de lichamelijke inspanning. Er is sprake van instabiele angina pectoris bij recent ontstane ernstige of frequent optredende klachten, of bij progressie van de klachten, waarbij deze steeds vaker en onregelmatiger optreden.74 De combinatie van angina pectoris en sPAV kan de trainbaarheid van de patiënt beïnvloeden. Zie de KNGF-richtlijn Hartrevalidatie (opent in nieuw tabblad) voor aanbevelingen over de fysiotherapeutische behandeling bij patiënten met angina pectoris.45
B.4.5 Cerebrovasculair accident (CVA)
Een CVA, ofwel beroerte, is onder te verdelen in een hersenbloeding en een herseninfarct. Een hersenbloeding wordt veroorzaakt door een beschadiging van een bloedvat in de hersenen waardoor het bloed vanuit het bloedvat het hersenweefsel instroomt. Bij een herseninfarct wordt een bloedvat in de hersenen afgesloten door atherosclerose of een bloedpropje (embolie), waardoor zuurstoftekort optreedt in een deel van de hersenen en dit hersenweefsel uiteindelijk afsterft. Van de patiënten met een CVA overlijdt ongeveer 15% binnen één week en 25% binnen 1 maand.75 Patiënten die hun CVA overleven, hebben vaak te maken met zowel lichamelijke, geestelijke als cognitieve beperkingen, zoals verlamming, uitvalsverschijnselen, depressie en afasie (problemen met taal, spreken, lezen en schrijven).75
De mogelijke gevolgen van een CVA, waaronder een verminderde loopvaardigheid, kunnen een beperking vormen voor de trainbaarheid van de patiënt. De fysiotherapeut dient hiermee rekening te houden in het trainingsprogramma. Zie de KNGF-richtlijn Beroerte (opent in nieuw tabblad) voor aanbevelingen over de fysiotherapeutische behandeling bij patiënten met een beroerte.76
B.4.6 Artrose
Artrose kan soortgelijke klachten geven als sPAV (differentiaaldiagnostiek, maar kan ook als comorbiditeit van sPAV optreden. Uit de Amerikaanse ‘The Women’s Health and Aging Study’ bleek dat de prevalentie van knie- en heupartrose respectievelijk 41,5% en 25,9% was bij vrouwen van 65 jaar en ouder met een enkel-armindex < 0,90.77 Als artrose tot problemen leidt bij de loopbandtraining, kunnen andere inspanningsvormen zoals fietsen geprobeerd worden.
Zie ook de KNGF-richtijn Artrose heup-knie (opent in nieuw tabblad).
B.4.7 Klachten van wervelkolom, SI-gewricht, heupgewricht, kniegewricht en voet
Klachten in de biomechanische keten tussen wervelkolom en voetregio kunnen voor patiënten met sPAV leiden tot een extra beperking in de loopfunctie. Kenmerkend voor deze beperking zijn vooral de startklachten bij aanvang van het lopen. Als een patiënt enige tijd loopt, nemen de klachten af en verbetert het looppatroon. Bij verdere provocatie van een aangedaan gewricht kunnen de klachten echter opnieuw optreden, waardoor het looppatroon bij langdurig lopen kan gaan lijken op het beeld bij sPAV.
Het vaststellen van beperkingen in de biomechanische keten tussen wervelkolom en voetregio valt onder de basisvaardigheden van de fysiotherapeut.
B.5 Indicatiestelling
Op basis van de gegevens die zijn verkregen uit de verwijzing, de anamnese en het lichamelijk onderzoek bepaalt de fysiotherapeut of er een indicatie is voor fysiotherapie. De indicatiestelling vindt plaats aan de hand van de antwoorden op de volgende vier screeningsvragen:
- Is de functionele en/of maximale loopafstand en/of het uithoudingsvermogen verminderd in verhouding tot het gewenste activiteitenniveau (al dan niet veroorzaakt door inadequaat pijngedrag of angst voor inspanning)?
- Zijn er problemen met specifieke functionele vaardigheden?
- Bestaat er een afwijkend looppatroon ten gevolge van de aan sPAV gerelateerde klachten?
- Is er sprake van door de fysiotherapeut beïnvloedbaar risico-gedrag, zoals bewegingsarmoede, roken, voeding?
Er is een indicatie voor fysiotherapie indien minimaal vraag 1 en/of vraag 2 met ‘ja’ beantwoord kunnen worden, eventueel in combinatie met een positief antwoord op vraag 3 en 4, én als de fysiotherapeut inschat dat de in deze vragen beschreven problemen in voldoende mate beïnvloedbaar zijn door fysiotherapie, rekening houdend met de mogelijke invloed van comorbiditeiten. Indien de fysiotherapeut inschat dat de behandeling van sPAV te veel beperkt zal worden door de comorbiditeiten van de patiënt, dient de patiënt terugverwezen te worden naar de verwijzer.
Indien de fysiotherapeut de indicatie voor fysiotherapie niet kan bevestigen of indien er rode/gele vlaggen worden gesignaleerd, neemt de fysiotherapeut contact op met de verwijzer voor overleg. Indien wenselijk adviseert de fysiotherapeut de patiënt contact op te nemen met een medisch specialist.
Of er een indicatie is voor fysiotherapie wordt vastgesteld aan de hand van de antwoorden op de volgende vier screeningsvragen:
- Is de functionele en/of maximale loopafstand en/of het uithoudingsvermogen verminderd in verhouding tot het gewenste activiteitenniveau (al dan niet veroorzaakt door inadequaat pijngedrag of angst voor inspanning)?
- Zijn er problemen met specifieke functionele vaardigheden?
- Bestaat er een afwijkend looppatroon ten gevolge van de aan sPAV gerelateerde klachten?
- Is er sprake van door de fysiotherapeut beïnvloedbaar risico-gedrag, zoals bewegingsarmoede, roken en voeding?
Er is een indicatie voor fysiotherapie indien minimaal vraag 1 en/of vraag 2 met ‘ja’ beantwoord kunnen worden, eventueel in combinatie met een positief antwoord op vraag 3 en 4, én als de fysiotherapeut inschat dat de in deze vragen beschreven problemen in voldoende mate beïnvloedbaar zijn door fysiotherapie, rekening houdend met de mogelijke invloed van comorbiditeiten. Indien de fysiotherapeut inschat dat de behandeling van sPAV te veel beperkt zal worden door de comorbiditeiten van de patiënt, dient de patiënt terugverwezen te worden naar de verwijzer.
Indien de fysiotherapeut de indicatie voor fysiotherapie niet kan bevestigen of indien er rode/gele vlaggen worden gesignaleerd, neemt de fysiotherapeut contact op met de verwijzer voor overleg. Indien wenselijk adviseert de fysiotherapeut de patiënt contact op te nemen met een medisch specialist.
B.6 Opstellen van het behandelplan
Na de indicatiestelling wordt, in overleg met de patiënt (shared decision-making), op grond van de hulpvraag van de patiënt en de diagnostische bevindingen het behandelplan geformuleerd. Het behandelplan wordt, met instemming van de patiënt, schriftelijk vastgelegd en besproken met de patiënt en bij voorkeur ook met de partner/mantelzorger. Als de patiënt tevens onder behandeling is bij, of begeleid wordt door een andere discipline vindt hiermee idealiter afstemming plaats.
Voor meer informatie over samen beslissen, zie module ‘A.8 Samen beslissen (opent in nieuw tabblad)‘ en module ‘C.8 De keuze voor de behandeling (opent in nieuw tabblad)‘.
Na de indicatiestelling wordt, in overleg met de patiënt (shared decision-making78), het behandelplan opgesteld.

