Therapeutisch proces
Inleiding
Het primaire doel van de behandeling bij patiënten met sPAV is het aanpakken van de hulpvraag van de patiënt, waarbij het verbeteren van functioneren, verbeteren van activiteiten en het bevorderen van participatie centraal staan. Daarnaast is een positieve beïnvloeding van risicofactoren voor atherosclerose een belangrijk aandachtspunt in de behandeling.
De hoofddoelen van de fysiotherapeutische behandeling kunnen als volgt worden samengevat:
- de patiënt in staat stellen de door hem gewenste activiteiten en participatie uit te voeren (de hulpvraag van de patiënt),
- het beïnvloeden van risicofactoren voor atherosclerose,
- het aanleren van een toenemende mate van zelfstandigheid en zelfmanagement in de training en het onderhouden van een actieve leefstijl door de patiënt en
- het verbeteren van de kwaliteit van leven van de patiënt.
Gedurende de eerste vier weken van de fysiotherapeutische behandeling vinden er gemiddeld drie sessies per week plaats, daarna volstaan twee sessies per week tot aan het einde van de derde maand. Van maand vier t/m 12 van de behandelingsperiode vinden er gemiddeld één tot twee sessies per maand plaats. Na deze behandelperiode vindt idealiter elk kwartaal (vier keer per jaar) een controle plaats bij een zorgverlener. In de volgende tabel staat een voorbeeld van een behandelschema dat is samengesteld op basis van consensus binnen de werkgroep. Dit behandelschema (ongeveer 40 sessies in het eerste jaar) is richtinggevend. In specifieke gevallen kunnen meer of minder sessies nodig zijn.

Voorbeeld van een behandelschema.
Tijdens de fysiotherapeutische behandeling streven patiënt en fysiotherapeut naar afname van de afhankelijkheid van de patiënt (zelfmanagement). De fysiotherapeut stuurt erop aan dat de patiënt steeds zelfstandiger gaat trainen en dat de patiënt zelf verantwoording neemt voor de eigen training. Vanaf het begin van de behandeling is het dan ook belangrijk om aan de patiënt duidelijk te maken dat verdergaande resultaten vooral bereikt worden als de patiënt, naast de fysiotherapeutische behandeling, zelfstandig traint in de thuissituatie. Daartoe krijgt hij van de fysiotherapeut een trainingsprogramma. In de loop van de tijd neemt de frequentie van de fysiotherapeutische behandelingen af en nemen de door de patiënt zelfstandig uitgevoerde bewegingsactiviteiten in frequentie en omvang toe. Tijdens de behandelsessies bespreekt de fysiotherapeut het belang, de voortgang en eventuele knelpunten van het trainingsprogramma voor thuis met de patiënt.
Na afloop van de behandelperiode van drie maanden (of eerder als de behandeldoelen zijn behaald) kan de fysiotherapeut gedurende drie tot zes maanden de patiënt coachen. De patiënt voert het trainingsprogramma zelfstandig uit en de fysiotherapeut kan de trainingsvoortgang evalueren en controleren aan de hand van een logboek, dat door de patiënt wordt ingevuld. Een voorbeeld van een activeringsprogramma is opgenomen in bijlage (opent in nieuw tabblad) 3. Op deze manier is de kans groter dat de patiënt een actieve leefstijl kan blijven handhaven.
Afhankelijk van de diagnostische bevindingen kan de behandeling gericht zijn op:
- het geven van informatie en voorlichting ter bevordering van het ziekte-inzicht van de patiënt;
- het verbeteren van het (subjectieve en objectieve) inspanningsvermogen;
- het optimaliseren van activiteiten en participatie van de patiënt;
- het ondersteunen van de patiënt op het gebied van cardiovasculair risicomanagement.
In de volgende paragrafen worden de afzonderlijke elementen van de behandeling nader beschreven.
Het primaire doel van de behandeling bij patiënten met sPAV is het aanpakken van de hulpvraag van de patiënt, waarbij het verbeteren van functioneren, verhogen van activiteiten en het bevorderen van participatie centraal staan. Patiënten met sPAV hebben een verhoogd risico op het ontwikkelen van andere aandoeningen zoals cardio- of cerebrovasculaire aandoeningen. Positieve beïnvloeding van de risicofactoren voor atherosclerose is een belangrijk aandachtspunt in de behandeling. Om die reden is tijdens de behandeling aandacht voor stoppen met roken en is het belangrijk om de motivatie voor stoppen met roken te beïnvloeden. Er moet aandacht zijn voor het belang van een gezond voedingspatroon, al dan niet in overleg met andere zorgverleners. De fysiotherapeut levert ook een bijdrage aan de bestrijding van bewegingsarmoede en het stimuleren van een lichamelijk actieve leefstijl bij de patiënt.
De hoofddoelen van de fysiotherapeutische behandeling kunnen als volgt worden samengevat:
- de patiënt in staat stellen de door hem gewenste activiteiten en participatie uit te voeren (de hulpvraag van de patiënt),
- het beïnvloeden van risicofactoren voor atherosclerose,
- het aanleren van een toenemende mate van zelfstandigheid en zelfmanagement in de training en het onderhouden van een actieve leefstijl door de patiënt en
- het verbeteren van de kwaliteit van leven van de patiënt.
In de loop van de behandeling evalueert de fysiotherapeut deze doelstellingen op systematische wijze. Afhankelijk van de diagnostische bevindingen kan de behandeling gericht zijn op:
- het geven van informatie en voorlichting ter bevordering van het ziekte-inzicht van de patiënt;
- het verbeteren van het (subjectieve en objectieve) inspanningsvermogen van de patiënt:
- het optimaliseren van de activiteiten en participatie van de patiënt;
- het ondersteunen van de patiënt op het gebied van cardio-vasculair risicomanagement.
C.1 Informatie en voorlichting ter bevordering van het ziekte-inzicht van de patiënt
Het wordt aanbevolen een persoonlijk voorlichtingsplan op te stellen, dat is gebaseerd op de behoefte aan informatie, adviezen en begeleiding die tijdens het diagnostisch proces in kaart zijn gebracht.
Voorlichting geven en (mede daardoor) therapietrouw bevorderen zijn belangrijke onderdelen in de behandeling van patiënten met sPAV. Het geven van goede en adequate voorlichting vormt de basis voor de inzet en medewerking van de patiënt en het bereiken van gedragsverandering. Gedragsverandering speelt een belangrijke rol in het verminderen van de risicofactoren voor atherosclerose en is noodzakelijk om inspanningsbeperkingen te verminderen en het looppatroon te verbeteren. Voorlichting is een proces, waarbij de gedragsverandering de eindstap is. Deze eindstap is niet mogelijk als de voorgaande stappen niet zijn gezet. Daarom is het geven van informatie en voorlichting als apart onderdeel van de behandeling geformuleerd. Een voorbeeld van een voorlichtingsplan voor patiënten met sPAV is opgenomen in bijlage 4 (opent in nieuw tabblad).
De behoefte van de patiënt aan informatie en voorlichting die tijdens het diagnostisch proces in kaart is gebracht, vormt het uitgangspunt voor het individueel opgestelde voorlichtingsplan. Tijdens de behandeling informeert en adviseert de fysiotherapeut de patiënt en biedt hij steun (begeleiding). Hierbij kan de fysiotherapeut gebruikmaken van motiverende gespreksvoering (motivational interviewing). Deze persoonsgerichte gespreksstijl is gericht op het bevorderen van veranderingen in het gewoontegedrag door het verduidelijken en oplossen van ambivalentie ten opzichte van verandering. De relatie tussen de hulpverlener en de patiënt is gericht op samenwerking, eigen verantwoordelijkheid en vrijheid van gedragskeuze, met als doel de patiënt te motiveren voor verandering. Patiënt en hulpverlener vervullen een gelijkwaardige rol, zij behandelen elkaar respectvol en het gesprek is vraaggestuurd (shared decisionmaking).
Bij het geven van voorlichting kan gebruik worden gemaakt van bestaand voorlichtingsmateriaal, zoals brochures en online (video)materiaal (bijvoorbeeld van De Hart&Vaatgroep, de Nederlandse Hartstichting, ClaudicatioNet (opent in nieuw tabblad), www.etalagebenen.nl en naar de patiënteninformatie op de site van het Nederlands Huisartsen Genootschap, www.thuisarts.nl).
Voorlichting geven en (mede daardoor) therapietrouw bevorderen, zijn belangrijke onderdelen in de behandeling van patiënten met sPAV. Het geven van goede en adequate voorlichting vormt de basis voor de inzet en medewerking van de patiënt en het bereiken van een gedragsverandering. Gedragsverandering speelt een belangrijke rol in het verminderen van de risicofactoren voor atherosclerose en is noodzakelijk om inspanningsbeperkingen te verminderen en het looppatroon te verbeteren. Van der Burgt en Verhulst schreven een boek over patiëntenvoorlichting en compliancebevordering door paramedici, Doen en blijven doen. Daarin werken zij een voorlich- tingsmodel uit dat bestaat uit zes stappen.79 Per stap wordt aan- dacht besteed aan de problemen die de patiënt ervaart. Een voorlichtingsplan voor patiënten met PAV is opgenomen in bijlage 4 (opent in nieuw tabblad) van de Praktijkrichtlijn. De laatste stap in het voorlichtingsmodel betreft de gedragsverandering. De bereidheid om van gedrag te veranderen, wordt bepaald door een samenspel tussen de attitude van de patiënt zelf (hoe denkt de patiënt over de gedragsverandering?), sociale invloeden (hoe kijken anderen tegen de gedragsverandering aan?), verwachte uitkomsten en eigen-effectiviteit van de patiënt (zal het lukken om het gedrag te veranderen?).79,80
Er dient voortdurend rekening te worden gehouden met:
- ‘locus of control’: in welke mate denkt de patiënt invloed uit te kunnen oefenen op zijn situatie?
- attributie: waaraan schrijft de patiënt de invloeden op zijn levensloop toe?
- wijze van coping: hoe gaat de patiënt om met gebeurtenissen?
- (emotionele) gesteldheid van de patiënt.
De behoefte aan informatie en voorlichting die tijdens het diagnostisch proces in kaart is gebracht, vormt het uitgangspunt voor het individueel opgestelde voorlichtingsplan. De werkgroep beveelt een voorlichtingsplan aan als hulpmiddel bij het systematisch aanbieden van alle noodzakelijke informatie, zonder de patiënt te overvoeren. Tijdens de behandeling informeert en adviseert de fysiotherapeut de patiënt en biedt hij steun (begeleiding). Hierbij kan de fysiotherapeut gebruikmaken van motiverende gespreksvoering (motivational interviewing). Deze persoonsgerichte gespreksstijl is gericht op het bevorderen van veranderingen in het gewoontegedrag door het verduidelijken en oplossen van ambivalentie ten opzichte van verandering. De relatie tussen de hulpverlener en de patiënt is gericht op samenwerking, eigen verantwoordelijkheid en vrijheid van gedragskeuze, met als doel de patiënt te motiveren voor verandering. Patiënt en hulpverlener vervullen een gelijkwaardige rol, zij behandelen elkaar respectvol en het gesprek is vraaggestuurd (shared decision making).
Bij het geven van voorlichting kan gebruik worden gemaakt van bestaand voorlichtingsmateriaal, zoals brochures en online (video)materiaal (bijvoorbeeld van De Hart&Vaatgroep, de Nederlandse Hartstichting, ClaudicatioNet (opent in nieuw tabblad), www.etalagebenen.nl en Thuisarts.nl, waar de patiënteninformatie van het Nederlands Huisartsen Genootschap staat).
C.2 Verbeteren van het (objectieve en subjectieve) inspanningsvermogen
Het inspanningsvermogen kan worden verbeterd door:
- het vergroten van de functionele loopafstand;
- het vergroten van het aeroob uithoudingsvermogen;
- het leren omgaan met de klachten door:
- het verhogen van de pijntolerantie en
- het overwinnen van angst voor inspanning.
C.2.1 Vergroten van de functionele loopafstand
Het hoofddoel van oefentherapie bij patiënten met sPAV is het vergroten van de functionele loopafstand. Oefentherapie, veelal looptraining, is een effectief en veilig middel om de loopafstand(en) bij patiënten met sPAV te vergroten. De beste resultaten worden gezien indien looptrainingen (veelal op een loopband) bij aanvang twee tot drie keer per week in trainingssessies van minimaal 30 minuten worden uitgevoerd, afbouwend naar steeds meer zelfstandig oefenen, gedurende minimaal twee tot zes maanden, waarbij training plaatsvindt onder begeleiding van een fysiotherapeut. Er bestaat nog geen eenduidig bewijs voor de intensiteit van het trainingsprogramma. Zowel trainen tot de pijn begint als trainen tot bijna maximale pijn lijken te resulteren in een verbetering van de loopafstanden.
Verbeteren van het looppatroon bij het vergroten van de functionele loopafstand
Bij patiënten met sPAV treden specifieke veranderingen op in het looppatroon om de pijnklachten te verminderen of te voorkomen. Wanneer patiënten al gedurende lange tijd klachten hebben, zullen de veranderingen in het looppatroon niet zonder meer verdwijnen. Zelfs na behandelingen die leiden tot een verbeterde doorbloeding zoals vaatchirurgie of ‘dotteren’, kan het veranderde looppatroon in stand blijven.
Het is onvoldoende duidelijk of oefentherapie een bijdrage kan leveren aan het verbeteren van het looppatroon. De fysiotherapeut bespreekt met de patiënt de behoefte om tijdens de behandeling aandacht te besteden aan het verbeteren van het looppatroon.
Aanpassen van het oefenprogramma op basis van comorbiditeit
De behandelaar bepaalt welke aanpassingen in de generieke oefenprogramma’s nodig zijn om te komen tot een adequaat oefenprogramma, waarin voldoende rekening gehouden wordt met de comorbiditeit van de patiënt, of wint advies in bij collegae of specialisten op het gebied van de betreffende aandoening. Indien de comorbiditeit in kwestie de behandeling dusdanig beïnvloedt dat fysiotherapie geen kans van slagen heeft, is overleg met de verwijzer aangewezen.
Veel voorkomende comorbiditeiten bij patiënten met sPAV zijn hartaandoeningen, cerebrovasculair accident (CVA), diabetes mellitus, obesitas, chronisch obstructieve longziekten (COPD) en mobiliteitsbeperkende aandoeningen zoals artrose en reuma. Van de behandelaar wordt bij de behandeling van patiënten met sPAV deskundigheid verwacht op het gebied van deze aandoeningen.
Op basis van bovenstaande formuleerde de werkgroep de volgende samenvattende aanbevelingen
(5) Training
Het is sterk aan te bevelen om patiënten met sPAV te behandelen met oefentherapie ter vergroting van de loopafstand. Deze oefentherapie kan bestaan uit alleen lopen/wandelen, actieve (been)oefeningen of fysieke training of loopbandtraining, eventueel in combinatie met spierversterking.
(6) Looptraining
Ter vergroting van de functionele loopafstand geniet looptraining de voorkeur in de behandeling van patiënten met sPAV. Indien lopen te belastend is voor de patiënt, kunnen met name bij aanvang van de behandeling andere belastingsvormen, zoals fietsen, een alternatief vormen.
(7) Duur van het trainingsprogramma
De werkgroep adviseert om patiënten met sPAV gedurende ten minste zes maanden te trainen.
(8) Trainingsintensiteit
Er kan geen aanbeveling worden geformuleerd betreffende de intensiteit van de training. Zowel trainingsprogramma’s met een lage als een hoge intensiteit lijken te leiden tot een toename van de loopafstand.
(9) Trainingsfrequentie
De werkgroep adviseert om de training bij patiënten met sPAV drie keer per week uit te voeren.
(10) Trainingsduur
De werkgroep adviseert een trainingsduur van ten minste 30 minuten per trainingssessie om tot een zo groot mogelijke verbetering van de loopafstand te komen.
(11) Begeleiden van de trainingsprogramma’s
Ter vergroting van de loopafstand bij patiënten met sPAV genieten begeleide trainingsprogramma’s sterk de voorkeur. Er kan nog geen advies worden gegeven over het optimale aantal trainingssessies dat begeleid moet worden.
(12) Verbeteren van het looppatroon
Er kan geen aanbeveling worden geformuleerd over het toepassen van oefentherapie bij patiënten met sPAV ter verbetering van het looppatroon.
(13) De invloed van comorbiditeit
De werkgroep is van mening dat oefentherapie ook bij sPAV-patiënten met comorbiditeiten aangewezen kan zijn. De fysiotherapeut stelt het oefenprogramma zodanig samen dat er voldoende rekening gehouden wordt met de aanwezige comorbiditeit. Indien de comorbiditeit van de patiënt de behandeling dusdanig beïnvloedt dat fysiotherapie geen kans van slagen heeft, is overleg met de verwijzer aangewezen.
Het hoofddoel van oefentherapie bij patiënten met sPAV is het vergroten van de functionele loopafstand. In de literatuur wordt echter meestal het effect van therapie op de pijnvrije en maximale loopafstand beschreven. Vandaar dat de bewijsvoering vooral betrekking heeft op deze loopafstanden.
De effectiviteit van oefentherapie bij patiënten met sPAV is onderzocht in meerdere systematische reviews. Oefentherapie, veelal looptraining, is een bewezen effectief en veilig middel om de loopafstand(en) bij patiënten met sPAV te vergroten.5,81-88 De trainingsprogramma’s in de meeste studies varieerden van alleen lopen/wandelen, actieve (been)oefeningen of fysieke training en combinaties hiervan, tot loopbandtraining, eventueel in combinatie met spierversterking.
Watson et al. includeerden in hun Cochrane review 22 studies met in totaal rond de 1200 mannen en vrouwen met stabiele sPAV.81 De follow-upperiode varieerde van twee weken tot twee jaar. Hoewel in de verschillende studies diverse vormen van oefentherapie werden toegepast (variërend van krachttraining tot ‘nordic walking’ en arm- en beenoefeningen), was de aanbeveling van alle onderzoekers om minimaal twee keer per week te oefenen, waarbij de voorkeur uitging naar oefenen onder supervisie.
Oefentherapie leidde tot een significante verbetering van de pijnvrije en maximale looptijden en -afstanden in vergelijking met de gangbare of placebobehandeling.81 De pijnvrije loopafstand was na oefentherapie gemiddeld 82,19 m (95%-BI = 71,73-92,65) groter dan na de standaard- of placebobehandeling. Het verschil in de gemiddelde maximale loopafstanden tussen de groepen bedroeg 113,20 m (95%-BI = 94,96-131,43).
Daarnaast werd in de review van Watson et al. een vergelijking gemaakt tussen verschillende therapievormen bij patiënten met sPAV.81 Omdat in deze review maar zeer weinig studies waren geïncludeerd, met ook nog eens weinig onderzoekspersonen, was er onvoldoende bewijs om een uitspraak te doen over de effecten van oefentherapie in vergelijking met een operatieve behandeling, angioplastiek of behandeling met antistollingsmedicatie. Hoewel de pijnvrije en maximale loopafstanden meer leken te verbeteren met angioplastiek dan met oefentherapie op de korte termijn (zes maanden), blijft dit effect waarschijnlijk niet behouden op de langere termijn. Na één jaar leek oefentherapie tot significante verbeteringen te leiden vergeleken met angioplastiek.81
In twee randomized controlled trials (RCT’s) werd het effect van oefentherapie vergeleken met dat van een operatieve behandeling op de maximale loopafstand en looptijd.89,90 In de studie van Lundgren et al. werden drie groepen met elkaar vergeleken: alleen een operatieve behandeling, alleen oefentherapie en een combinatie van een operatieve behandeling en oefentherapie.89 Een operatieve behandeling bleek tot een grotere toename in de loopafstand te leiden dan oefentherapie, maar de grootste toename in de loopafstand werd gevonden in de gecombineerde groep.89 De verschillen tussen de groepen waren echter niet statistisch significant. Een operatieve behandeling bleek daarnaast tot een grotere verbetering van de enkel-armindex te leiden dan oefentherapie.89 Gelin et al. vonden dat een operatieve behandeling tot een significant grotere toename in de maximale loopafstand leidde in vergelijking met oefentherapie na één jaar.90 Een probleem in de groep die oefentherapie ontving, was de geringe therapietrouw.90 Hoewel een operatieve behandeling op kortere termijn al resultaat geeft, brengt een operatie ook een verhoogd risico op complicaties met zich mee.81
In een beschrijvende review van Stewart et al. werden 15 studies opgenomen die het effect van looptraining vergeleken met placebobehandeling, angioplastiek of medicatie.82 Ondanks verschillen in het trainingsprogramma toonden alle studies een verbetering van de loopafstand of -tijd aan door looptraining.
In een review van Frans et al. werd het effect van (gesuperviseerde) oefentherapie vergeleken met het effect van een angioplastiek.91 Drie studies die waren geïncludeerd in deze review vergeleken het verschil in effect tussen gesuperviseerde oefentherapie en angioplastiek bij arteriële obstructies in de arteria femoralis en/of arteria poplitea. Gesuperviseerde oefentherapie in combinatie met angioplastiek leidde tot de grootste toename in de maximale en pijnvrije loopafstanden en de enkel-armindex.91 De vergelijking tussen alleen gesuperviseerde oefentherapie en alleen angioplastiek toonde ofwel geen verschil aan, ofwel een verschil in het voordeel van de angioplastiek.91 Alle behandelingen leidden tot eenzelfde significante verbetering van de kwaliteit van leven.91 In vijf studies uit deze review werd geen onderscheid gemaakt in de lokalisatie van de arteriële obstructie. Op basis van deze studies bleek een combinatie van angioplastiek en gesuperviseerde looptherapie tot een grotere toename in de maximale loopafstand te leiden dan een angioplastiek alleen.91 De vergelijking tussen angioplastiek en gesuperviseerde oefentherapie leverde inconsistente resultaten op: de ene studie concludeerde dat gesuperviseerde looptherapie een positief effect had op de maximale en pijnvrije loopafstand, en dat angioplastiek een positief effect had op de enkel-armindex, terwijl de andere studie geen significante verschillen vond tussen de groepen.91 Op basis van de resultaten van deze review lijkt een combinatie van gesuperviseerde oefentherapie en angioplastiek de beste resultaten te geven, maar hiervoor is nog onvoldoende bewijs voorhanden.
Murphy et al. vergeleken in hun RCT het effect van medicatie, gesuperviseerde oefentherapie en angioplastiek met stentplaatsing op de verandering in de maximale looptijd bij patiënten met sPAV op basis van een arteriële obstructie in de aorta of arteria iliaca.92 Na zes maanden leidde gesuperviseerde looptherapie tot de grootste toename in de maximale looptijd. Medicatie had het minste effect op de looptijd.92
De fysiologische effecten van looptraining die het fysieke prestatievermogen bij patiënten kunnen verbeteren zijn: een toename en effectievere verdeling van de bloedstroom, een efficiënter gebruik van de aerobe energievoorziening vanwege een toename van oxidatieve enzymen, een geringere afhankelijkheid van de anaerobe energievoorziening en een verbetering van de reologische eigenschappen van het bloed (afname van de viscositeit).22,49,81,93,94 Een vergroting van de efficiëntie van het lopen draagt bij aan een verbetering van de loopprestaties, waaronder een vergroting van de loopafstand.22
Tijdens het trainen is de fysiotherapeut alert op tekenen van cardiale overbelasting, zoals angina pectoris, eventueel met uitstraling naar de (linker)arm, ernstige vermoeidheid of kortademigheid die niet in relatie staat tot de geleverde inspanning, flauwvallen, duizeligheid en/of vegetatieve reacties (transpiratie, bleekheid)45 en pijn in de benen zonder vasculaire oorzaak.49 Indien deze klachten optreden, zal de fysiotherapeut de trainingsbelasting, indien nodig, aanpassen.
Oefentherapie kan tevens bijdragen aan een verbetering van de kwaliteit van leven van patiënten met sPAV.87,95,96 Positieve effecten werden met name gevonden op het onderdeel fysiek functioneren (voornamelijk gemeten met de Short Form General Health Survey: de SF-36 en de SF-20).87,95,96 Enkele studies toonden aan dat oefentherapie tevens gunstige effecten heeft op andere aspecten van de kwaliteit van leven, zoals lichamelijke pijn, vitaliteit en algemene gezondheid.95,96
Conclusie
Training (niveau 1)
- Het is aangetoond dat oefentherapie, variërend van alleen lopen/wandelen, actieve (been)oefeningen of fysieke training en combinaties hiervan, tot loopbandtraining eventueel in combinatie met spierversterking, een effectieve behandeling is bij patiënten met sPAV. Oefentherapie leidt tot een significante toename van de pijnvrije en maximale loopafstand. Kwaliteit van de gevonden artikelen: A (Bendermacher et al., 200688, Robeer et al., 199885, Watson et al., 200881), B (Fakhry et al., 201284, Gardner et al., 199586, Kruidenier et al., 201287 en Wind et al., 200783).
Belastingsvorm bij het vergroten van de functionele loopafstand
Looptraining, veelal op een loopband uitgevoerd, geeft de beste resultaten in het vergroten van de pijnvrije en maximale loopafstand.86,97,98
Parmenter et al. vergeleken in hun review het effect van verschillende belastingsvormen op de pijnvrije en maximale loopafstand.98 De meeste bewegingsactiviteiten, zoals aerobe oefentherapie van de onderste extremiteiten, fietsen, ‘nordic walking’ en een combinatie van armfietsen en fietsen/lopen, leidden tot een toename in de pijnvrije en maximale loopafstand.98Looptherapie waarbij geen pijn optreedt, leidde in dit onderzoek tot de grootste verbetering in de pijnvrije loopafstand. De grootste verbetering in de maximale loopafstand werd gevonden bij aerobe oefentherapie voor de onderste extremiteiten (bestaande uit een combinatie van oefeningen gericht op spierkracht en uithoudingsvermogen).98
In de review van Gardner et al. bleken programma’s waarin alleen werd gelopen effectiever te zijn dan programma’s die bestonden uit een combinatie van trainingen.86 De belastingsvorm (lopen) was de op twee na belangrijkste trainingsvariabele.86
Conclusie
Looptraining (niveau 2)
- Het is aannemelijk dat looptraining de effectiefste manier van trainen is bij patiënten met sPAV.
- Looptraining leidt tot een significante toename van de pijnvrije en maximale loopafstand. Kwaliteit van de gevonden artikelen: B (Bulmer et al., 200497, Gardner et al., 199586 en Parmenter et al., 201198).
Overige overwegingen
Het lopen (op een loopband met helling) kan een erg belastende activiteit zijn voor patiënten met sPAV. Belastende oefeningen kunnen vooral bij aanvang van de therapie minder goed worden getolereerd. Wanneer de cardiale belastbaarheid van de patiënt het toelaat, kunnen andere belastingsvormen een alternatief vormen. Zo kunnen tijdens de warming-up minder belastende oefeningen of activiteiten worden gebruikt, zoals oefeningen waarbij het lichaamsgewicht niet gedragen hoeft te worden, denk aan fietsen.49
De toename van de (pijnvrije) loopafstand wordt in belangrijke mate toegeschreven aan lokale adaptaties, zoals een toename van de collaterale flow, een redistributie van de aanwezige flow en metabole aanpassingen van de spiervezels, waardoor de afhankelijkheid van het anaerobe metabolisme afneemt.49
Er is nog niet voldoende bewijs voor het effect van oefentherapie om deze behandeling in de richtlijn aan te bevelen. Vanwege de matige kwaliteit van de studies die zijn opgenomen in de review van Parmenter et al. en het beperkte aantal studies, is er meer onderzoek (RCT’s) nodig.
Duur van het trainingsprogramma bij het vergroten van de functionele loopafstand
In een studie van Gardner et al. namen de pijnvrije en maximale looptijden vooral toe in de eerste twee maanden van de gesuperviseerde looptraining.99 Deze verbeteringen bleven tot vier maanden na het trainingsprogramma behouden, maar er trad geen verdere verbetering van de pijnvrije en maximale looptijd op. Uit de review van Bulmer et al. blijkt dat de verbeteringen in de pijnvrije en maximale loopvaardigheden (looptijd en/of -afstand) afvlakken wanneer een trainingsprogramma langer dan 17 weken duurt.97 Het maximale effect van het trainingsprogramma leek bereikt te worden bij programma’s van 12 tot 24 weken. Dit is in tegenspraak met oudere literatuur waarin Gardner et al. de grootste verbeteringen in loopafstand zagen bij een trainingsprogramma van meer dan zes maanden.86 In deze studie was de lengte van het programma de op een na belangrijkste trainingsvariabele.86 Fakhry et al. vonden echter dat geen van de onderzochte trainingsvariabelen, waaronder duur van het programma, van invloed waren op de toename in de maximale en pijnvrije loopafstanden.84
Conclusie
Duur van het trainingsprogramma (niveau 2)
- Het is aannemelijk dat de grootste effecten in toename van de loopafstand optreden gedurende de eerste zes maanden van de training. Kwaliteit van de gevonden artikelen: B (Bulmer et al., 200497, Gardner et al., 201299 en 199586).
Intensiteit van de belasting bij het vergroten van de functionele loopafstand
Ter vergroting van de loopafstand zijn bij patiënten met sPAV belastende oefeningen (bijvoorbeeld lopen) het effectiefst. De intensiteit van de belasting wordt voornamelijk gedoseerd aan de hand van de pijnscore. Looptraining tot bijna maximale pijn kan worden gegeven in intervalvorm, waarbij volledig herstel in de rustperiodes toegestaan kan worden. Bij trainingsvormen met belasting van de kuitmusculatuur wordt gelopen tot een score van drie op een ACSM-vierpuntsschaal.49 Naast de pijnscore kan men ook gebruikmaken van andere parameters, zoals de Borg-score, de zuurstofopname en de hartfrequentie.
Volgens Gardner et al. was de trainingsintensiteit (trainen tot aanvang van de pijn ten opzichte van trainen tot bijna maximale pijn) de belangrijkste trainingsvariabele.86 Fakhry et al. daarentegen vonden dat geen van de onderzochte trainingsvariabelen, waaronder het eindpunt van de training op basis van de ervaren pijn, van invloed waren op de toename in de maximale en pijnvrije loopafstanden.84 Ook uit de review van Parmenter et al. bleek dat zowel trainen tot aanvang van de pijn als tot bijna maximale pijn leidde tot een significante toename van de pijnvrije en maximale loopafstanden en -tijden.98 Deze resultaten komen overeen met die uit een studie van Gardner et al. Deze onderzoekers vergeleken het resultaat van een programma met een lage trainingsintensiteit (40% van de maximale belasting, vastgesteld met een maximale inspanningstest met toenemende belasting: loopsnelheid 3,2 km/uur, verhoging hellingshoek met 2% elke twee minuten) met een programma met een hoge trainingsintensiteit (80% van de maximale belasting).100 Beide programma’s, met gesuperviseerde loopbandtraining tot bijna maximale pijn, drie dagen per week gedurende zes maanden, resulteerden in vergelijkbare toenames in de pijnvrije en maximale loopafstand.100 Daarnaast leidden beide programma’s tot verbeteringen in de VO2max en kwaliteit van leven.100
Conclusie
Trainingsintensiteit (niveau 2)
- Het is aannemelijk dat zowel trainingsprogramma’s met een lage als met een hoge intensiteit effectief zijn ter verbetering van de loopafstand.
Kwaliteit van de gevonden artikelen: B (Gardner et al., 2005100, Gardner et al., 199586 en Parmenter et al., 201198).
Trainingsfrequentie bij het vergroten van de functionele loopafstand
Trainingen die drie keer per week worden uitgevoerd, leiden tot een grotere toename van de (pijnvrije en maximale) loopafstand in vergelijking met trainingen met lagere trainingsfrequenties.81,86,97 In de review van Bulmer et al. werden de resultaten van 22 studies met elkaar vergeleken. Trainingen die drie keer per week werden uitgevoerd leidden tot een toename in de maximale loopafstand variërend van 64 tot 165%.97 Studies met trainingsprogramma’s waarbij vaker dan drie keer per week werd getraind, beschreven een kleinere toename in de maximale loopafstand (variërend van 44 tot 99%).
Conclusie
Trainingsfrequentie (niveau 2)
- Het is aannemelijk dat training bij patiënten met sPAV het effectiefst is als de training drie keer per week wordt uitgevoerd.
Kwaliteit van de gevonden artikelen: B (Bulmer et al., 200497 en Gardner et al., 199586).
Trainingsduur bij het vergroten van de functionele loopafstand
Een trainingsduur van ten minste 30 minuten per trainingssessie leidt tot een verbetering van de pijnvrije en maximale loopafstand.81,86,97
Conclusie
Trainingsduur (niveau 2)
- Het is aannemelijk dat training bij patiënten met sPAV het effectiefst is als de trainingsduur per sessie ten minste 30 minuten bedraagt.
Kwaliteit van de gevonden artikelen: B (Bulmer et al., 200497 en Gardner et al., 199586).
Begeleid versus onbegeleid trainen bij het vergroten van de functionele loopafstand
In een review van Bendermacher et al. zijn de effecten van begeleid en onbegeleid trainen met elkaar vergeleken.88 De frequentie van de begeleide looptraining varieerde tussen de studies, maar bestond meestal uit drie oefensessies van 30 tot 60 minuten per week gedurende 12 weken. Patiënten in de onbegeleide trainingsgroep kregen het advies ten minste drie keer per week 20 tot 60 minuten te wandelen gedurende 12 weken. Op basis van acht studies waarin 319 mannen en vrouwen waren geïncludeerd, werd geconcludeerd dat gesuperviseerde looptraining een significante en klinisch relevante verbetering van de maximale loopafstand opleverde vergeleken met onbegeleide looptraining bij patiënten met claudicatio intermittens.88Het verschil in de maximale loopafstand na drie maanden bedroeg 150 m in het voordeel van begeleid trainen. Het gunstige effect van begeleid ten opzichte van onbegeleid trainen bestond zes, negen en 12 maanden na de looptraining nog steeds.88 Ook het effect van gesuperviseerde looptraining op de pijnvrije loopafstand was na drie en zes maanden groter dan na onbegeleide looptraining, hoewel na 12 maanden geen significant verschil tussen de groepen meer werd gevonden.88 Ook uit de meta-analyse van Kruidenier et al. bleek gesuperviseerde oefentherapie (begeleid door een verpleegkundige of fysiotherapeut) te leiden tot een grotere toename van de pijnvrije en maximale loopafstand in vergelijking met niet-gesuperviseerde oefentherapie.87 Daarnaast was er geen verschil in effect op de kwaliteit van leven tussen begeleid en onbegeleid trainen.87
Het positieve effect van gesuperviseerde oefentherapie op de loopafstand werd ook gevonden in een RCT van Nicolaï et al.101 Gesuperviseerde oefentherapie door een fysiotherapeut leidde tot een grotere toename van zowel de maximale als de functionele loopafstand in vergelijking met het advies om drie keer per dag te trainen tot maximale pijn.
Ook voor het verbeteren van de kwaliteit van leven en de scores op de Walking Impairment Questionnaire (WIQ) bleek bij patiënten met claudicatio intermittens gesuperviseerde oefentherapie effectiever te zijn dan het advies om drie keer per dag te trainen tot maximale pijn.101 Het geven van extra feedback op basis van een accelerometer die de patiënt dagelijks droeg, in aanvulling op de gesuperviseerde oefentherapie, bleek niet bij te dragen aan een verdere verbetering van de loopafstanden, de scores op de WIQ en de kwaliteit van leven.101
Gesuperviseerde looptherapie in een regionale setting bleek net zo effectief als gesuperviseerde looptherapie in een klinische setting.102 Over de optimale mate van begeleiding en het aantal trainingssessies dat begeleid moet worden, is nog onvoldoende informatie beschikbaar.
Conclusie
Begeleiden van de trainingsprogramma’s (niveau 1)
- Het is aangetoond dat begeleide trainingsprogramma’s effectiever zijn dan onbegeleide trainingsprogramma’s bij het vergroten van de pijnvrije, functionele en maximale loopafstanden bij patiënten met sPAV.
Kwaliteit gevonden artikelen: A1 (Bendermacher et al., 200688), B (Kruidenier et al., 201287 en Nicolaï et al., 2010101).
Verbeteren van het looppatroon bij het vergroten van de functionele loopafstand
Bij patiënten met sPAV treden specifieke veranderingen op in het looppatroon om de klachten te verminderen of te voorkomen. Deze compensatiemechanismen zullen niet zonder meer verdwijnen door een training die uitsluitend gericht is op een vergroting van de loopafstand, zeker niet wanneer patiënten al gedurende lange tijd klachten hebben. Zelfs na behandelingen die leiden tot een verbeterde doorbloeding, zoals een dotterbehandeling of vaatchirurgie, handhaven patiënten soms het veranderde looppatroon.
Mogelijke doelen van specifieke oefentherapie zijn het verbeteren van de coördinatie en het verminderen van de compensatiemechanismen. In de studie van Wenkstetten-Holub et al. bleek de loopsnelheid te zijn toegenomen na gesuperviseerde oefentherapie gedurende zes maanden.103 Ook in de studie van Collins et al. nam de loopsnelheid toe na een zes maanden durend oefenprogramma voor thuis.104 Andere studies daarentegen vonden geen effecten van gesuperviseerde oefentherapie, variërend in duur van drie tot 12 maanden, op de (pijnvrije) loopsnelheid, afwikkeling van de voet (plantaire flexie), heupextensie en andere gangparameters, waaronder staplengte, stapfrequentie en duur van de standfase.105-107
De fysiotherapeut bespreekt met de patiënt of deze er behoefte aan heeft dat er tijdens de behandeling aandacht wordt besteed aan het verbeteren van het looppatroon.
Conclusie
Verbeteren van het looppatroon (niveau 2)
- Er is tegenstrijdig bewijs dat (gesuperviseerde) oefentherapie een bijdrage kan leveren aan het verbeteren van het looppatroon.
Kwaliteit van gevonden artikelen: B+ (Collins et al., 2011104), B- (Crowther et al., 2009106en Crowther et al., 2008107), C+ (Wenkstetten-Holub et al., 2012103) en C- (King et al., 2012105).
Aanpassen van het oefenprogramma op basis van comorbiditeit
Bij patiënten met sPAV komen in de regel veel comorbiditeiten voor. Het betreft met name hartaandoeningen, CVA, diabetes mellitus, obesitas, COPD en mobiliteitsbeperkende aandoeningen, zoals artrose en reuma. De fysiotherapeut moet over deskundigheid beschikken ten aanzien van deze aandoeningen.
Voor specifieke aanbevelingen met betrekking tot de fysiotherapeutische behandeling bij deze aandoeningen kan de fysiotherapeut de betreffende KNGF-richtlijnen raadplegen. De behandelaar bepaalt welke aanpassingen in de generieke oefenprogramma’s nodig zijn om te komen tot een adequaat oefenprogramma, waarin voldoende rekening gehouden wordt met de comorbiditeit van de patiënt, of wint advies in bij collegae of specialisten op het gebied van de betreffende aandoening.
Indien de comorbiditeit in kwestie de behandeling dusdanig beïnvloedt dat fysiotherapie geen kans van slagen heeft, is overleg met de verwijzer aangewezen. Ook wanneer de fysiotherapeut op basis van zijn ervaringen en vaardigheden merkt dat het trainingsresultaat minder is dan verwacht, kan hij de mogelijke invloed van de aandoeningen van de individuele patiënt in de rapportage aan de verwijzer vermelden.
Op basis van bovenstaande formuleerde de werkgroep de volgende samenvattende aanbevelingen
(5) Training
Het is sterk aan te bevelen om patiënten met sPAV te behandelen met oefentherapie ter vergroting van de loopafstand. Deze oefentherapie kan bestaan uit alleen lopen/wandelen, actieve (been)oefeningen of fysieke training of loopbandtraining, eventueel in combinatie met spierversterking.
(6) Looptraining
Ter vergroting van de functionele loopafstand geniet looptraining de voorkeur in de behandeling van patiënten met sPAV. Indien lopen te belastend is voor de patiënt, kunnen met name bij aanvang van de behandeling andere belastingsvormen, zoals fietsen, een alternatief vormen.
(7) Duur van het trainingsprogramma
De werkgroep adviseert om patiënten met sPAV gedurende ten minste zes maanden te trainen.
(8) Trainingsintensiteit
Er kan geen aanbeveling worden geformuleerd betreffende de intensiteit van de training. Zowel trainingsprogramma’s met een lage als een hoge intensiteit lijken te leiden tot een toename van de loopafstand.
(9) Trainingsfrequentie
De werkgroep adviseert om de training bij patiënten met sPAV drie keer per week uit te voeren.
(10) Trainingsduur
De werkgroep adviseert een trainingsduur van ten minste 30 minuten per trainingssessie om tot een zo groot mogelijke verbetering van de loopafstand te komen.
(11) Begeleiden van de trainingsprogramma’s
Ter vergroting van de loopafstand bij patiënten met sPAV genieten begeleide trainingsprogramma’s sterk de voorkeur. Er kan nog geen advies worden gegeven over het optimale aantal trainingssessies dat begeleid moet worden.
(12) Verbeteren van het looppatroon
Er kan geen aanbeveling worden geformuleerd over het toepassen van oefentherapie bij patiënten met sPAV ter verbetering van het looppatroon.
(13) De invloed van comorbiditeit
De werkgroep is van mening dat oefentherapie ook bij sPAV-patiënten met comorbiditeiten aangewezen kan zijn. De fysiotherapeut stelt het oefenprogramma zodanig samen dat er voldoende rekening gehouden wordt met de aanwezige comorbiditeit. Indien de comorbiditeit van de patiënt de behandeling dusdanig beïnvloedt dat fysiotherapie geen kans van slagen heeft, is overleg met de verwijzer aangewezen.
C.2.2 Vergroten van het aeroob uithoudingsvermogen
Een afname van het inspanningsvermogen kan bij patiënten met sPAV het gevolg zijn van de beperking van de arteriële doorbloeding van de musculatuur, die optreedt door de arteriële obstructie. Inactiviteit zal op den duur leiden tot een verdere afname van het aeroob uithoudingsvermogen. Looptraining kan bij patiënten met sPAV leiden tot een significante verbetering van het aeroob uithoudingsvermogen.
Naast het lopen zijn andere activiteiten waarbij grote spiergroepen actief zijn en dynamische contracties worden uitgevoerd, geschikt om het aeroob uithoudingsvermogen te trainen. Uiteraard dient de fysiotherapeut hierbij rekening te houden met de voorkeur van de patiënt. Naast de fysiotherapeutische behandeling is een activeringsprogramma voor patiënten een goede aanvulling voor het vergroten van het aeroob uithoudingsvermogen (zie bijlage 3 (opent in nieuw tabblad)).
Uit onderzoek is gebleken dat looptraining bij patiënten met sPAV kan leiden tot een significante toename van de VO2max.100,108-111 Een verbeterd aeroob uithoudingsvermogen leidt vervolgens tot een afname van de totale en cardiale sterfte, en afname van de morbiditeit.45,112Lopen is een functionele oefenvorm ter vergroting van het aeroob uithoudingsvermogen. Tijdens het lopen is de specifieke coördinatie van het lopen beter te oefenen. Naast het lopen zijn andere activiteiten waarbij grote spiergroepen actief zijn en dynamische contracties worden uitgevoerd, geschikt om het aeroob uithoudingsvermogen te trainen. Uiteraard dient de fysiotherapeut hierbij rekening te houden met de voorkeur van de patiënt. Naast de fysiotherapeutische behandeling is een activeringsprogramma (opent in nieuw tabblad) voor patiënten een goede aanvulling op de behandeling ter vergroting van het aeroob uithoudingsvermogen.
In deze Verantwoording en toelichting wordt niet uitgebreid stilgestaan bij de onderbouwing van adviezen voor de vergroting van het aeroob uithoudingsvermogen, omdat deze in de inspanningsfysiologische literatuur zijn beschreven.49,113,114
C.2.3 Het leren omgaan met de klachten
Het is goed om aan de psychische toestand van de patiënt aandacht te besteden. Het actief betrekken van de patiënt bij de behandeling en het ontmoeten van lotgenoten heeft een positief effect op de manier waarop de patiënt met de klachten omgaat. Bij patiënten die op inadequate wijze omgaan met klachten kan gebruikgemaakt worden van principes uit de gedragsgeoriënteerde revalidatie (zoals bij de hartrevalidatie). Centraal hierbij staan de gerichtheid op het gedrag en de situaties waarin dit gedrag zich voordoet, en niet zozeer op de onderliggende pathologie (stoornis).
Verhogen van de pijntolerantie
Niet elke patiënt zal op dezelfde manier met zijn klachten omgaan. Bij sommige patiënten zal pijn leiden tot vermindering van activiteiten. Bij de behandeling zal de fysiotherapeut patiënten leren om niet direct te stoppen als de pijn begint op te treden, maar om telkens iets verder ‘door de pijn heen te lopen’. Hierbij is het van belang dat de patiënt begrijpt dat deze aanpak nodig is om een verbetering te bewerkstelligen en accepteert dat de pijn een wezenlijk onderdeel van de training is. De pijn wordt hierbij gescoord op de ACSM-schaal voor pijn. Bij deze vorm van training zal de fysiotherapeut letten op tekenen van overbelasting.
Overwinnen van de angst voor inspanning
Bij het overwinnen van angst voor inspanning kan men gebruikmaken van methoden die ook in de hartrevalidatie worden gehanteerd. Hierbij leert de patiënt wat de normale inspanningsverschijnselen zijn en leert hij deze te herkennen. Het is hierbij aan te raden de patiënt te leren de subjectieve belasting te beoordelen met de Borg-schaal.
Bij de behandeling van patiënten met sPAV is het goed om aan de psychische toestand van de patiënt aandacht te besteden. Het actief betrekken van de patiënt bij de behandeling en het ontmoeten van lotgenoten kan al een positief effect hebben op de manier waarop de patiënt met de klachten omgaat. Bij patiënten die op inadequate wijze omgaan met klachten kan gebruik worden gemaakt van principes uit de gedragsgeoriënteerde revalidatie (zoals bij de hartrevalidatie). Centraal hierbij staan de gerichtheid op het gedrag en de situaties waarin dit gedrag zich voordoet, en niet zozeer op de onderliggende pathologie (stoornis). De patiënt leert tijdens de behandeling een adequate copingstijl te ontwikkelen in relatie tot sPAV. Binnen de gedragsgeoriënteerde behandeling wordt geprobeerd de omgeving (onder andere de partner, de werkgever) zoveel mogelijk bij de behandeling te betrekken. In deze richtlijn worden de gedragsgeoriënteerde principes niet nader besproken.
Ter vergroting van het subjectieve inspanningsvermogen kan de behandeling gericht worden op twee verschillende aspecten: het verhogen van de pijntolerantie en het overwinnen van angst voor inspanning.
Verhogen van de pijntolerantie
Niet elke patiënt zal op dezelfde manier met zijn klachten omgaan. Bij sommige patiënten zal pijn leiden tot een vermindering van activiteiten. Tijdens de behandeling zullen veel patiënten moeten leren om niet direct te stoppen als de pijn begint, maar om telkens iets verder ‘door de pijn heen te lopen’. Een dergelijke training is belastend voor de patiënt. Toch is deze klachtenprovocerende belasting nodig om verbetering te bewerkstelligen.
Bij deze vorm van training zal de fysiotherapeut letten op tekenen van overbelasting. Toename van de loopafstand draagt bij aan een verbeterde psychische toestand van de patiënt, doordat de patiënt minder participatieproblemen zal ondervinden.
Conclusie
Verhogen van de pijntolerantie (niveau 4)
- De werkgroep is van mening dat het verhogen van de pijntolerantie door de patiënt te leren telkens iets verder ‘door de pijn heen te lopen,’ een gunstig effect heeft op de maximale loopafstand.
Overwinnen van angst voor inspanning
Bij het overwinnen van angst voor inspanning adviseert de werkgroep gebruik te maken van de methoden die in de hartrevalidatie worden gehanteerd.45 Hierbij wordt het behandeldoel zo concreet mogelijk gemaakt, bijvoorbeeld: ‘de patiënt kan de lichaamsreacties juist interpreteren’ (volgens observaties fysiotherapeut), ‘de patiënt geeft aan zich meer bewust te zijn van de toestand van het eigen lichaam’, ‘de patiënt geeft tijdens een interview of op een vragenlijst aan minder of geen angst te ervaren in bepaalde situaties, bijvoorbeeld tijdens zware lichamelijke inspanning’.
Hierbij is belangrijk dat de patiënt zich veilig voelt. Een juiste interpretatie van de lichaamsreacties kan hieraan bijdragen. Dit kan bewerkstelligd worden door de normale verschijnselen van inspanning te leren kennen en bovendien vroegtijdig de verschijnselen van cardiale overbelasting te leren onderkennen. Het is verstandig om patiënten de subjectieve belasting te leren beoordelen met behulp van de Borgschaal (opent in nieuw tabblad). De meeste patiënten leren in vijf bijeenkomsten de Borgschaal te gebruiken.115 Naast de fysiotherapeutische behandeling is het volgen van het eerder genoemde activeringsprogramma belangrijk voor het vergroten van het subjectieve inspanningsvermogen.
Conclusie
Overwinnen van angst voor inspanning (niveau 4)
- De werkgroep is van mening dat het overwinnen van angst voor inspanning bijdraagt aan een vermindering van de subjectieve inspanningsbeperking.
C.3 Optimaliseren van activiteiten en participatie
Indien de patiënt problemen ondervindt met specifieke functionele vaardigheden, dienen deze expliciet geoefend te worden.
Uit de anamnese en het functieonderzoek kan naar voren komen dat de patiënt problemen ondervindt met specifieke functionele vaardigheden, zoals traplopen of op één been staan. Deze vaardigheden moeten specifiek worden getraind op een zo functioneel mogelijke manier. Het betreft hier oefentherapie die bij voorkeur wordt uitgevoerd onder begeleiding van een fysiotherapeut. Bij de uitvoering van de therapie wordt rekening gehouden met de individuele situatie van de patiënt, onder andere diens belastbaarheid, kracht, coördinatie, balans/evenwicht en medicijngebruik. In deze richtlijn wordt de invulling van deze oefentherapie niet nader besproken. Deze wordt bekend verondersteld bij de fysiotherapeut.
C.4 Ondersteuning bieden op het gebied van cardiovasculair risicomanagement
Ten aanzien van het aanleren en behouden van een gezonde leefstijl om het risico op het ontwikkelen van (andere) hart- en vaatziekten te verminderen, kunnen de volgende subdoelen geformuleerd worden:
- ontwikkelen en onderhouden van een lichamelijk actieve leefstijl;
- stoppen met roken;
- ontwikkelen van een gezond voedingspatroon;
- bevorderen van therapietrouw aan voorgeschreven medicatie.
Hierbij kan de fysiotherapeut, indien gewenst, samenwerken met andere zorgverleners en de patiënt indien nodig doorverwijzen.
Patiënten met sPAV hebben een verhoogd risico op het ontwikkelen van (andere) hart- en vaatziekten.5 Het aanleren en behouden van een gezonde leefstijl kan dit risico verminderen. Naast oefentherapie is het daarom belangrijk aandacht te besteden aan een gezonde leefstijl, zoals ook wordt aanbevolen door Nederlandse vaatchirurgen.116 Conform de aanpak binnen de hartrevalidatie kunnen de volgende subdoelen geformuleerd worden: ontwikkelen en onderhouden van een lichamelijk actieve leefstijl, stoppen met roken, ontwikkelen van een gezond voedingspatroon en bevorderen van therapietrouw aan voorgeschreven medicatie.45,52
C.4.1 Ontwikkelen en behouden van een actieve leefstijl
Het stimuleren van de patiënt om een actieve leefstijl te ontwikkelen en vervolgens te leren hoe deze te onderhouden, is een belangrijk aspect van de behandeling door de fysiotherapeut, met als doel het resultaat van de behandeling te behouden en de risicofactoren voor atherosclerose positief te beïnvloeden. Doel hierbij is de patiënt (minimaal) te laten voldoen aan de Nederlandse Norm Gezond Bewegen (NNGB). Desalniettemin is het goed de patiënt erop te wijzen dat elke bewegingsactiviteit een bijdrage levert.
Indien patiënten (bij aanvang van de therapie) de vereiste belastingsduur en -omvang door middel van wandelen niet kunnen volbrengen, kunnen deze patiënten naast looptraining ook andere vormen van inspanning uitvoeren die beter worden getolereerd, zoals fietsen of roeien. Indien gewenst kunnen bij toename van de loopafstand de andere inspanningsvormen geleidelijk worden afgebouwd en de omvang van het lopen geleidelijk worden opgevoerd.
De fysiotherapeut stimuleert de patiënt om na afloop van de behandelperiode zelf actief te blijven en de gezonde leefgewoonten te continueren. Beweging maakt hiervan een belangrijk onderdeel uit. Op basis van het trainingsprogramma voor thuis zal de patiënt uiteindelijk de bewegingsactiviteiten zelfstandig, dat wil zeggen zonder fysiotherapeutische begeleiding, op een verantwoorde wijze moeten kunnen (en durven) uitvoeren.
De fysiotherapeutische begeleiding wordt teruggebracht als de behandeldoelen bereikt zijn, wanneer de patiënt de doelen verder zelfstandig kan bereiken of wanneer de patiënt, in overleg met de fysiotherapeut, geen baat meer verwacht van de behandeling.
Op de lange termijn zijn beweegvormen die leuk zijn en in groepsverband worden uitgevoerd gemakkelijker vol te houden. Indien voorhanden wijst de fysiotherapeut de patiënt op locoregionale beweeg- en activiteitenprogramma’s (bijvoorbeeld sportief wandelen, medische fitnessprogramma’s en Hart in Beweging), die de patiënt kunnen motiveren om zijn actieve leefstijl te onderhouden op basis van zelfmanagement.
Het stimuleren van de patiënt om een actieve leefstijl te ontwikkelen en vervolgens te leren hoe deze te onderhouden, is een belangrijk aspect van de behandeling, met als doel het resultaat van de behandeling te behouden en de risicofactoren voor atherosclerose positief te beïnvloeden. Doel hierbij is de patiënt te laten voldoen aan de NNGB.53 Desalniettemin is het goed de patiënt erop te wijzen dat elke bewegingsactiviteit een bijdrage levert.
Izquierdo-Porera et al. vonden dat looptraining bij patiënten met sPAV niet alleen tot functionele prestatieverbeteringen leidde, maar ook risicofactoren voor hart- en vaatziekten positief beïnvloedde.108 Zo trad er door looptraining een verbetering op van het LDL-cholesterolgehalte (8%), het totaal cholesterolgehalte (5%) en de systolische bloeddruk (6%). De training duurde zes maanden en bestond uit lopen op een loopband tot bijna maximale pijn (score drie op de ACSM-schaal voor pijn (opent in nieuw tabblad)). Zowel de duur als de intensiteit werden in de loop van het programma progressief verhoogd.
Veel patiënten met sPAV zullen (bij aanvang van de therapie) de vereiste belastingsduur en -omvang door middel van wandelen niet kunnen volbrengen. Deze patiënten kunnen naast looptraining ook andere vormen van inspanning uitvoeren die beter worden getolereerd, bijvoorbeeld fietsen of roeien. Indien gewenst kunnen bij toename van de loopafstand de andere inspanningsvormen geleidelijk worden afgebouwd en de training door middel van lopen geleidelijk worden opgevoerd.
De fysiotherapeut stimuleert de patiënt om na afloop van de behandelperiode zelf actief te blijven en de gezonde leefgewoonten te continueren. Beweging maakt hiervan een belangrijk onderdeel uit.
Op basis van het trainingsprogramma voor thuis zal de patiënt uiteindelijk de bewegingsactiviteiten zelfstandig, dat wil zeggen zonder fysiotherapeutische begeleiding, op een verantwoorde wijze moeten kunnen (en durven) uitvoeren.
De fysiotherapeutische begeleiding wordt teruggebracht als de behandeldoelen bereikt zijn, wanneer de patiënt de doelen verder zelfstandig kan bereiken of wanneer de patiënt, in overleg met de fysiotherapeut, geen baat meer verwacht van de behandeling.
Op de lange termijn zijn beweegvormen die leuk zijn en in groepsverband worden uitgevoerd gemakkelijker vol te houden. Indien voorhanden, wijst de fysiotherapeut de patiënt op locoregionale beweeg- en activiteitenprogramma’s (bijvoorbeeld sportief wandelen, medische fitnessprogramma’s, Hart in Beweging), die de patiënt kunnen motiveren om zijn actieve leefstijl te onderhouden.
C.4.2 Stoppen met roken
De fysiotherapeut kan het rookgedrag van de patiënt benoemen en moet, indien van toepassing, de patiënt herhaaldelijk en actief stimuleren om te stoppen met roken. Hierbij kan hij gebruikmaken van motiverende gesprekstechnieken.
Er bestaan verscheidene interventies die gericht zijn op stoppen met roken, zoals beschreven in de Multidisciplinaire Richtlijn Hartrevalidatie en de Zorgstandaard Vasculair risicomanagement van het Platform Vitale Vaten. Eventueel kan de fysiotherapeut de patiënt terugverwijzen naar de verwijzer of naar andere hulpverleners of wijzen op cursussen die zijn gericht op stoppen met roken (zie www.rokeninfo.nl van het Nationaal Expertisecentrum Tabaksontmoediging van het Trimbos-instituut, www.trimbos.nl).
Roken is van invloed op het inspanningsvermogen van patiënten met sPAV. Uit een vergelijking tussen rokende en niet-rokende patiënten met sPAV bleek dat rokers een kortere pijnvrije en maximale loopafstand, een lagere VO2max en een verminderde perifere circulatie hebben, evenals een verminderde loopfunctie, maar ook dat zij minder lichamelijk actief zijn en dat zij een lagere kwaliteit van leven hebben.117,118 Roken verhoogt dus niet alleen het risico op hart- en vaatziekten, maar ook het risico op een functioneel afhankelijke levensstijl. De fysiotherapeut kan het rookgedrag van de patiënt benoemen en de patiënt herhaaldelijk en actief stimuleren om te stoppen met roken. Hierbij kan hij gebruikmaken van motiverende gesprekstechnieken.
Er bestaan verscheidene interventies die gericht zijn op stoppen met roken, zoals beschreven in de Multidisciplinaire Richtlijn Hartrevalidatie52 en de Zorgstandaard Vasculair risicomanagement119 van het Platform Vitale Vaten. De fysiotherapeut kan de patiënt terugverwijzen naar de verwijzer of naar andere hulpverleners of wijzen op cursussen gericht op stoppen met roken, zoals aangeboden door onder andere zorgverzekeraars en Stivoro.
C.4.3 Ontwikkelen van een gezond voedingspatroon
Het ontwikkelen en bevorderen van een gezond voedingspatroon bij de patiënt behoort strikt genomen niet tot de fysiotherapeutische behandeling. De fysiotherapeut kan de patiënt wijzen op het belang van gezonde voeding en een regelmatig eetpatroon, de relatie tussen energie-inname en verbranding (benodigde beweging voor calorieverbruik van een bepaald voedingsmiddel) en het gezondheidsrisico dat overgewicht met zich meebrengt. Voor specialistische vragen kan de fysiotherapeut de patiënt verwijzen naar een diëtist, bij voorkeur binnen de bestaande ketenzorg.
Een gezond voedingspatroon kan bijdragen aan een verlaging van het risico op (andere) hart- en vaatziekten. Het ontwikkelen en bevorderen van een gezond voedingspatroon bij de patiënt behoort strikt genomen niet tot de fysiotherapeutische behandeling. Wél kan de fysiotherapeut de patiënt wijzen op het belang van gezonde voeding en een regelmatig eetpatroon, de relatie tussen energie-inname en verbranding (benodigde beweging voor calorieverbruik van een bepaald voedingsmiddel) en het gezondheidsrisico dat overgewicht met zich meebrengt. Voor specialistische vragen kan de fysiotherapeut de patiënt verwijzen naar een diëtist(e), bij voorkeur binnen de bestaande ketenzorg.
C.4.4 Bevorderen van therapietrouw aan medicatie
Therapietrouw kan bevorderd worden door uitleg te geven over het te verwachten effect van de medicatie en de wijze van gebruik. Tevens kan extra informatie over de werking van de medicatie en eventuele hulpmiddelen bij inname (pillendoosje, medicijnrol) motiverend werken. Daarnaast kan de fysiotherapeut structureel (bijvoorbeeld vier keer per jaar) navragen of er problemen zijn rond de voorgeschreven medicatie, of alle voorgeschreven medicatie daadwerkelijk wordt ingenomen en of de patiënt zelf (‘kleine’) aanpassingen in dosering/frequentie heeft gedaan in verband met (vermeende) bijwerkingen. De mate van begeleiding wordt hierbij bepaald door de aangegeven of bemerkte problematiek.
Als de fysiotherapeut vermoedt of constateert dat de patiënt de voorgeschreven medicatie niet of onvoldoende gebruikt, dient dit ter sprake te worden gebracht en gerapporteerd (mogelijk door de patiënt zelf) aan de huisarts dan wel de praktijkondersteuner (POH), die in veel huisartsenpraktijken patiënten begeleidt in het kader van cardiovasculair risicomanagement. De POH’er geeft ondersteuning en advies bij het aanpassen van de leefstijl, stoppen met roken en het voedingspatroon. In de komende jaren zal op locoregionaal niveau gezocht moeten worden naar een modus om de geboden zorg complementair te laten zijn. Goede communicatie en duidelijke afspraken over elkaars inbreng zijn hierbij van essentieel belang.
Het verminderen van het risico op (andere) hart- en vaatziekten kan deels bewerkstelligd worden door het voorschrijven van medicatie. Conform de aanpak binnen de hartrevalidatie kan de therapietrouw bevorderd worden door uitleg te geven over het te verwachten effect van de medicatie en de wijze waarop de medicatie gebruikt moet worden.52 Tevens kan extra informatie over de werking van de medicatie en eventuele hulpmiddelen bij inname (pillendoosje, medicijnrol) motiverend werken. Daarnaast kan de fysiotherapeut structureel (bijvoorbeeld vier keer per jaar) navragen of er problemen zijn rond de voorgeschreven medicatie, of alle voorgeschreven medicatie daadwerkelijk wordt ingenomen en of de patiënt zelf (‘kleine’) aanpassingen in dosering/frequentie heeft gedaan in verband met (vermeende) bijwerkingen. De mate van begeleiding wordt hierbij bepaald door de aangegeven of opgemerkte problematiek. Als de fysiotherapeut vermoedt of constateert dat de patiënt de voorgeschreven medicatie niet of onvoldoende gebruikt, dient dit ter sprake te worden gebracht en gerapporteerd (mogelijk door de patiënt zelf) aan de huisarts, dan wel de praktijkondersteuner huisartsenzorg (POH), die in veel huisartsenpraktijken patiënten begeleidt in het kader van cardiovasculair risicomanagement. De POH geeft ondersteuning en advies bij het aanpassen van de leefstijl, stoppen met roken en het voedingspatroon.3,120
In de komende jaren zal op locoregionaal niveau gezocht moeten worden naar een modus om de geboden zorg complementair te laten zijn. Goede communicatie en duidelijke afspraken over elkaars inbreng zijn hierbij van essentieel belang.
C.5 Afsluiting van de behandeling
Als de in het behandelplan geformuleerde behandeldoelen zijn bereikt, of als de fysiotherapeut inschat dat de patiënt de doelstellingen zelfstandig kan bereiken, zonder fysiotherapeutische begeleiding, kan de frequentie van de sessies naar beneden worden bijgesteld. De hoeveelheid begeleiding door de fysiotherapeut kan ook verminderd worden als de patiënt, in overleg met de fysiotherapeut, verwacht geen baat meer te hebben bij de behandeling ten aanzien van de behandeldoelen.
Bij patiënten bij wie de situatie onvoldoende verbetert en bij wie daarom een operatieve behandeling aangewezen is, wordt echter aanbevolen de looptraining te continueren tot aan de operatie. Na de operatie kan de behandeling eventueel worden voortgezet.
Als er sprake is van comorbiditeit(en), dient de behandeling hierop aangepast te worden: dit kan consequenties hebben voor het aantal, de frequentie of de duur van de sessies en voor het maximaal te behalen resultaat van de behandeling.
C.6 Evaluatie van de behandeling
De patiënt wordt drie, zes, negen en 12 maanden na aanvang van de behandeling door de fysiotherapeut gezien voor gestandaardiseerde follow-upmetingen. Centraal bij de evaluatie staat het meten van het effect van de behandeling op de kwaliteit van leven van de patiënt (gemeten met de EQ-5D). Aan de hand van de loopbandtest wordt de (verbetering van de) functionele status van de patiënt vastgesteld. Hiermee kan worden gecontroleerd of de patiënt vooruitgang heeft geboekt op de belangrijkste klachten op het gebied van fysieke activiteiten. Tevens worden de resultaten ten aanzien van het looppatroon, de risicofactoren voor hart- en vaatziekten en de psychische factoren geëvalueerd. Indien nodig worden, aan de hand van de bevindingen, de behandeldoelen bijgesteld. In bijlage 5 (opent in nieuw tabblad) staan per subdoel de evaluatie-instrumenten met de gewenste eindresultaten.
Indien geen verbetering is opgetreden in de toestand van de patiënt maakt de fysiotherapeut een inschatting of er in de komende periode (bijvoorbeeld drie maanden) wel een verbetering kan worden verwacht. Indien de patiënt de behandeldoelen niet heeft bereikt en de fysiotherapeut in overleg met de patiënt verwacht dat de patiënt het maximale heeft bereikt, wordt de frequentie van de behandelsessies verminderd, of wordt de behandeling beëindigd en wordt de patiënt terugverwezen naar de verwijzer. Ook als tussentijds complicaties optreden wordt de patiënt terugverwezen naar de verwijzer. Evaluatie van de behandeling vindt echter altijd plaats drie, zes, negen en 12 maanden na aanvang van de behandeling.
Idealiter vindt na deze 12 maanden elk kwartaal een controle plaats door een zorgverlener, waarbij de functionele status en de kwaliteit van leven van de patiënt geëvalueerd worden. Indien er geen bijzonderheden zijn, hoeft er geen zorgtraject te worden ingezet. Indien er wel problemen geconstateerd worden (terugval in loopafstand, opnieuw roken, niet (juist) gebruiken van bepaalde medicatie), kan in overleg met de patiënt worden bepaald of een kort behandelingstraject bij een fysiotherapeut zinvol wordt geacht. Ook kan een doorverwijzing naar een medisch specialist noodzakelijk zijn.
C.7 Verslaggeving, terugrapportage naar de verwijzer en samenwerking
Voor een juiste verslaglegging wordt verwezen naar de vigerende KNGF-richtlijn Fysiotherapeutische dossiervoering (opent in nieuw tabblad).(voorheen 44)Indien om bepaalde redenen niet behandeld kan worden volgens de richtlijn, wordt hiervan kort en bondig melding gemaakt. De verwijzer en de huisarts, indien deze niet de verwijzer is, worden na drie en 12 maanden, of als zich problemen voordoen, geïnformeerd over de behandeling, de behandeldoelen, de behandelresultaten en de gegeven adviezen volgens een standaard terugkoppelingsbrief (een voorbeeldbrief is te downloaden via de website van Chronisch ZorgNet (opent in nieuw tabblad)).
Aanbevolen wordt om in ieder geval in de terugrapportage op te nemen:
- Hulpvraag en behandeldoelen;
- Aantal behandelingen;
- Functionele en maximale loopafstanden;
- Conclusie met betrekking tot de behandeldoelen;
- Mogelijkheden tot verbetering.
Indien deze richtlijn wordt gebruikt als onderdeel van ketenzorg, dienen de ketenzorgafspraken (bijvoorbeeld terugkerend multidisciplinair overleg of afstemming met andere zorgverleners over ieders verantwoordelijkheden) te worden gevolgd. Bij wijzigingen of specifieke problemen die van belang zijn voor andere hulpverleners, worden de ketenzorgpartners hierover geïnformeerd.
C.8 De keuze voor een behandeling
C.8.1 De keuze voor looptraining en/of andere vormen van beweeginterventies
Aanbevelingen
- Zet samen beslissen (persoonsgerichte zorg) in om samen met de patiënt een keuze te maken voor looptraining en/of andere vormen van beweeginterventie(s), gericht op het bevorderen van het fysiek functioneren en de kwaliteit van leven, binnen de fysio-/oefentherapeutische behandeling van patiënten met symptomatisch Perifeer Arterieel Vaatlijden (sPAV).
- Volg hierbij de vier stappen van het proces van samen beslissen zoals beschreven in module ‘A.8.2 Achtergrond’ (opent in nieuw tabblad).
o Betrek bij stap twee ‘option talk’:
- de beschikbare wetenschappelijke kennis over de behandelopties (zie ‘Toelichting: Conclusies op basis van de literatuur C.8.1’ );
- de klinische expertise van de therapeut met betrekking tot de behandelopties;
- de voor- en nadelen van de behandelopties (waarin o.a. aandacht is voor de FITT-factoren: Frequentie, Intensiteit, Tijd en Type van de training);
- de trainingsprincipes (zoals de specificiteit van een behandeloptie in relatie tot de trainingsdoelen en de mogelijkheid om met een behandeloptie de minimaal vereiste drempel voor een trainingsprikkel – en vervolgens een trainingseffect – te bereiken);
- de verwachte uitkomsten van de behandelopties (zie ‘Verantwoording: Effectiviteit en bewijskracht C.8.1’ );
- de invloed en de gevolgen van de behandelopties op de persoonlijke situatie en mogelijkheden van de patiënt (o.a. comorbiditeit, bewegingsangst en arbeidsomstandigheden).
- Evalueer de voortgang van de behandeling op gezette tijden (zie module C.6 ‘Evaluatie van de behandeling’ (opent in nieuw tabblad) ) en zet samen beslissen in om samen met de patiënt te bespreken of de gekozen beweeginterventie(s) nog voldoende op hem zijn afgestemd.
| Definitie ‘Beweeginterventies’Alle vormen van fysieke training of beweging met een cardio- en/of krachtcomponent die zich richten op het fysiek functioneren. Bijvoorbeeld: looptraining, krachttraining, fietstraining, nordic walking, et cetera. |
Beschrijving
Uit de bevindingen van de beschikbare wetenschappelijke literatuur kan niet worden geconcludeerd dat traditionele looptraining beter of slechter is voor het fysiek functioneren en de kwaliteit van leven dan andere vormen van beweeginterventies. Kortom, ondanks dat we weten dat beweging effectief is voor patiënten met sPAV, zijn we zeer onzeker of de ene vorm van training effectiever is dan de andere. Uit de voorkeuren van patiënten, de klinische expertise van therapeuten en de voor- en nadelen van de interventies blijkt dat zowel traditionele looptraining als andere vormen van beweeginterventies als relevante behandelopties worden beschouwd. In deze module wordt hierdoor geen aanbeveling gegeven voor één specifieke behandeloptie, maar wordt het toepassen van samen beslissen om te komen tot een keuze voor een beweeginterventie, nog belangrijker om het fysiek functioneren en de kwaliteit van leven te bevorderen binnen de fysio-/oefentherapeutische behandeling van patiënten met sPAV.
Aanleiding
Conform (inter)nationale richtlijnen is gesuperviseerde beweegtraining of looptraining de primair aanbevolen behandeling voor patiënten met symptomatisch Perifeer Arterieel Vaatlijden (sPAV) (Aboyans, 2018; Bartelink, 2014; Merry, 2014; Society for Vascular Surgery Lower Extremity Guidelines Writing, 2015). Desalniettemin zijn voor het vormgeven van het fysio-/oefentherapeutische behandelplan verschillende vormen en doseringen van beweeg- of looptraining mogelijk (Merry, 2014). Het behandelplan omvat daarmee meerdere beslissingen waarbij ruimte is voor samen beslissen. Dit is bij uitstek het geval bij beslissingen waarbij meerdere redelijke opties bestaan en de uiteindelijke keuze afhangt van de persoonlijke voorkeuren en waarden van de patiënt, of bij beslissingen waarbij de betrokkenheid en toewijding van de patiënt cruciaal zijn voor de uitvoering van de behandeling, zoals bij leefstijlkeuzes (van der Horst, 2023).
Uit de knelpuntenanalyse (gericht op samen beslissen) blijkt dat therapeuten vaak het gevoel hebben dat gesuperviseerde pijninducerende looptraining de primair in te zetten interventie moet zijn. Voor veel therapeuten is het onvoldoende duidelijk wat de voor- en nadelen van de verschillende mogelijke behandelopties zijn binnen de behandeling van patiënten met sPAV. Dit terwijl inzicht hebben in de beschikbare wetenschappelijke evidentie, en daarmee in de waarde van de verschillende behandelopties, juist van belang is voor het effectief toepassen van samen beslissen. Het aanbieden van deze kennis, naast de kennis uit de KNGF-richtlijn sPAV uit 2014 , kan fysio-/oefentherapeuten ondersteunen tijdens het samen beslissen, en helpen om patiënten met sPAV goed te laten participeren tijdens het proces van samen beslissen. Dit is vooral waardevol tijdens de option talk. Option talk, oftewel het optiegesprek, is een van de essentiële stappen in het proces van samen beslissen en omvat het informeren van de patiënt over de mogelijke behandelopties, inclusief bijbehorende voor- en nadelen, op basis van de beschikbare (of soms beperkte) wetenschappelijke kennis en klinische expertise (Elwyn, 2017; Stiggelbout, 2015).
Binnen module C.8.1 wordt ingegaan op de waarde van andere vormen van beweeginterventies ten opzichte van traditionele looptraining bij patiënten met sPAV. Binnen (inter)nationale richtlijnen is de primair aanbevolen interventie voor patiënten met sPAV een gesuperviseerde beweeginterventie die hoofdzakelijk bestaat uit looptraining (Aboyans, 2018; Bartelink, 2014; Gerhard-Herman, 2017; Society for Vascular Surgery Lower Extremity Guidelines Writing, 2015). Echter bestaan er meer opties naast looptraining, zoals krachttraining, fietstraining of nordic walking (looptraining met speciale wandelstokken). Uit de knelpuntenanalyse blijkt dat het voor therapeuten onduidelijk is of en wanneer er een voorkeur bestaat voor looptraining of andere vormen van beweeginterventies. In de praktijk wordt nu vaak primair de keuze gemaakt voor looptraining. Echter, die is niet altijd uitvoerbaar door patiënten (bijvoorbeeld door comorbiditeiten) of sluit niet altijd goed aan bij de hulpvraag van en/of de gewenste uitkomsten voor patiënten.
Om therapeuten inzicht te geven in de beschikbare wetenschappelijke evidentie is het van belang om aanbevelingen te formuleren voor de gewenste en ongewenste effecten van andere vormen van beweeginterventies ten opzichte van traditionele looptraining bij patiënten met sPAV. Hiertoe is de volgende uitgangsvraag geformuleerd:
Uitgangsvraag
Kan in plaats van traditionele looptraining ook gekozen worden voor andere vormen van beweeginterventies bij patiënten met sPAV?
Conclusies op basis van de literatuur
Op basis van de conclusies van de geselecteerde literatuur kunnen een aantal resultaten worden geformuleerd. Deze ‘Gestandaardiseerde formuleringen van de resultaten’ worden gevormd door de grootte van het effect en de bewijskracht te combineren en ze doen een uitspraak over de zekerheid van het bewijs dat in de literatuur is gevonden (Langendam, 2022).
Cruciale uitkomstmaten:
- Het wetenschappelijke bewijs is zeer onzeker over het effect van andere vormen van beweeginterventies (nordic walking, krachttraining, een combinatie van nordic walking en krachttraining, of stretchoefeningen) ten opzichte van traditionele gesuperviseerde of niet-gesuperviseerde looptraining bij patiënten met sPAV op fysiek functioneren (gemeten als de functionele loopafstand en maximale loopafstand met de loopbandtest, en de pijnvrije en totale loopafstand met de zes minuten wandeltest (6MWT)).
Toelichting: De geselecteerde gerandomiseerde studies beschrijven dat zowel andere vormen van beweeginterventies als traditionele looptraining positieve effecten hebben op fysiek functioneren. De bewijskracht van de resultaten uit de systematische literatuuranalyse is zeer laag, waardoor we zeer onzeker zijn over het effect dat vanuit de literatuur is aangetoond.
- Het wetenschappelijke bewijs is zeer onzeker over het effect van andere vormen van beweeginterventies (nordic walking, krachttraining of warmwatertraining) ten opzichte van traditionele gesuperviseerde of niet-gesuperviseerde looptraining bij patiënten met sPAV op kwaliteit van leven (gemeten met de SF-36 subschaal physical functioning).
Toelichting: De geselecteerde gerandomiseerde studies beschrijven dat zowel andere vormen van beweeginterventies als traditionele looptraining positieve effecten hebben op kwaliteit van leven. De bewijskracht van de resultaten uit de systematische literatuuranalyse is zeer laag, waardoor we zeer onzeker zijn over het effect dat vanuit de literatuur is aangetoond.
- Slechts één studie rapporteerde absolute resultaten over het fysiek functioneren gemeten met de walking impairment questionnaire (WIQ). In dit geval is ervoor gekozen om de resultaten narratief te beschrijven en is geen conclusie geformuleerd volgens de GRADE-methodiek.
- Er zijn geen studies gevonden die resultaten hebben beschreven op de overige cruciale uitkomstmaten: mate van pijn, levensverwachting of arbeidsparticipatie.
Belangrijke uitkomstmaten:
- Drie van de veertien geselecteerde studies beschrijven resultaten over ongewenste effecten gerelateerd aan een van de interventies. Deze drie studies vonden geen verschillen in ongewenste effecten tussen traditionele looptraining en andere vormen van beweeginterventies (krachttraining, crosstraining of warmwatertraining). Eén studie rapporteerde géén ongewenste effecten, één studie rapporteerde twaalf niet-ernstige ongewenste effecten (bestaande uit hypertensie, hypoglykemie en lichte knieklachten), en één studie rapporteerde vier ernstige ongewenste voorvallen waardoor patiënten deelname aan de studie moesten beëindigen (beroerte, hartinfarct of revascularisatie van het been).
Rationale van de aanbeveling
De werkgroep heeft besloten om een sterke aanbeveling voor het toepassen van samen beslissen op te nemen in deze richtlijnmodule. Hierbij waren er een aantal criteria (zie Verantwoording; ‘Van bewijs naar aanbeveling’) die zwaar en minder zwaar hebben gewogen.
Uit de resultaten van het systematische literatuuronderzoek kan niet worden geconcludeerd dat traditionele looptraining beter is voor het fysiek functioneren en de kwaliteit van leven op korte termijn (<1 jaar) dan andere beweeginterventies. Tegelijkertijd kan ook niet worden geconcludeerd dat andere beweeginterventies beter zijn voor het fysiek functioneren en de kwaliteit van leven dan traditionele looptraining. Kortom, we zijn zeer onzeker of de ene vorm van training effectiever is dan de andere. Wel suggereren de resultaten dat zowel looptraining als andere beweeginterventies mogelijk een positief effect hebben op fysiek functioneren en kwaliteit van leven. Het besluit van de werkgroep dat hieruit voortkomt, is dat andere vormen van beweeginterventies mogelijk niet onderdoen voor traditionele looptraining wanneer men kijkt naar de effecten op fysiek functioneren en kwaliteit van leven, en daarmee een goed alternatief kunnen zijn binnen de fysio-/oefentherapeutische behandeling voor patiënten met sPAV.
Een achterbanraadpleging onder patiënten met sPAV laat zien dat veel variatie bestaat in de voorkeur en waardering van patiënten ten aanzien van traditionele looptraining of andere vormen van beweeginterventies. Patiënten hechten veel waarde aan het kunnen kiezen tussen verschillende beweeginterventies.
De werkgroep beoordeelt dat de resultaten van het systematische literatuuronderzoek en de voorkeuren van patiënten laten zien dat voor zowel traditionele looptraining als andere beweeginterventies geldt dat de gewenste effecten (positieve effecten op fysiek functioneren en kwaliteit van leven) de ongewenste effecten overtreffen.
De economische overwegingen en kosteneffectiviteit zijn gelijkwaardig voor traditionele looptraining en andere beweeginterventies. De werkgroep verwacht dat het aanbieden van andere beweeginterventies naast looptraining kan zorgen voor een toename van de gezondheidsgelijkheid, doordat de aangeboden zorg beter kan worden afgestemd op de individuele patiënt (inclusieve zorg). De overige criteria van het proces van bewijs naar aanbeveling (aanvaardbaarheid en haalbaarheid) worden als niet-bezwaarlijk bevonden in het aanbieden van andere vormen van beweeginterventies naast traditionele looptraining.
Concluderend is het wetenschappelijke bewijs onzeker over het effect van andere vormen van beweeginterventies ten opzichte van traditionele looptraining, maar beoordeelt de werkgroep dat de gunstige effecten en de voorkeuren van patiënten overheersend zijn, waardoor er een sterke aanbeveling is geformuleerd voor het toepassen van samen beslissen om te komen tot een keuze voor de toe te passen beweeginterventie.
Literatuur
Zoeken en selecteren
Onderzoeksvraag
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende onderzoeksvraag:
- Wat is het effect van andere vormen van beweeginterventies ten opzichte van traditionele (gesuperviseerde of niet-gesuperviseerde) looptraining op het fysiek functioneren, de kwaliteit van leven, de mate van pijn, de levensverwachting en de arbeidsparticipatie bij patiënten met symptomatisch Perifeer Arterieel Vaatlijden (sPAV)?
Relevante uitkomstmaten
De werkgroep achtte het fysiek functioneren, de kwaliteit van leven, de mate van pijn, de levensverwachting en de arbeidsparticipatie cruciale uitkomstmaten voor de besluitvorming. De werkgroep achtte ongewenste effecten gerelateerd aan een van de interventies, belangrijke uitkomstmaten.
Per uitkomstmaat:
- Fysiek functioneren
- Zes minuten wandeltest (6MWT): Uit de wetenschappelijke literatuur blijkt dat een verschil van acht meter als belangrijk effect beschouwd kan worden bij patiënten met PAV (klinisch relevant verschil) (McDermott, 2021). De werkgroep beschouwt* deze waarden ook als klinisch relevant voor patiënten met sPAV.
- Loopbandtest: De werkgroep definieerde*, op basis van de wetenschappelijke literatuur, een verschil van 250 meter (functionele loopafstand) en 305 meter (maximale loopafstand) als belangrijk effect bij patiënten met sPAV (klinisch relevant verschil) (van den Houten, 2016a).
- Shuttle Walk Test (SWT): Uit de wetenschappelijke literatuur blijkt dat een verschil van 174 seconden als belangrijk effect beschouwd kan worden bij patiënten met COPD (klinisch relevant verschil) (Zatloukal, 2019). Omdat wetenschappelijke literatuur over de klinische relevantie bij patiënten met sPAV ontbreekt, beschouwt* de werkgroep deze waarden als voldoende gelijkwaardig en daarmee als ook klinisch relevant voor patiënten met sPAV.
- Walking Impairment Questionnaire (WIQ): De werkgroep definieerde*, op basis van de wetenschappelijke literatuur, een verschil van 0.11 punten (op een schaal van 0 tot 1, waarbij een hogere score correspondeert met een betere mate van fysiek functioneren) als belangrijk effect bij patiënten met sPAV (klinisch relevant verschil) (Conijn, 2015).
- Kwaliteit van leven
- 36-Item Short Form Health Survey (SF-36): Uit de wetenschappelijke literatuur blijkt dat een verschil van 10 punten (physical functioning, bodily pain, general health en mental health), 12.5 punten (physical role, vitality en social functioning) en 8.3 punten (emotional role) als belangrijk effect beschouwd kan worden bij patiënten met COPD (klinisch relevant verschil) (Wyrwich, 2005). De schaal van de SF-36 loopt van 0 tot 100, waarbij een hogere score correspondeert met een betere kwaliteit van leven. Omdat wetenschappelijke literatuur over de klinische relevantie bij patiënten met sPAV ontbreekt, beschouwt* de werkgroep deze waarden als voldoende gelijkwaardig en daarmee als ook klinisch relevant voor patiënten met sPAV.
- Vascular Quality of Life Questionnaire-6 (VascuQol-6): De werkgroep definieerde*, op basis van de wetenschappelijke literatuur, een verschil van 1.7 punten (op een schaal van 6 tot 24, waarbij een hogere score correspondeert met een betere kwaliteit van leven) als belangrijk effect bij patiënten met sPAV (klinisch relevant verschil) (Nordanstig, 2017).
- EuroQol (EQ-5D): Uit de wetenschappelijke literatuur blijkt dat een verschil van 0.028 punten (op een schaal van -1 tot 1, waarbij een hogere score correspondeert met een betere kwaliteit van leven) als belangrijk effect beschouwd kan worden bij patiënten met COPD (klinisch relevant verschil) (Bae, 2020). Omdat wetenschappelijke literatuur over de klinische relevantie bij patiënten met sPAV ontbreekt, beschouwt* de werkgroep deze waarden als voldoende gelijkwaardig en daarmee als ook klinisch relevant voor patiënten met sPAV.
- Mate van pijn
- Numerical pain rating scale (NPRS): Uit de wetenschappelijke literatuur blijkt dat een verschil van 2 punten (op een schaal van 0 tot 10, waarbij een hogere score correspondeert met een hogere mate van pijn) als belangrijk effect beschouwd kan worden bij patiënten met chronische pijn (klinisch relevant verschil) (Farrar, 2001). Omdat wetenschappelijke literatuur over de klinische relevantie bij patiënten met sPAV ontbreekt, beschouwt* de werkgroep deze waarden als voldoende gelijkwaardig en daarmee als ook klinisch relevant voor patiënten met sPAV.
- Levensverwachting
- Mortaliteit: De werkgroep definieerde* een verschil van 1 op 100 personen als belangrijk effect bij patiënten met sPAV (klinisch relevant verschil).
- Arbeidsparticipatie
- Voor het meten van de arbeidsparticipatie is op voorhand geen meetinstrument met bijbehorende grenzen van klinische relevantie vastgesteld.
- Ongewenste effecten
- Major Adverse Events (ernstige ongewenste voorvallen): De werkgroep definieerde* een verschil van 1 op 50 personen als belangrijk effect bij patiënten met sPAV (klinisch relevant verschil).
- Ziekenhuisopnames: De werkgroep definieerde* een verschil van 1 op 50 personen als belangrijk effect bij patiënten met sPAV (klinisch relevant verschil).
*De werkgroep benadrukt dat het per individu kan verschillen of een effect wel of niet als klinisch relevant wordt beschouwd. Dit kan bijvoorbeeld afhankelijk zijn van de individuele hulpvraag en/of therapiedoelen. Desondanks zijn voor de start van het literatuuronderzoek bovenstaande specifieke grenzen voor klinische relevantie vastgesteld. De genoemde meetinstrumenten met bijbehorende criteria dienen als leidraad voor deze richtlijnmodule, met ruimte voor aanpassingen op basis van individuele patiëntbehoeften. De meetinstrumenten genoemd in de generieke KNGF-richtlijn sPAV (opent in nieuw tabblad) blijven de basis vormen voor diagnostiek en evaluatie.
Zoekactie van de literatuur
Op 17 augustus 2023 is door L. Marcellis (met ondersteuning van informatiespecialist A. Tillema) een systematische zoekactie uitgevoerd in MEDLINE, Embase, Cinahl en Cochrane (zie bijlage C.8.4-1 (opent in nieuw tabblad) voor de zoekverantwoording). De systematische zoekactie leverde 4.602 unieke treffers op. Na screening (door D. Conijn (DC), L. Marcellis (LM), M. Simon (MS) en T. Hoogeboom (TH)) van de titel en het abstract op de inclusiecriteria en exclusiecriteria (zie tabel 1) zijn 4.451 artikelen geëxcludeerd. Gekozen werd om artikelen van voor 2005 te excluderen omdat er een duidelijke toename zichtbaar was van het aantal publicaties in 2005. Artikelen waarvan het op basis van titel en abstract niet duidelijk was of deze voldeden aan de inclusiecriteria, werden dubbel gescreend door LM en vervolgens onderling besproken. Van 148 studies is het volledige artikel gescreend door LM, waarbij twijfelgevallen dubbel werden gescreend door DC en vervolgens onderling werden besproken. Uiteindelijk leverde de zoekactie negentien studies (gerapporteerd in 22 artikelen) op voor modules C.8.1, C.8.2, C.8.3 en C.8.4.
Voor module C.8.1 werden veertien studies (gerapporteerd in 17 artikelen) geselecteerd (Bronas, 2011; Bulinska, 2016; Chehuen, 2017; Collins, 2012; Cucato, 2013; Dziubek, 2020; Gardner, 2014; Kropielnicka, 2018; Meneses, 2011; Park, 2020; Ritti-Dias, 2010; Salisbury, 2022; Sanderson, 2006; Spafford, 2014; Szymczak, 2016; Treat-Jacobson, 2009; Van Schaardenburgh, 2017). Zie bijlage C.8.1-2 (opent in nieuw tabblad) voor het stroomdiagram van het inclusieproces. De artikelen die op basis van de volledige tekst zijn geëxcludeerd, en de reden van exclusie zijn weergegeven in bijlage C.8.1-3 (opent in nieuw tabblad).

Karakteristieken van geïncludeerde studies
De kenmerken van de geïncludeerde studies zijn weergegeven in bijlage C.8.1-4 (opent in nieuw tabblad).
De veertien ingesloten randomized controlled trials (RCT’s) includeerden in totaal 827 patiënten met sPAV (n=395 in de interventiegroepen en n=432 in de controlegroepen). Eén studie was relatief klein met slechts 19 geïncludeerde patiënten (Salisbury, 2022), negen studies includeerden meer dan 25 maar minder dan 70 patiënten (Chehuen, 2017; Cucato, 2013; Park, 2020; Ritti-Dias, 2010; Sanderson, 2006; Spafford, 2014; Szymczak, 2016; Treat-Jacobson, 2009; Van Schaardenburgh, 2017) en vier studies includeerden 70 of meer patiënten (Bulinska, 2016; Collins, 2012; Gardner, 2014; Kropielnicka, 2018). De gemiddelde leeftijd van patiënten varieerde van 60 tot 78 jaar. Het percentage vrouwen varieerde van 6 tot 54%. Eén studie includeerde enkel vrouwen (Park, 2020) en twee studies includeerden enkel mannen (Chehuen, 2017; Cucato, 2013). De studies zijn uitgevoerd in Australië (Sanderson, 2006), Brazilië (Chehuen, 2017; Cucato, 2013; Ritti-Dias, 2010), Noorwegen (Van Schaardenburgh, 2017), Polen (Bulinska, 2016; Kropielnicka, 2018; Szymczak, 2016), de Verenigde Staten (Collins, 2012; Gardner, 2014; Salisbury, 2022; Treat-Jacobson, 2009), het Verenigd Koninkrijk (Szymczak, 2016) en Zuid-Korea (Park, 2020). Van de veertien studies vergeleken tien studies gesuperviseerde looptraining met een andere beweeginterventie (Chehuen, 2017; Collins, 2012; Cucato, 2013; Dziubek, 2020; Kropielnicka, 2018; Park, 2020; Ritti-Dias, 2010; Salisbury, 2022; Sanderson, 2006; Szymczak, 2016) en twee studies vergeleken niet-gesuperviseerde looptraining met een andere beweeginterventie (Spafford, 2014; Van Schaardenburgh, 2017). De overige twee studies vergeleken zowel gesuperviseerde als niet-gesuperviseerde looptraining met een andere beweeginterventie (Gardner, 2014; Treat-Jacobson, 2009). Niet-gesuperviseerd trainen hield in dat patiënten zelfstandig trainden, maar wel begeleiding kregen van een zorgprofessional (door middel van activiteitenmonitors, telefonische feedback of fysieke controleafspraken). Andere vormen van beweeginterventies bestonden uit nordic walking (Bulinska, 2016; Collins, 2012; Spafford, 2014), fietstraining (Sanderson, 2006), handfietstraining (Treat-Jacobson, 2009), crosstraining (Salisbury, 2022), warmwatertraining (Park, 2020), stretchoefeningen (Chehuen, 2017; Cucato, 2013), krachttraining (Gardner, 2014; Ritti-Dias, 2010; Szymczak, 2016; Van Schaardenburgh, 2017) of een combinatie van nordic walking en krachttraining (Kropielnicka, 2018). De duur van de oefensessies varieerde van 20 tot 60 minuten met een frequentie van twee tot vier keer per week. De interventieduur varieerde van zes weken (Sanderson, 2006), acht weken (Van Schaardenburgh, 2017), twaalf weken (Bulinska, 2016; Chehuen, 2017; Cucato, 2013; Gardner, 2014; Kropielnicka, 2018; Park, 2020; Ritti-Dias, 2010; Salisbury, 2022; Spafford, 2014; Szymczak, 2016; Treat-Jacobson, 2009) tot 24 weken (Collins, 2012). Twee studies startten met een trainingsperiode van twaalf weken, gevolgd door een ongestructureerde follow-upperiode van nogmaals twaalf weken (Ritti-Dias, 2010; Treat-Jacobson, 2009).
Individuele studiekwaliteit (RoB)
Het risico op vertekening (risk of bias, RoB) van de gerandomiseerde studies is dubbel gescoord door LM en DC, LM en TH of LM en MS met behulp van de Cochrane Risk-of-Bias-2 tool (Higgins, 2019). Inconsistentie in het oordeel op de verschillende items is onderling besproken (LM en DC, LM en TH of LM en MS), waarna consensus is bereikt. Een overzicht van de beoordeling van de studiekwaliteit (RoB) per studie is weergegeven in bijlage C.8.1-5 (opent in nieuw tabblad) Risk-of-bias-tabel.
Effectiviteit en bewijskracht
Zie de Toelichting voor de conclusies op basis van de literatuur. Hieronder volgt een beschrijving van de effectiviteit en de bewijskracht voor de vergelijking(en).
Traditionele looptraining versus andere vormen van beweeginterventies
Het effect van traditionele looptraining vergeleken met andere vormen van beweeginterventies op fysiek functioneren en kwaliteit van leven is beschreven in negen studies (Bulinska, 2016; Chehuen, 2017; Collins, 2012; Cucato, 2013; Gardner, 2014; Kropielnicka, 2018; Park, 2020; Ritti-Dias, 2010; Van Schaardenburgh, 2017). Een overzicht van de resultaten wordt weergegeven in tabel 2. Zie bijlage C.8.1-6 (opent in nieuw tabblad) voor de forest plots van de uitkomsten op fysiek functioneren (totale loopafstand en pijnvrije loopafstand gemeten met de 6MWT, en functionele loopafstand en maximale loopafstand gemeten met de loopbandtest) en kwaliteit van leven (gemeten met de SF-36 subschaal physical functioning). Hieronder worden de effectiviteit en bewijskracht per uitkomstmaat beschreven.
Drie geselecteerde studies hebben het effect op fysiek functioneren (6MWT of loopbandtest) gemeten, maar geen absolute follow-updata gerapporteerd (Park, 2020; Salisbury, 2022; Treat-Jacobson, 2009). Eén studie heeft het effect op fysiek functioneren (WIQ) en kwaliteit van leven (SF-36) gemeten, maar geen absolute follow-updata gerapporteerd (Gardner, 2014). De ontbrekende follow-updata zijn opgevraagd bij de auteurs, maar een reactie werd niet ontvangen. Van twee studies konden de resultaten op fysiek functioneren niet worden geïncludeerd in de meta-analyse vanwege niet-normaal verdeelde data (Spafford, 2014; Szymczak, 2016). Omdat de resultaten door deze niet-normale verdeling niet goed vergelijkbaar zijn met andere studies, is in deze gevallen ervoor gekozen om de resultaten narratief te beschrijven en de studies niet te includeren in een meta-analyse.
Slechts één geselecteerde studie heeft het effect op fysiek functioneren (loopbandtest) na zes weken gemeten en gerapporteerd (Sanderson, 2006). Tevens heeft slechts één geselecteerde studie het effect op fysiek functioneren (WIQ) gemeten en gerapporteerd met normaal verdeelde data (Collins, 2012). Ook heeft slechts één geselecteerde studie het effect op kwaliteit van leven met alle SF-36-subschalen gemeten en gerapporteerd (Van Schaardenburgh, 2017). In deze gevallen is ervoor gekozen om de resultaten narratief te beschrijven en deze studies niet te includeren in een meta-analyse.
Twee studies rapporteerden geen absolute follow-updata met betrekking tot de resultaten op fysiek functioneren gemeten met de loopbandtest (Kropielnicka, 2018; Sanderson, 2006), maar werden eveneens geïncludeerd in een systematisch literatuuronderzoek van Jansen et al. (Jansen, 2020). De ontbrekende follow-updata voor de betreffende studies werden door Jansen et al. ontvangen nadat een verzoek was ingediend bij de auteurs. Voor de huidige richtlijn hebben we ook getracht de ontbrekende data op te vragen bij de auteurs. Aangezien geen reactie is ontvangen, werden voor deze studies de gerapporteerde data uit Jansen et al. gebruikt.
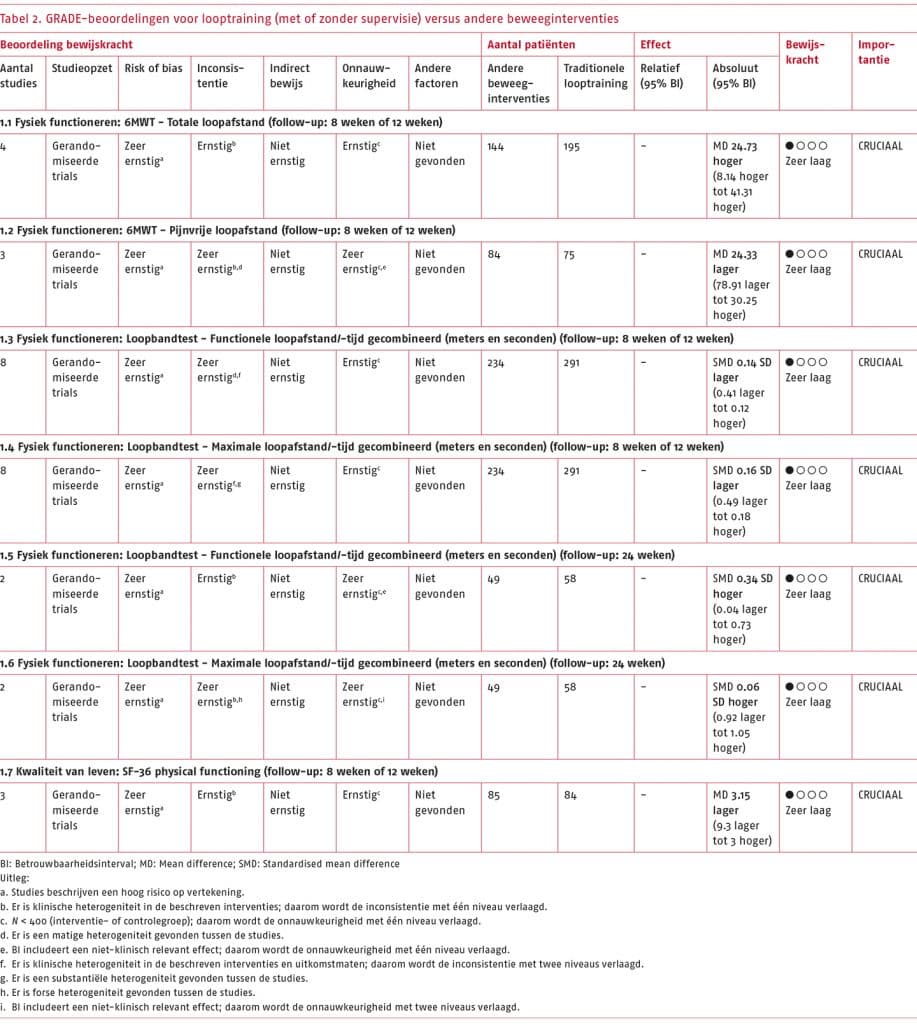
Vergelijking 1. Fysiek functioneren – 6MWT totale loopafstand (follow-up: 8 of 12 weken)
In vier studies is de effectiviteit van looptraining vergeleken met die van andere vormen van beweeginterventies (nordic walking, krachttraining of een combinatie van beide) op fysiek functioneren, gemeten als 6MWT totale loopafstand na acht of twaalf weken (Bulinska, 2016; Gardner, 2014; Kropielnicka, 2018; Van Schaardenburgh, 2017). Het gemiddelde verschil (MD) tussen de groepen was 24.73 meter (95% BI 8.14 tot 41.31; p=0.003; n=144 groep andere beweeginterventies, n=195 looptraininggroep) in het voordeel van de andere beweeginterventies. Dit effect wordt door de werkgroep als een significant en klinisch relevant effect beschouwd (McDermott et al., 2021).
De bewijskracht is met vier niveaus verlaagd tot zeer laag, gezien het risico op vertekening door de individuele studiekwaliteit (-2 niveaus), door de gevonden inconsistentie (-1 niveau) en door de gevonden onnauwkeurigheid (-1 niveau).
Vergelijking 2. Fysiek functioneren – 6MWT pijnvrije loopafstand (follow-up: 8 of 12 weken)
In drie studies is de effectiviteit van looptraining vergeleken met die van andere vormen van beweeginterventies (nordic walking of krachttraining) op fysiek functioneren, gemeten als 6MWT pijnvrije loopafstand na 8 of 12 weken (Bulinska, 2016; Kropielnicka, 2018; Van Schaardenburgh, 2017). Het gemiddelde verschil (MD) tussen de groepen was 24.33 meter (95% BI -78.91 tot 30.25; p=0.38; n=84 groep andere beweeginterventies, n=75 looptraininggroep) in het voordeel van de looptraining. Dit effect wordt door de werkgroep als een niet-significant en klinisch relevant effect beschouwd (McDermott et al., 2021).
De bewijskracht is met zes niveaus verlaagd tot zeer laag, gezien het risico op vertekening door de individuele studiekwaliteit (-2 niveaus), door de gevonden inconsistentie (-2 niveaus) en door de gevonden onnauwkeurigheid (-2 niveaus).
Vergelijking 3. Fysiek functioneren – Loopbandtest functionele loopafstand (follow-up: 8 of 12 weken)
In acht studies is de effectiviteit van looptraining vergeleken met die van andere vormen van beweeginterventies (nordic walking, krachttraining, een combinatie van nordic walking en krachttraining, of stretchoefeningen) op fysiek functioneren, gemeten als functionele loopafstand met de loopbandtest na acht of twaalf weken (Bulinska, 2016; Chehuen, 2017; Collins, 2012; Cucato, 2013; Gardner, 2014; Kropielnicka, 2018; Ritti-Dias, 2010; Van Schaardenburgh, 2017). Het gestandaardiseerde gemiddelde verschil (SMD) tussen de groepen was 0.14 SD (95% BI -0.41 tot 0.12, p=0.28, n=234 groep andere beweeginterventies, n=291 looptraininggroep) in het voordeel van de looptraining. Dit effect wordt door de werkgroep als een niet-significant en niet-klinisch relevant effect beschouwd (Sawilowsky, 2009).
De bewijskracht is met vijf niveaus verlaagd tot zeer laag, gezien het risico op vertekening door de individuele studiekwaliteit (-2 niveaus), door de gevonden inconsistentie (-2 niveaus) en door de gevonden onnauwkeurigheid (-1 niveau).
Vergelijking 4. Fysiek functioneren – Loopbandtest maximale loopafstand (follow-up: 8 of 12 weken)
In acht studies is de effectiviteit van looptraining vergeleken met die van andere vormen van beweeginterventies (nordic walking, krachttraining, een combinatie van nordic walking en krachttraining, of stretchoefeningen) op fysiek functioneren, gemeten als functionele loopafstand met de loopbandtest na acht of twaalf weken (Bulinska, 2016; Chehuen, 2017; Collins, 2012; Cucato, 2013; Gardner, 2014; Kropielnicka, 2018; Ritti-Dias, 2010; Van Schaardenburgh, 2017). Het gestandaardiseerde gemiddelde verschil (SMD) tussen de groepen was 0.16 SD (95% BI -0.49 tot 0.18, p=0.36, n=234 groep andere beweeginterventies, n=291 looptraininggroep) in het voordeel van de looptraining. Dit effect wordt door de werkgroep als een niet-significant en niet-klinisch relevant effect beschouwd (Sawilowsky, 2009).
De bewijskracht is met vijf niveaus verlaagd tot zeer laag, gezien het risico op vertekening door de individuele studiekwaliteit (-2 niveaus), door de gevonden inconsistentie (-2 niveaus) en door de gevonden onnauwkeurigheid (-1 niveau).
Vergelijking 5. Fysiek functioneren – Loopbandtest functionele loopafstand (follow-up: 24 weken)
In twee studies is de effectiviteit van looptraining vergeleken met die van andere vormen van beweeginterventies (nordic walking of krachttraining) op fysiek functioneren, gemeten als functionele loopafstand met de loopbandtest na 24 weken (Collins, 2012; Ritti-Dias, 2010). Het gestandaardiseerde gemiddelde verschil (SMD) tussen de groepen was 0.34 SD (95% BI -0.04 tot 0.73, p=0.08, n=49 groep andere beweeginterventies, n=58 looptraininggroep) in het voordeel van de andere beweeginterventies. Dit effect wordt door de werkgroep als een niet-significant en niet-klinisch relevant effect beschouwd (Sawilowsky, 2009).
De bewijskracht is met vijf niveaus verlaagd tot zeer laag, gezien het risico op vertekening door de individuele studiekwaliteit (-2 niveaus), door de gevonden inconsistentie (-1 niveau) en door de gevonden onnauwkeurigheid (-2 niveaus).
Vergelijking 6. Fysiek functioneren – Loopbandtest maximale loopafstand (follow-up: 24 weken)
In twee studies is de effectiviteit van looptraining vergeleken met die van andere vormen van beweeginterventies (nordic walking of krachttraining) op fysiek functioneren, gemeten als maximale loopafstand met de loopbandtest na 24 weken (Collins, 2012; Ritti-Dias, 2010). Het gestandaardiseerde gemiddelde verschil (SMD) tussen de groepen was 0.06 SD (95% BI -0.92 tot 1.05, p=0.9, n=49 groep andere beweeginterventies, n=58 looptraininggroep) in het voordeel van de andere beweeginterventies. Dit effect wordt door de werkgroep als een niet-significant en niet-klinisch relevant effect beschouwd (Sawilowsky, 2009).
De bewijskracht is met zeven niveaus verlaagd tot zeer laag, gezien het risico op vertekening door de individuele studiekwaliteit (-2 niveaus), door de gevonden inconsistentie (-2 niveaus) en door de gevonden onnauwkeurigheid (-3 niveaus).
Vergelijking 7. Kwaliteit van leven – SF-36 physical functioning (follow-up: 8 of 12 weken)
In drie studies is de effectiviteit van looptraining vergeleken met die van andere vormen van beweeginterventies (nordic walking, krachttraining of warmwatertraining) op kwaliteit van leven, gemeten met de SF-36 subschaal physical functioning (Collins, 2012; Park, 2020; Van Schaardenburgh, 2017). Het gemiddelde verschil (MD) tussen de groepen was 3.15 punten (95% BI -9.3 tot 3.00; p=0.32; n=85 groep andere beweeginterventies groep, n=84 looptraininggroep) in het voordeel van de looptraining. Dit effect wordt door de werkgroep als een niet-significant en niet-klinisch relevant effect beschouwd (Wyrwich et al., 2005).
De bewijskracht is met vier niveaus verlaagd tot zeer laag, gezien het risico op vertekening door de individuele studiekwaliteit (-2 niveaus), door de gevonden inconsistentie (-1 niveau) en door de gevonden onnauwkeurigheid (-1 niveau).
Overige cruciale uitkomstmaten
Er zijn geen studies gevonden die resultaten hebben beschreven op de overige cruciale uitkomstmaten (levensverwachting, mate van pijn en arbeidsparticipatie).
Ongewenste effecten
Er zijn drie studies gevonden die resultaten hebben beschreven met betrekking tot ongewenste effecten (Gardner, 2014; Park, 2020; Salisbury, 2022). Vanwege de gevonden klinische heterogeniteit in deze data is ervoor gekozen om deze resultaten niet te includeren in een meta-analyse en enkel narratief te beschrijven. De studie van Gardner et al. rapporteerde veertien ongewenste voorvallen gedurende de studie. Vier patiënten (twee in krachttraininggroep en twee in looptraininggroep) moesten deelname aan de studie beëindigen (beroerte; n=2, hartinfarct; n=1, revascularisatie van been; n=1) vanwege een ernstig ongewenst voorval (Gardner, 2014). De studie van Park et al. rapporteerde geen ongewenste voorvallen (Park, 2020). De studie van Salisbury et al. rapporteerde twaalf niet-ernstige ongewenste voorvallen (hypertensie, hypoglykemie, lichte knieklachten). In de looptraininggroep kwam dit neer op drie ongewenste voorvallen per 180 trainingsuren, in de crosstraininggroep op negen ongewenste voorvallen per 236 trainingsuren (Salisbury, 2022).
Individuele RCT’s
In negen studies werden resultaten gerapporteerd die niet zijn geïncludeerd in een van de meta-analyses. Redenen hiervoor zijn het ontbreken van absolute follow-updata (Gardner, 2014; Park, 2020; Salisbury, 2022; Treat-Jacobson, 2009), het presenteren van niet-normaal verdeelde data (Spafford, 2014; Szymczak, 2016), of het betreft slechts één studie die resultaten rapporteert op een bepaalde uitkomstmaat met een bepaalde follow-up (Collins, 2012; Sanderson, 2006; Van Schaardenburgh, 2017). De resultaten van deze negen studies worden hieronder narratief beschreven.
Sanderson et al.
In de RCT van Sanderson et al. is de effectiviteit van gesuperviseerde fietstraining vergeleken met die van gesuperviseerde looptraining op fysiek functioneren na zes weken (gemeten als functionele en maximale looptijd met de loopbandtest) (Sanderson, 2006). Data worden gepresenteerd als gemiddelde ± SD voor functionele looptijd, en als gemiddelde verandering (95%-BI) voor maximale looptijd (zie tabel 3).
De bevindingen over de functionele looptijd bevestigen de resultaten van het systematische literatuuronderzoek, dat na acht en twaalf weken ook verschillen in het voordeel van de looptraininggroep vond op functionele loopafstand/-tijd gemeten met de loopbandtest. Echter, de resultaten uit het systematische onderzoek waren niet-significant. De bevindingen over de maximale looptijd bevestigen de resultaten van het systematische literatuuronderzoek, dat na acht en twaalf weken ook niet-significante verschillen in het voordeel van de looptraininggroep vond op maximale loopafstand/-tijd gemeten met de loopbandtest.
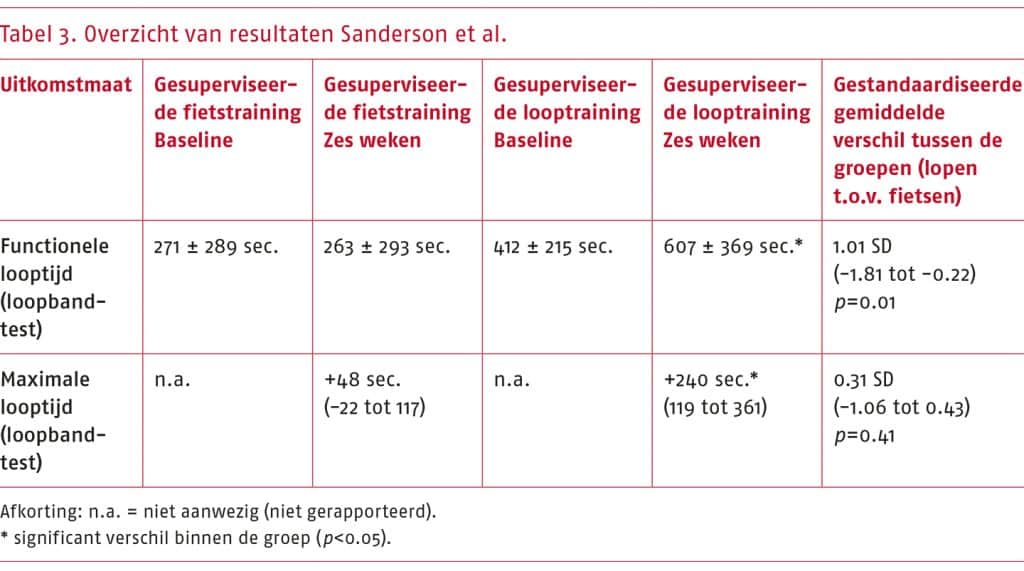
Treat-Jacobson et al.
In de RCT van Treat-Jacobson et al. is de effectiviteit van gesuperviseerde handfietstraining vergeleken met die van gesuperviseerde looptraining of niet-gesuperviseerde looptraining op fysiek functioneren na drie en zes maanden (gemeten als functionele en maximale loopafstand met de loopbandtest) (Treat-Jacobson, 2009). Data worden gepresenteerd als gemiddelde ± SD (zie tabel 4).
De bevindingen over de functionele loopafstand laten enkel significante verschillen zien in het voordeel van handfietstraining wanneer handfietstraining wordt vergeleken met niet-gesuperviseerde looptraining. Geen significante verschillen worden gevonden tussen de looptraining of tussen handfietstraining en gesuperviseerde looptraining. Deze bevindingen zijn deels tegengesteld aan de resultaten van het systematische literatuuronderzoek, dat na acht en twaalf weken niet-significante verschillen in het voordeel van de looptraininggroep vond, en na zes maanden niet-significante verschillen in het voordeel van andere beweeginterventies. De bevindingen over maximale loopafstand laten significante verschillen zien in het voordeel van handfietstraining en gesuperviseerde looptraining, wanneer deze worden vergeleken met niet-gesuperviseerde looptraining. Geen significante verschillen worden gevonden tussen handfietstraining en gesuperviseerde looptraining. Deze bevindingen zijn deels tegengesteld aan de resultaten van het systematische literatuuronderzoek, dat na acht en twaalf weken niet-significante verschillen in het voordeel van de looptraininggroep vond, en na zes maanden niet-significante verschillen in het voordeel van andere beweeginterventies.
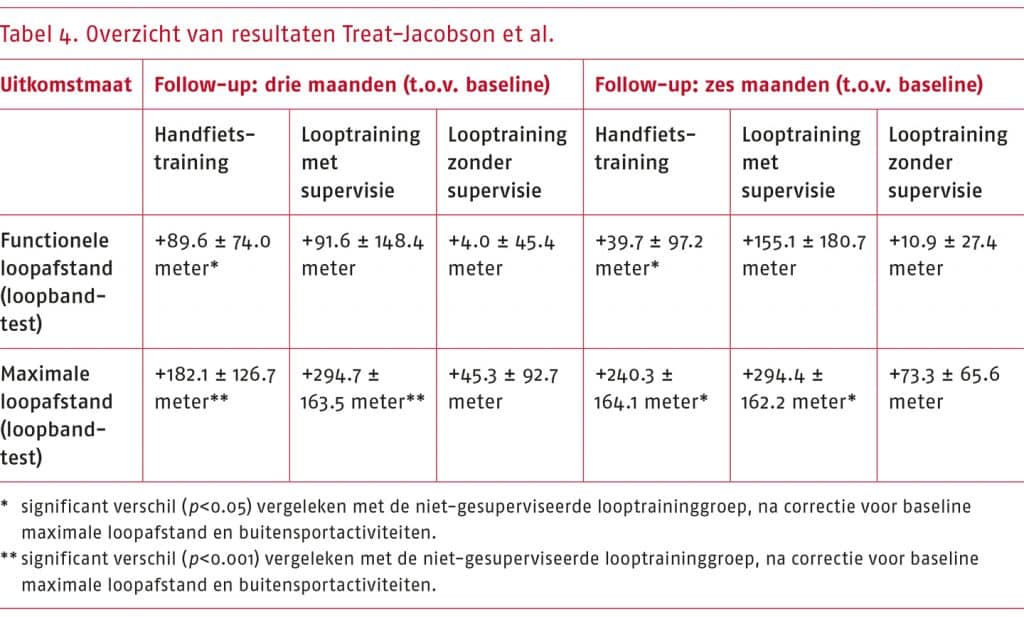
Collins et al.
In de RCT van Collins et al. is de effectiviteit van gesuperviseerde nordic walking vergeleken met die van gesuperviseerde looptraining op fysiek functioneren na zes weken, drie maanden en zes maanden (gemeten met de WIQ distance subschaal) (Collins, 2012). Data worden gepresenteerd als gemiddelde ± SD (zie tabel 5).
P-waarden van verschillen binnen de groepen werden niet gerapporteerd. Het gemiddelde verschil (MD) tussen de groepen op drie maanden was 2.30 punten (95% BI -16.26 tot 11.66, p=0.75) in het voordeel van de looptraininggroep. Deze bevindingen bevestigen de resultaten van het systematische literatuuronderzoek op fysiek functioneren na acht of twaalf weken gemeten met de pijnvrije loopafstand (6MWT) en de functionele en maximale loopafstand (loopbandtest). De bevindingen zijn tegengesteld aan de resultaten van het systematische literatuuronderzoek op fysiek functioneren na acht of twaalf weken gemeten met de totale loopafstand (6MWT).
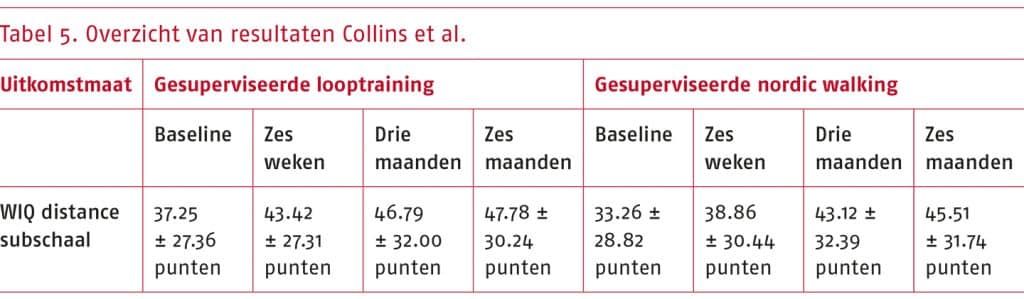
Spafford et al.
In de RCT van Spafford et al. is de effectiviteit van niet-gesuperviseerde nordic walking vergeleken met die van niet-gesuperviseerde looptraining op fysiek functioneren na drie maanden (gemeten als functionele en maximale loopafstand met de SWT) (Spafford, 2014). Alle data worden gepresenteerd als mediaan (range) (zie tabel 6).
Verschillen tussen de groepen waren voor beide uitkomstmaten niet-significant, wat de bevindingen bevestigt van het systematische literatuuronderzoek, dat ook niet-significante verschillen op functionele en maximale loopafstand liet zien.

Szymczak et al.
In de RCT van Szymczak et al. is de effectiviteit van gesuperviseerde krachttraining vergeleken met die van gesuperviseerde looptraining op fysiek functioneren na drie maanden (gemeten als totale en pijnvrije loopafstand met de 6MWT en functionele en maximale loopafstand gemeten met de loopbandtest) (Szymczak, 2016). Data worden gepresenteerd als mediaan ± range vanwege een niet-normale verdeling van de data (zie tabel 7).
De studie beschrijft dat geen statistisch significante verschillen (p-waarden niet gerapporteerd) werden gevonden tussen de groepen. Voor functionele en maximale loopafstand gemeten met de loopbandtest zijn deze bevindingen tegengesteld aan de resultaten van het systematische literatuuronderzoek, waarin verschillen werden gevonden in het voordeel van de looptraininggroep. Echter, zowel deze RCT als het systematische literatuuronderzoek laat niet-significante verschillen zien. Voor de pijnvrije loopafstand gemeten met de 6MWT bevestigen de bevindingen de resultaten van het systematische literatuuronderzoek, en voor de totale loopafstand gemeten met de 6MWT zijn de bevindingen tegengesteld aan de resultaten van het literatuuronderzoek, dat significante verschillen vond in het voordeel van andere vormen van beweeginterventies.
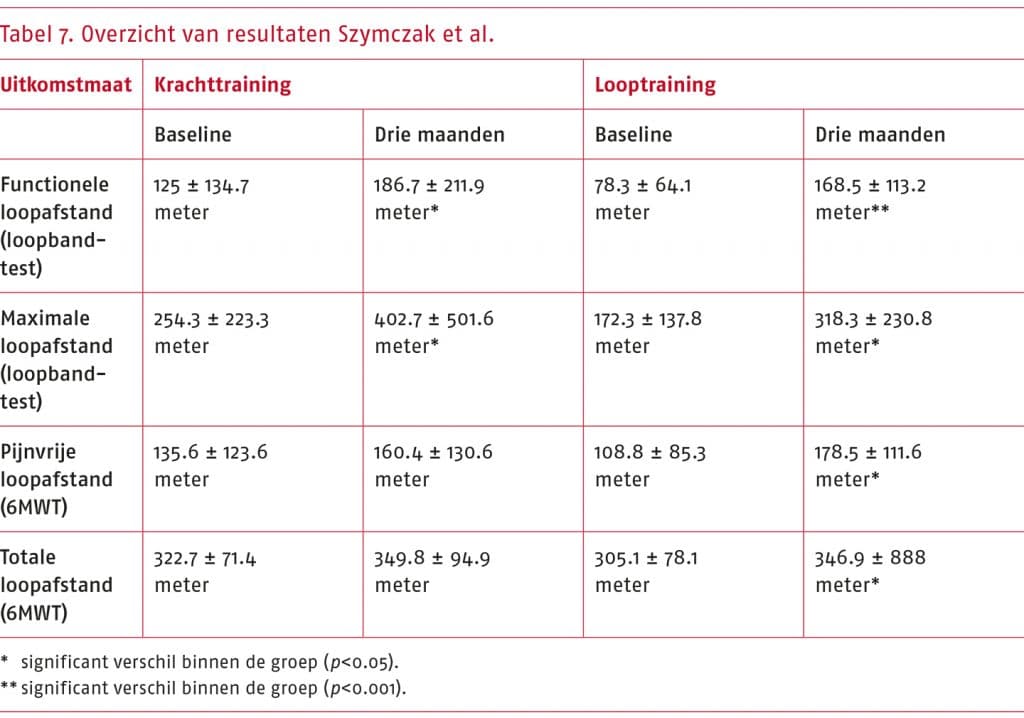
Gardner et al.
In de RCT van Gardner et al. is de effectiviteit van gesuperviseerde krachttraining vergeleken met die van zowel gesuperviseerde als niet-gesuperviseerde looptraining op fysiek functioneren en kwaliteit van leven na drie maanden (gemeten met de WIQ voor fysiek functioneren en de SF-36 voor kwaliteit van leven) (Gardner, 2014). De studie rapporteerde geen data (cijfermatige resultaten) met betrekking tot deze resultaten. Echter, de studie beschrijft wel dat de verschilscores significant verschillend waren tussen de groepen. In beide looptraininggroepen werd een significante verbetering (p<0.05) binnen de groepen gevonden op de WIQ en SF-36 physical functioning. Deze verschilscores waren groter dan de verschilscores in de krachttraininggroep (p<0.05). Deze bevindingen bevestigen de niet-significante resultaten van het systematische literatuuronderzoek op fysiek functioneren gemeten met de functionele en maximale loopafstand (loopbandtest) en pijnvrije loopafstand (6MWT). Ook bevestigen deze bevindingen de niet-significante resultaten van het literatuuronderzoek op kwaliteit van leven gemeten met de SF-36 physical functioning. De bevindingen zijn tegengesteld aan de significante resultaten van het literatuuronderzoek op fysiek functioneren gemeten met de totale loopafstand (6MWT).
Van Schaardenburgh et al.
In de RCT van Van Schaardenburgh et al. is de effectiviteit van niet-gesuperviseerde krachttraining vergeleken met die van niet-gesuperviseerde looptraining op fysiek functioneren en kwaliteit van leven na acht weken (gemeten als maximale loopafstand met de 6MWT voor fysiek functioneren en de SF-36 voor kwaliteit van leven) (Van Schaardenburgh, 2017). Data worden gepresenteerd als gemiddelde ± SEM (zie tabel 8). P-waarden van verschillen tussen groepen worden niet gerapporteerd, waardoor de bevindingen van deze studie niet direct te vergelijken zijn met de bevindingen van het systematische literatuuronderzoek.
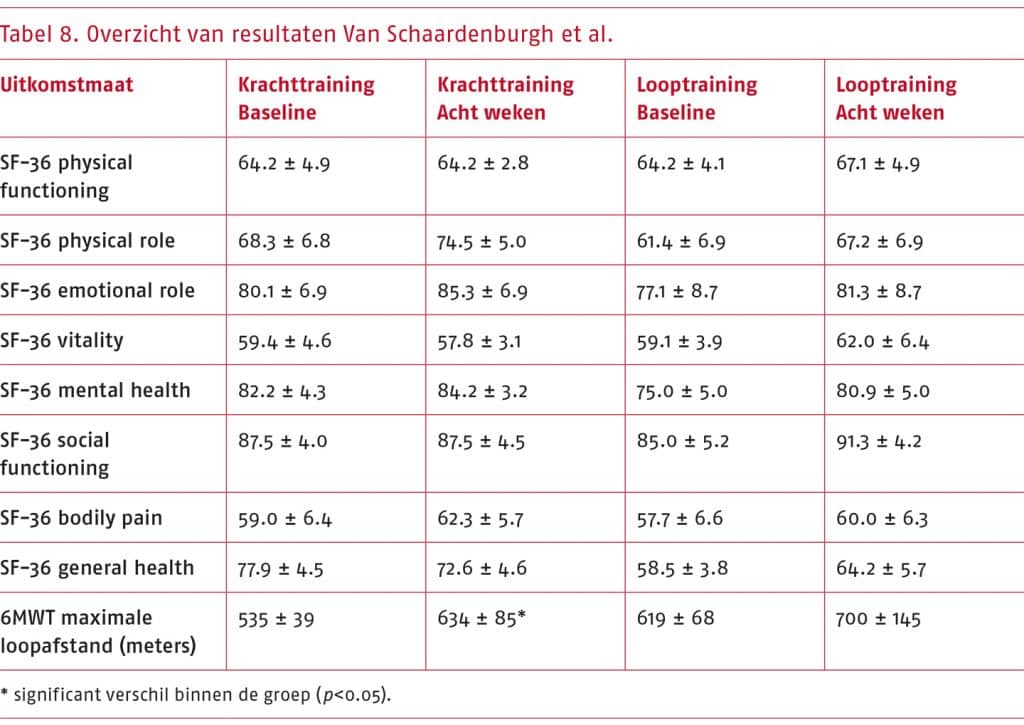
Park et al.
In de RCT van Park et al. is de effectiviteit van warmwatertraining vergeleken met die van gesuperviseerde looptraining op fysiek functioneren na drie maanden (gemeten als pijnvrije en totale loopafstand met de 6MWT) (Park, 2020). De studie rapporteerde geen data (cijfermatige resultaten) met betrekking tot deze resultaten. Echter, de studie beschrijft wel dat de 6MWT totale en pijnvrije loopafstand significant (p<0.05) verbeterden in beide groepen, waarbij de verbetering in de warmwatertraininggroep significant groter was (p<0.05) dan de verbetering in de looptraininggroep. Deze bevindingen bevestigen deels de resultaten van het systematische literatuuronderzoek, dat voor de totale loopafstand ook een significant grotere verbetering vond in het voordeel van andere vormen van beweeginterventies. Echter, op de pijnvrije loopafstand vond het literatuuronderzoek een niet-significant grotere verbetering in het voordeel van looptraining.
Salisbury et al.
In de RCT van Salisbury et al. is de effectiviteit van gesuperviseerde crosstraining vergeleken met die van gesuperviseerde looptraining op fysiek functioneren na drie maanden (gemeten als maximale en pijnvrije loopafstand met de 6MWT) (Salisbury, 2022). Data worden gepresenteerd als gemiddelde ± SD (zie tabel 9).
Het gemiddelde verschil tussen de groepen was voor zowel functionele loopafstand als maximale loopafstand niet-significant. Deze bevindingen bevestigen de resultaten van het systematische literatuuronderzoek, dat ook geen significante verschillen vond.
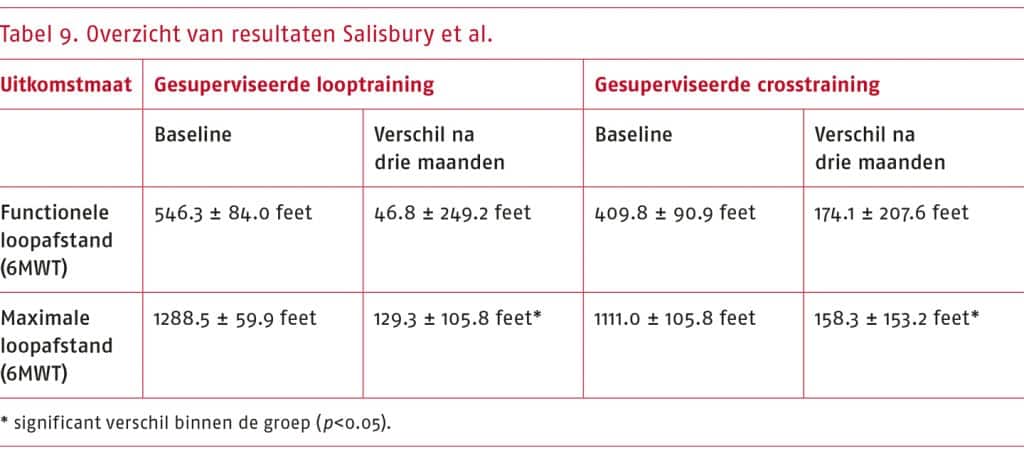
Van bewijs naar aanbeveling
Critera
Het onderdeel van bewijs naar aanbeveling bevat negen criteria, die hieronder worden opgesomd.
Gewenste effecten
Een overzicht van de resultaten uit de systematische literatuuranalyse wordt weergegeven in tabel 10. In bijlage C.8.1-7 (opent in nieuw tabblad)wordt een overzicht gegeven van zowel de resultaten van de individuele RCT’s als de resultaten van de literatuuranalyse. Zowel in de resultaten van de literatuuranalyse als in de resultaten van de individuele RCT’s worden tegengestelde effecten gevonden. Echter, vrijwel alle gevonden verschillen tussen de groepen zijn niet-significant en veelal niet-klinisch relevant.
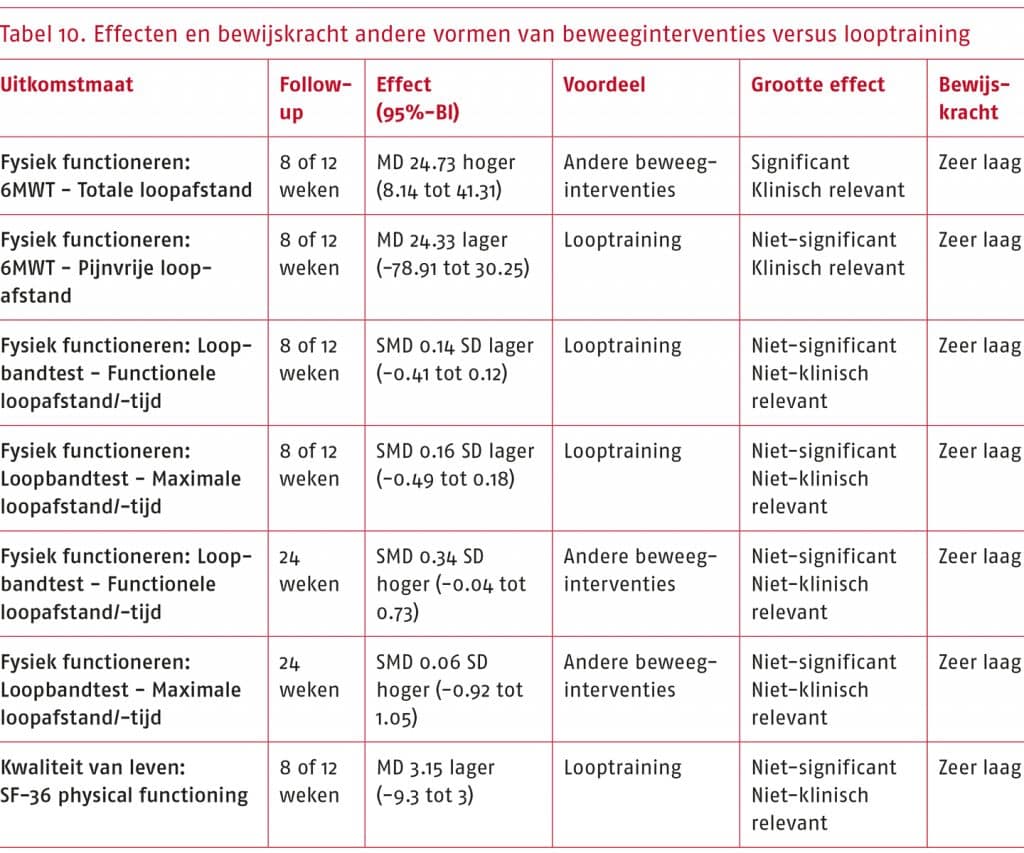
De werkgroep beoordeelt de gewenste effecten op het fysiek functioneren (gemeten als functionele of maximale loopafstand met de loopbandtest) van andere vormen van beweeginterventies ten opzichte van traditionele looptraining voor patiënten met sPAV als niet-significant en niet-klinisch relevant. De bevindingen laten zien dat zowel andere beweeginterventies (nordic walking, krachttraining, een combinatie van nordic walking en krachttraining, stretchoefeningen) als traditionele looptraining zorgen voor verbetering van het fysiek functioneren.
De werkgroep beoordeelt de gewenste effecten op het fysiek functioneren (gemeten als pijnvrije of totale loopafstand met de 6MWT) van andere vormen van beweeginterventies ten opzichte van traditionele looptraining voor patiënten met sPAV als klinisch relevant en significant voor de totale loopafstand, en klinisch relevant en niet-significant voor de pijnvrije loopafstand. De bevindingen zijn tegengesteld en laten zien dat andere beweeginterventies (nordic walking, krachttraining, een combinatie van nordic walking en krachttraining) zorgen voor een significante en klinisch relevante grotere verbetering van de totale loopafstand (6MWT), en dat traditionele looptraining zorgt voor een niet-significante maar wel klinisch relevante grotere verbetering van de pijnvrije loopafstand (6MWT). Zowel andere vormen van beweeginterventies als traditionele looptraining zorgen voor verbetering van het fysiek functioneren bij patiënten met sPAV.
De werkgroep beoordeelt de gewenste effecten op de kwaliteit van leven (gemeten met de SF-36 subschaal physical functioning) van andere vormen van beweeginterventies ten opzichte van traditionele looptraining voor patiënten met sPAV als niet-significant en niet-klinisch relevant. De bevindingen laten zien dat zowel andere beweeginterventies (nordic walking, krachttraining of warmwatertraining) als traditionele looptraining zorgen voor verbetering van de kwaliteit van leven (SF-36 physical functioning) bij patiënten met sPAV.
De werkgroep geeft aan dat het aannemelijk is dat zowel het inzetten van andere vormen van beweeginterventies (nordic walking, krachttraining, crosstraining, fietsen, handfietsen, stretchoefeningen, warmwatertraining) als traditionele looptraining waardevolle gewenste effecten heeft om het fysiek functioneren en de kwaliteit van leven bij patiënten met sPAV te verbeteren.
Ongewenste effecten
De werkgroep beoordeelt de kans op ongewenste effecten van andere vormen van beweeginterventies ten opzichte van traditionele looptraining voor patiënten met sPAV als klein. Alhoewel slechts drie van de veertien studies informatie rapporteren over ongewenste effecten, beoordeelt de werkgroep dat zowel het uitvoeren van andere vormen van beweeginterventies als traditionele looptraining voor patiënten met sPAV veilig is. De drie studies rapporteren geen verschillen tussen andere beweeginterventies en looptraining op het gebied van ongewenste effecten.
Daarnaast is door Gommans et al. uitvoerig onderzoek gedaan naar de veiligheid van gesuperviseerde beweeginterventies voor patiënten met sPAV, waarbij werd gekeken naar de complicatieratio (aantal ongewenste effecten per aantal trainingsuren) (Gommans, 2015). Deze systematische review includeerde 74 artikelen en rapporteerde een complicatieratio van één ongewenst voorval per 10.340 trainingsuren. Interventies van geïncludeerde artikelen bestonden uit looptraining, krachttraining, handfietsen, nordic walking, circuittraining en gecombineerde interventies. Gommans et al. concluderen dat gesuperviseerde beweeginterventies veilig zijn met een buitengewoon lage complicatieratio. De werkgroep beoordeelt dat deze studie aantoont dat trainen met begeleiding van een fysio- of oefentherapeut, onafhankelijk of het looptraining of een andere vorm van een beweeginterventie betreft, veilig en daarmee verantwoord is.
De werkgroep wil benadrukken dat iedere patiënt zorgvuldige monitoring en daarmee een bepaalde mate van begeleiding van een fysio- of oefentherapeut moet krijgen om de veiligheid te kunnen garanderen. Dit kan variëren van trainen met supervisie in de praktijkruimte van de therapeut, tot zelfstandig trainen met supervisie van de therapeut op afstand.
Kwaliteit van bewijs
De werkgroep beoordeelt de bewijskracht van de gewenste effecten als zeer laag voor patiënten met sPAV op de uitkomst fysiek functioneren (gemeten als de totale en pijnvrije loopafstand met de 6MWT en de functionele en maximale loopafstand met de loopbandtest) en kwaliteit van leven (gemeten met de SF-36 physical functioning). Het is hierbij van belang om rekening te houden met het feit dat de bewijskracht met name is afgewaardeerd als gevolg van de gevonden heterogeniteit in interventies en het risico op vertekening door de individuele studiekwaliteit en door de kleine onderzoekspopulaties.
Waarden en voorkeuren van patiënten
De werkgroep is tot het oordeel gekomen dat patiënten zeer grote waarde hechten aan de gekozen trainingsvorm en dat daar weinig variatie in zit tussen patiënten. De werkgroep beoordeelt dat er veel variatie bestaat tussen patiënten over de waardering van verschillende trainingsvormen, zoals looptraining of andere beweeginterventies. Het zal per patiënt verschillend zijn wat die voorkeuren zijn.
Dit wordt ondersteund door een achterbanraadpleging (n=60 patiënten met sPAV) van Stichting Harteraad. Uit de resultaten van deze raadpleging blijkt dat 52% van de patiënten de voorkeur geeft aan looptraining, 42% de voorkeur geeft aan een andere vorm van beweging dan lopen, en 7% geen specifieke voorkeur heeft. Redenen waarom patiënten een voorkeur hebben voor looptraining zijn de mogelijkheid om dit makkelijk in het dagelijks leven in te passen, het gemak van de training en de meetbaarheid van de progressie. Redenen waarom patiënten een voorkeur hebben voor andere beweeginterventies zijn afkeer voor lopen (met pijn), voorkeur voor afwisseling van verschillende vormen van beweging, en het langer vol kunnen houden van andere beweeginterventies vergeleken met lopen.
Balans gewenste en ongewenste effecten
De werkgroep is tot het oordeel gekomen dat de gewenste effecten van het aanbieden van andere vormen van beweeginterventies als alternatief voor traditionele looptraining zeker de ongewenste effecten overtreffen.
De motivatie hiervoor is:
- Zowel looptraining als andere vormen van beweeginterventies hebben positieve effecten op het fysiek functioneren en de kwaliteit van leven van patiënten met sPAV. Uit de effecten en de bewijskracht vanuit de literatuur, waarin beide interventies met elkaar worden vergeleken, blijkt geen duidelijke voorkeur voor een van de interventies. Andere vormen van beweeginterventies zijn daarmee een geschikt alternatief voor traditionele looptraining, met vergelijkbare gewenste effecten zonder relevante ongewenste effecten.
- Er zijn geen aanwijzingen dat andere vormen van beweeginterventies onveiliger zijn dan traditionele looptraining bij patiënten met sPAV.
- Patiënten met sPAV hebben verschillende voorkeuren voor de vorm van beweging en hechten veel waarde aan het kunnen kiezen tussen verschillende beweeginterventies. Dit maakt dat vanuit patiëntperspectief geen generieke voorkeur bestaat voor looptraining of andere vormen van beweeginterventies.
- De werkgroep verwacht dat het aanpassen van de trainingsvorm aan de voorkeuren van de patiënt, en dus zowel looptraining als andere vormen van beweeginterventies als trainingsvorm aanbieden, een positieve invloed kan hebben op therapietrouw, motivatie en zelfmanagement, wat weer kan bijdragen aan mogelijk positievere effecten van training (Daley, 2003; Lin, 2019; Parfitt, 2004).
Economische overwegingen en kosteneffectiviteit
De werkgroep beoordeelt de benodigde middelen voor looptraining ten opzichte van andere vormen van beweeginterventies als vergelijkbaar. Zowel looptraining als andere beweeginterventies kunnen wisselend van aard zijn en variëren van met supervisie trainen in een oefenruimte van de therapeut, tot zelfstandig trainen, waar materialen of lidmaatschappen voor nodig kunnen zijn.
Gesuperviseerde beweegtraining is een aangetoond kosteneffectieve behandeling (Fokkenrood, 2014; van Asselt, 2011; van den Houten, 2016b). De werkgroep vindt het aannemelijk dat zowel looptraining als andere beweeginterventies onder gesuperviseerde beweegtraining vallen, omdat beide interventies bestaan uit trainen met een bepaalde mate van supervisie door een fysio- of oefentherapeut. De werkgroep beoordeelt beide interventies qua kosteneffectiviteit dan ook gelijk aan elkaar.
De werkgroep beoordeelt dat het aanbieden van andere vormen van beweeginterventies naast looptraining geen directe economische impact heeft. Het kiezen voor looptraining of andere beweeginterventies zal volgens de werkgroep geen invloed hebben op het aantal therapieafspraken en voor de invulling van de interventie bestaat geen economisch gewin op zorgkosten. Door de trainingsvorm aan te laten sluiten op de voorkeuren van de patiënt verwacht de werkgroep dat effecten van therapie mogelijk vergroot worden (door o.a. hogere motivatie en therapietrouw), wat een positief effect kan hebben op het voorkomen van invasieve behandelingen, het verlagen van zorggebruik en daarmee het beperken van zorgkosten.
Gelijkheid
De werkgroep verwacht dat het aanbieden van andere vormen van beweeginterventies naast looptraining zal leiden tot een mogelijke toename van de gezondheidsgelijkheid.
Uit de knelpuntenanalyse onder therapeuten en uit de literatuur komt naar voren dat men bezorgd is dat het toepassen van samen beslissen (zoals het aanbieden van andere beweeginterventies naast looptraining) een risico vormt voor de gezondheidsgelijkheid, door de gedachte dat samen beslissen meer waardevol is voor hoger opgeleide personen, die beter in staat zijn om op te komen voor hun behoeften en een hoger niveau van gezondheidsvaardigheden hebben (Coulter, 2011; Legare, 2008). Een systematic review van Durand et al. laat echter zien dat samen beslissen juist leidt tot een toename van gezondheidsgelijkheid, mits de informatievoorziening wordt aangepast aan de behoeften van de individuele patiënt (Durand, 2014).
De werkgroep beoordeelt dat het aanbieden van andere beweeginterventies als alternatief voor looptraining zorgt voor een betere aansluiting van de zorg op de wensen en mogelijkheden van de individuele patiënt met sPAV (en mogelijke comorbiditeiten) en daarmee voor een betere aansluiting van de zorg op een grotere groep patiënten (inclusieve zorg).
Aanvaardbaarheid
De werkgroep verwacht dat het aanbieden van andere vormen van beweeginterventies naast looptraining door alle belangrijke stakeholders zal worden geaccepteerd.
Ondanks dat gesuperviseerde looptraining momenteel als primaire behandeling geldt binnen de zorg voor patiënten met sPAV in Nederland, verwacht de werkgroep dat alle stakeholders de gewenste variatie die ontstaat door het aanbieden van andere vormen van beweeginterventies, aanmoedigen.
Haalbaarheid
De implementatie van het aanbieden van andere vormen van beweeginterventies naast looptraining wordt door de werkgroep als realistisch beoordeeld. De norm is dat een beweeginterventie wordt aangeboden waarin altijd een bepaalde mate van supervisie door een fysio-/oefentherapeut aanwezig is. Hierbij kan in samenspraak met de patiënt worden bepaald, afhankelijk van de individuele wensen en doelen, welke beweeginterventie(s) worden ingezet. Het aanbieden van andere beweeginterventies dan looptraining kan betekenen dat therapeuten, patiënten of andere stakeholders, zoals huisartsen en vaatchirurgen, gewoontes moeten doorbreken waarin looptraining als enige mogelijke trainingsvorm wordt gezien.
Eventuele additionele overwegingen
De werkgroep is van mening dat de volgende overwegingen ook van belang zijn bij het aanbieden van andere vormen van beweeginterventies naast looptraining:
- Het is van belang dat de therapeut altijd samen met de patiënt de voortgang van de behandeling evalueert (door inzet van gestandaardiseerde meetinstrumenten (opent in nieuw tabblad)).
- Het is van belang dat de therapeut bij het aanbieden van en voorlichten over zowel looptraining als andere vormen van beweeginterventies rekening houdt met de behandeldoelen van de patiënt en de bijbehorende specificiteit van de training. De gekozen beweeginterventie moet afgestemd zijn op de mogelijkheden en wensen van de individuele patiënt en moet kunnen zorgen voor de benodigde trainingsprikkel bij de patiënt, zodat het boeken van progressie mogelijk is.
- Bij patiënten met sPAV kunnen comorbiditeiten aanwezig zijn die een beperking opleveren bij het fysiek functioneren of de trainbaarheid. Het is van belang dat de therapeut bij het aanbieden van andere vormen van beweeginterventies rekening houdt met beweegvormen die aansluiten bij andere fysio-/oefentherapeutische richtlijnen gericht op die mogelijke comorbiditeiten (denk aan: coronaire hartaandoeningen, chronisch hartfalen, COPD, CVA of diabetes mellitus type 2).
- Bij het aanbieden van zowel looptraining als andere vormen van beweeginterventies blijft een belangrijke rol weggelegd voor de therapeut om ziekte-inzicht en zelfmanagement van de patiënt te bevorderen. Ook wanneer wordt gekozen voor andere vormen van beweeginterventies kan het bijvoorbeeld belangrijk zijn dat een patiënt inzicht krijgt in en ervaringen opdoet met het lopen in relatie tot ADL-activiteiten.
- Het is van belang dat patiënten positieve ervaringen opdoen met beweging. Training of beweging moet niet met tegenzin worden uitgevoerd; het streven moet zijn dat de ervaringen van patiënten met het bewegen de verwachtingen overtreffen, om zo optimale resultaten te behalen. Daarbij kan het van meerwaarde zijn om andere vormen van beweeginterventies aan te bieden naast looptraining.
- De ingezette beweeginterventie(s) kan (kunnen) altijd heroverwogen worden gedurende het behandeltraject, dit kan bijvoorbeeld afhankelijk zijn van de voortgang van de behandeling of van de voorkeuren en wensen van de patiënt.
Kennislacunes
- Het is aangetoond dat gesuperviseerde looptraining de eerste-keuzebehandeling moet zijn voor patiënten met sPAV, wanneer looptraining wordt vergeleken met een invasieve (dotter/bypass) behandeling of met een behandeling die enkel bestaat uit het ‘advies om te gaan lopen’ (Fakhry, 2018; van den Houten, 2016b; van den Houten, 2019). Het is echter onbekend of andere vormen van beweeginterventies hetzelfde effect hebben als looptraining, wanneer deze vergeleken worden met een invasieve behandeling of loopadvies.
- Er zijn geen studies gevonden die resultaten hebben beschreven op de uitkomstmaten ‘mate van pijn’, ‘levensverwachting’ en ‘arbeidsparticipatie’. Het is daarom onbekend wat de effectiviteit is van traditionele looptraining versus andere vormen van beweeginterventies op deze uitkomstmaten.
- De huidige module heeft zich gefocust op het onderzoeken van de effectiviteit van andere vormen van beweeginterventies ten opzichte van looptraining. Het is echter ook relevant om te onderzoeken wat de effectiviteit is van een gecombineerde beweeginterventie (zoals lopen en krachttraining) versus een mono-interventie (zoals alleen looptraining).
- De kwaliteit van bewijs is grotendeels op zeer lage kwaliteit van bewijs uitgekomen. Dit is te verklaren door de diversiteit van de interventies en door te kleine onderzoekspopulaties. Om gericht een uitspraak te kunnen doen over de effectiviteit van andere vormen van beweeginterventies vergeleken met looptraining dienen meer studies met vergelijkbare beweeginterventies uitgevoerd te worden bij patiënten met sPAV.
Aboyans, V., Ricco, J. B., Bartelink, M. E. L., Bjorck, M., Brodmann, M., Cohnert, T., Collet, J. P., Czerny, M., De Carlo, M., Debus, S., Espinola-Klein, C., Kahan, T., Kownator, S., Mazzolai, L., Naylor, A. R., Roffi, M., Rother, J., Sprynger, M., Tendera, M., et al. (2018). 2017 ESC Guidelines on the Diagnosis and Treatment of Peripheral Arterial Diseases, in collaboration with the European Society for Vascular Surgery (ESVS): Document covering atherosclerotic disease of extracranial carotid and vertebral, mesenteric, renal, upper and lower extremity arteriesEndorsed by: the European Stroke Organization (ESO)The Task Force for the Diagnosis and Treatment of Peripheral Arterial Diseases of the European Society of Cardiology (ESC) and of the European Society for Vascular Surgery (ESVS). Eur Heart J, 39(9), 763-816. https://doi.org/10.1093/eurheartj/ehx095
Bae, E., Choi, S. E., Lee, H., Shin, G.& Kang, D. (2020). Validity of EQ-5D utility index and minimal clinically important difference estimation among patients with chronic obstructive pulmonary disease. BMC Pulm Med, 20(1), 73. https://doi.org/10.1186/s12890-020-1116-z
Bartelink, M. E. L., Elsman, B. H. P., Oostindjer, A., Stoffers, H. E. J. H., Wiersma, T. J.& Geraets, J. J. X. R. (2014). NHG-Standaard Perifeer arterieel vaatlijden. Huisarts Wet, 57(2), 81-81.
Bronas, U. G., Treat-Jacobson, D.& Leon, A. S. (2011). Comparison of the effect of upper body-ergometry aerobic training vs treadmill training on central cardiorespiratory improvement and walking distance in patients with claudication. J Vasc Surg, 53(6), 1557-1564. https://doi.org/10.1016/j.jvs.2011.01.077
Bulinska, K., Kropielnicka, K., Jasinski, T., Wojcieszczyk-Latos, J., Pilch, U., Dabrowska, G., Skorkowska-Telichowska, K., Kalka, D., Zywar, K., Paszkowski, R., Wozniewski, M., Szuba, A.& Jasinski, R. (2016). Nordic pole walking improves walking capacity in patients with intermittent claudication: a randomized controlled trial. Disabil Rehabil, 38(13), 1318-1324. https://doi.org/10.3109/09638288.2015.1077398
Chehuen, M., Cucato, G. G., Carvalho, C. R. F., Ritti-Dias, R. M., Wolosker, N., Leicht, A. S.& Forjaz, C. L. M. (2017). Walking training at the heart rate of pain threshold improves cardiovascular function and autonomic regulation in intermittent claudication: A randomized controlled trial. J Sci Med Sport, 20(10), 886-892. https://doi.org/10.1016/j.jsams.2017.02.011
Collins, E. G., O’Connell, S., McBurney, C., Jelinek, C., Butler, J., Reda, D., Gerber, B. S., Hurt, C.& Grabiner, M. (2012). Comparison of walking with poles and traditional walking for peripheral arterial disease rehabilitation. J Cardiopulm Rehabil Prev, 32(4), 210-218. https://doi.org/10.1097/HCR.0b013e31825828f4
Conijn, A. P., Jonkers, W., Rouwet, E. V., Vahl, A. C., Reekers, J. A.& Koelemay, M. J. (2015). Introducing the Concept of the Minimally Important Difference to Determine a Clinically Relevant Change on Patient-Reported Outcome Measures in Patients with Intermittent Claudication. Cardiovasc Intervent Radiol, 38(5), 1112-1118. https://doi.org/10.1007/s00270-015-1060-0
Coulter, A., Collins, A.& King’s Fund, C. (2011). Making shared decision-making a reality : no decision about me, without me. King’s Fund.
Cucato, G. G., Chehuen Mda, R., Costa, L. A., Ritti-Dias, R. M., Wolosker, N., Saxton, J. M.& Forjaz, C. L. (2013). Exercise prescription using the heart of claudication pain onset in patients with intermittent claudication. Clinics (Sao Paulo), 68(7), 974-978. https://doi.org/10.6061/clinics/2013(07)14
Daley, A. M., IW. (2003). Preferred exercise mode and affective responses in physically active adults. Psychology of Sport and Exercise, 4(4), 347-356.
Durand, M. A., Carpenter, L., Dolan, H., Bravo, P., Mann, M., Bunn, F.& Elwyn, G. (2014). Do interventions designed to support shared decision-making reduce health inequalities? A systematic review and meta-analysis. PLoS One, 9(4), e94670. https://doi.org/10.1371/journal.pone.0094670
Dziubek, W., Stefanska, M., Bulinska, K., Barska, K., Paszkowski, R., Kropielnicka, K., Jasinski, R., Rachwalik, A., Wozniewski, M.& Szuba, A. (2020). Effects of Physical Rehabilitation on Spatiotemporal Gait Parameters and Ground Reaction Forces of Patients with Intermittent Claudication. J Clin Med, 9(9). https://doi.org/10.3390/jcm9092826
Elwyn, G., Durand, M. A., Song, J., Aarts, J., Barr, P. J., Berger, Z., Cochran, N., Frosch, D., Galasinski, D., Gulbrandsen, P., Han, P. K. J., Harter, M., Kinnersley, P., Lloyd, A., Mishra, M., Perestelo-Perez, L., Scholl, I., Tomori, K., Trevena, L., et al. (2017). A three-talk model for shared decision making: multistage consultation process. BMJ, 359, j4891. https://doi.org/10.1136/bmj.j4891
Fakhry, F., Fokkenrood, H. J., Spronk, S., Teijink, J. A., Rouwet, E. V.& Hunink, M. G. M. (2018). Endovascular revascularisation versus conservative management for intermittent claudication. Cochrane Database Syst Rev, 3(3), CD010512. https://doi.org/10.1002/14651858.CD010512.pub2
Farrar, J. T., Young, J. P., Jr., LaMoreaux, L., Werth, J. L.& Poole, M. R. (2001). Clinical importance of changes in chronic pain intensity measured on an 11-point numerical pain rating scale. Pain, 94(2), 149-158. https://doi.org/10.1016/S0304-3959(01)00349-9
Fokkenrood, H. J., Scheltinga, M. R., Koelemay, M. J., Breek, J. C., Hasaart, F., Vahl, A. C.& Teijink, J. A. (2014). Significant savings with a stepped care model for treatment of patients with intermittent claudication. Eur J Vasc Endovasc Surg, 48(4), 423-429. https://doi.org/10.1016/j.ejvs.2014.04.020
Gardner, A. W., Parker, D. E., Montgomery, P. S.& Blevins, S. M. (2014). Step-monitored home exercise improves ambulation, vascular function, and inflammation in symptomatic patients with peripheral artery disease: a randomized controlled trial. J Am Heart Assoc, 3(5), e001107. https://doi.org/10.1161/JAHA.114.001107
Gerhard-Herman, M. D., Gornik, H. L., Barrett, C., Barshes, N. R., Corriere, M. A., Drachman, D. E., Fleisher, L. A., Fowkes, F. G., Hamburg, N. M., Kinlay, S., Lookstein, R., Misra, S., Mureebe, L., Olin, J. W., Patel, R. A., Regensteiner, J. G., Schanzer, A., Shishehbor, M. H., Stewart, K. J., et al. (2017). 2016 AHA/ACC Guideline on the Management of Patients With Lower Extremity Peripheral Artery Disease: Executive Summary: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. Circulation, 135(12), e686-e725. https://doi.org/10.1161/CIR.0000000000000470
Gommans, L. N., Fokkenrood, H. J., van Dalen, H. C., Scheltinga, M. R., Teijink, J. A.& Peters, R. J. (2015). Safety of supervised exercise therapy in patients with intermittent claudication. J Vasc Surg, 61(2), 512-518 e512. https://doi.org/10.1016/j.jvs.2014.08.070
Higgins, J. P., Savović, J., Page, M. J., Elbers, R. G.& Sterne, J. A. (2019). Assessing risk of bias in a randomized trial. Cochrane handbook for systematic reviews of interventions, 205-228.
Jansen, S. C., Abaraogu, U. O., Lauret, G. J., Fakhry, F., Fokkenrood, H. J.& Teijink, J. A. (2020). Modes of exercise training for intermittent claudication. Cochrane Database Syst Rev, 8(8), CD009638. https://doi.org/10.1002/14651858.CD009638.pub3
Kropielnicka, K., Dziubek, W., Bulinska, K., Stefanska, M., Wojcieszczyk-Latos, J., Jasinski, R., Pilch, U., Dabrowska, G., Skorkowska-Telichowska, K., Kalka, D., Janus, A., Zywar, K., Paszkowski, R., Rachwalik, A., Wozniewski, M.& Szuba, A. (2018). Influence of the Physical Training on Muscle Function and Walking Distance in Symptomatic Peripheral Arterial Disease in Elderly. Biomed Res Int, 2018, 1937527. https://doi.org/10.1155/2018/1937527
Langendam, M. K., T. . (2022). Toepassen GRADE voor interventies tool. https://nl.gradeworkinggroup.org/docs/Tool_GRADE_voor_interventies_juni2022_final.pdf
Legare, F., Ratte, S., Gravel, K.& Graham, I. D. (2008). Barriers and facilitators to implementing shared decision-making in clinical practice: update of a systematic review of health professionals’ perceptions. Patient Educ Couns, 73(3), 526-535. https://doi.org/10.1016/j.pec.2008.07.018
Lin, E., Nguyen, C. H.& Thomas, S. G. (2019). Completion and adherence rates to exercise interventions in intermittent claudication: Traditional exercise versus alternative exercise – a systematic review. Eur J Prev Cardiol, 26(15), 1625-1633. https://doi.org/10.1177/2047487319846997
McDermott, M. M., Tian, L., Criqui, M. H., Ferrucci, L., Conte, M. S., Zhao, L., Li, L., Sufit, R., Polonsky, T. S., Kibbe, M. R., Greenland, P., Leeuwenburgh, C.& Guralnik, J. M. (2021). Meaningful change in 6-minute walk in people with peripheral artery disease. J Vasc Surg, 73(1), 267-276 e261. https://doi.org/10.1016/j.jvs.2020.03.052
Meneses, A. L., de Lima, G. H., Forjaz, C. L., Lima, A. H., Silva, G. Q., Cucato, G. G., Rodrigues, S. L., Wolosker, N., Marucci Mde, F.& Dias, R. M. (2011). Impact of a supervised strength training or walking training over a subsequent unsupervised therapy period on walking capacity in patients with claudication. J Vasc Nurs, 29(2), 81-86. https://doi.org/10.1016/j.jvn.2011.01.002
Merry, A. H. H., Teijink, J. A. W., Jongert, M. W. A., Poelgeest, A., Van Der Voort, S. S. E. M., Bartelink, M. E. L., Stoffers, H. E. J. H., Brooymans, F., Hendriks, H. J. M.& De Bie, R. A. (2014). KNGF-richtlijn Symptomatisch perifeer arterieel vaatlijden. www.kngfrichtlijnen.nl.
Nordanstig, J., Pettersson, M., Morgan, M., Falkenberg, M.& Kumlien, C. (2017). Assessment of Minimum Important Difference and Substantial Clinical Benefit with the Vascular Quality of Life Questionnaire-6 when Evaluating Revascularisation Procedures in Peripheral Arterial Disease. Eur J Vasc Endovasc Surg, 54(3), 340-347. https://doi.org/10.1016/j.ejvs.2017.06.022
Parfitt, G. G., C. (2004). The effect of choice of exercise mode on psychological responses. Psychology of Sport and Exercise, 5(2), 111-117.
Park, S. Y., Wong, A., Son, W. M.& Pekas, E. J. (2020). Effects of heated water-based versus land-based exercise training on vascular function in individuals with peripheral artery disease. J Appl Physiol (1985), 128(3), 565-575. https://doi.org/10.1152/japplphysiol.00744.2019
Ritti-Dias, R. M., Wolosker, N., de Moraes Forjaz, C. L., Carvalho, C. R., Cucato, G. G., Leao, P. P.& de Fatima Nunes Marucci, M. (2010). Strength training increases walking tolerance in intermittent claudication patients: randomized trial. J Vasc Surg, 51(1), 89-95. https://doi.org/10.1016/j.jvs.2009.07.118
Salisbury, D. L., Swanson, K., Brown, R. J.& Treat-Jacobson, D. (2022). Total body recumbent stepping vs treadmill walking in supervised exercise therapy: A pilot study. Vasc Med, 27(2), 150-157. https://doi.org/10.1177/1358863X211068888
Sanderson, B., Askew, C., Stewart, I., Walker, P., Gibbs, H.& Green, S. (2006). Short-term effects of cycle and treadmill training on exercise tolerance in peripheral arterial disease. J Vasc Surg, 44(1), 119-127. https://doi.org/10.1016/j.jvs.2006.03.037
Society for Vascular Surgery Lower Extremity Guidelines Writing, G., Conte, M. S., Pomposelli, F. B., Clair, D. G., Geraghty, P. J., McKinsey, J. F., Mills, J. L., Moneta, G. L., Murad, M. H., Powell, R. J., Reed, A. B., Schanzer, A., Sidawy, A. N.& Society for Vascular, S. (2015). Society for Vascular Surgery practice guidelines for atherosclerotic occlusive disease of the lower extremities: management of asymptomatic disease and claudication. J Vasc Surg, 61(3 Suppl), 2S-41S. https://doi.org/10.1016/j.jvs.2014.12.009
Spafford, C., Oakley, C.& Beard, J. D. (2014). Randomized clinical trial comparing Nordic pole walking and a standard home exercise programme in patients with intermittent claudication. Br J Surg, 101(7), 760-767. https://doi.org/10.1002/bjs.9519
Stiggelbout, A. M., Pieterse, A. H.& De Haes, J. C. (2015). Shared decision making: Concepts, evidence, and practice. Patient Educ Couns, 98(10), 1172-1179. https://doi.org/10.1016/j.pec.2015.06.022
Szymczak, M., Oszkinis, G.& Majchrzycki, M. (2016). The Impact of Walking Exercises and Resistance Training upon the Walking Distance in Patients with Chronic Lower Limb Ischaemia. Biomed Res Int, 2016, 7515238. https://doi.org/10.1155/2016/7515238
Treat-Jacobson, D., Bronas, U. G.& Leon, A. S. (2009). Efficacy of arm-ergometry versus treadmill exercise training to improve walking distance in patients with claudication. Vasc Med, 14(3), 203-213. https://doi.org/10.1177/1358863X08101858
van Asselt, A. D., Nicolai, S. P., Joore, M. A., Prins, M. H., Teijink, J. A.& Exercise Therapy in Peripheral Arterial Disease Study, G. (2011). Cost-effectiveness of exercise therapy in patients with intermittent claudication: supervised exercise therapy versus a ‘go home and walk’ advice. Eur J Vasc Endovasc Surg, 41(1), 97-103. https://doi.org/10.1016/j.ejvs.2010.06.024
van den Houten, M. M., Gommans, L. N., van der Wees, P. J.& Teijink, J. A. (2016a). Minimally Important Difference of the Absolute and Functional Claudication Distance in Patients with Intermittent Claudication. Eur J Vasc Endovasc Surg, 51(3), 404-409. https://doi.org/10.1016/j.ejvs.2015.11.008
van den Houten, M. M., Lauret, G. J., Fakhry, F., Fokkenrood, H. J., van Asselt, A. D., Hunink, M. G.& Teijink, J. A. (2016b). Cost-effectiveness of supervised exercise therapy compared with endovascular revascularization for intermittent claudication. Br J Surg, 103(12), 1616-1625. https://doi.org/10.1002/bjs.10247
van den Houten, M. M. L., Hageman, D., Gommans, L. N. M., Kleijnen, J., Scheltinga, M. R. M.& Teijink, J. A. W. (2019). The Effect of Supervised Exercise, Home Based Exercise and Endovascular Revascularisation on Physical Activity in Patients With Intermittent Claudication: A Network Meta-analysis. Eur J Vasc Endovasc Surg, 58(3), 383-392. https://doi.org/10.1016/j.ejvs.2018.12.023
van der Horst, D. E. M., Garvelink, M. M., Bos, W. J. W., Stiggelbout, A. M.& Pieterse, A. H. (2023). For which decisions is Shared Decision Making considered appropriate? – A systematic review. Patient Educ Couns, 106, 3-16. https://doi.org/10.1016/j.pec.2022.09.015
Van Schaardenburgh, M., Wohlwend, M., Rognmo, O.& Mattsson, E. (2017). Calf raise exercise increases walking performance in patients with intermittent claudication. J Vasc Surg, 65(5), 1473-1482. https://doi.org/10.1016/j.jvs.2016.12.106
Wyrwich, K. W., Tierney, W. M., Babu, A. N., Kroenke, K.& Wolinsky, F. D. (2005). A comparison of clinically important differences in health-related quality of life for patients with chronic lung disease, asthma, or heart disease. Health Serv Res, 40(2), 577-591. A comparison of clinically important differences in health-related quality of life for patients with chronic lung disease, asthma, or heart disease – PubMed
Zatloukal, J., Ward, S., Houchen-Wolloff, L., Harvey-Dunstan, T.& Singh, S. (2019). The minimal important difference for the endurance shuttle walk test in individuals with chronic obstructive pulmonary disease following a course of pulmonary rehabilitation. Chronic Respiratory Disease, 16. https://doi.org/10.1177/1479973119853828
C.8.2 De keuze voor gesuperviseerde en/of zelfstandig uitgevoerde beweeginterventies
Beschrijving
Volg de aanbevelingen uit de KNGF-richtlijn ‘Zorg op afstand’ (opent in nieuw tabblad), voor de toepassing van zorg op afstand (bijvoorbeeld wanneer iemand hoofdzakelijk zelfstandig traint) binnen de fysio-/oefentherapeutische behandeling van patiënten met symptomatisch Perifeer Arterieel Vaatlijden (sPAV). Volg in alle overige gevallen (wanneer iemand hoofdzakelijk gesuperviseerd traint) de aanbevelingen uit de KNGF-richtlijn sPAV ‘Therapeutisch proces: Inleiding (opent in nieuw tabblad)’ .
| Definitie ‘Gesuperviseerde beweeginterventies’ en ‘Zelfstandig uitgevoerde beweeginterventies’ Binnen deze richtlijnmodule wordt gesproken over ‘gesuperviseerde beweeginterventies’ of ‘zelfstandig uitgevoerde beweeginterventies’. Onder gesuperviseerde beweeginterventies wordt verstaan: een beweeginterventie die de patiënt hoofdzakelijk uitvoert met directe begeleiding van de fysio-/oefentherapeut. Onder zelfstandig uitgevoerde beweeginterventies wordt verstaan: een beweeginterventie die een patiënt hoofdzakelijk zelfstandig (in de thuisomgeving) uitvoert met periodieke contactmomenten met de fysio-/oefentherapeut (bijvoorbeeld door middel van zorg op afstand). |
Uit de bevindingen van de beschikbare wetenschappelijke literatuur kan worden geconcludeerd dat gesuperviseerde beweeginterventies waarschijnlijk een groter gewenst effect hebben op het fysiek functioneren dan zelfstandig uitgevoerde beweeginterventies. Deze bevindingen sluiten aan bij de voorkeuren van patiënten en de klinische expertise van therapeuten. Echter, ook zelfstandig uitgevoerde beweeginterventies hebben relevante gewenste effecten op het fysiek functioneren en de kwaliteit van leven en kunnen daarmee een waardevolle behandeloptie zijn wanneer dit aansluit bij de mogelijkheden en behoeften van de individuele patiënt. De bevindingen binnen deze richtlijnmodule leiden niet tot nieuwe aanbevelingen ten opzichte van de huidige KNGF-richtlijn sPAV en de KNGF-richtlijn Zorg (opent in nieuw tabblad)op afstand. Daarom wordt in deze module geen aanbeveling gegeven voor één specifieke behandeloptie, maar wordt verwezen naar de bestaande KNGF-richtlijnen.
Aanleiding
Conform (inter)nationale richtlijnen is gesuperviseerde beweegtraining of looptraining de primair aanbevolen behandeling voor patiënten met symptomatisch Perifeer Arterieel Vaatlijden (sPAV) (Aboyans, 2018; Bartelink, 2014; Merry, 2014; Society for Vascular Surgery Lower Extremity Guidelines Writing, 2015). Desalniettemin zijn voor het vormgeven van het fysio-/oefentherapeutische behandelplan verschillende vormen en doseringen van beweeg- of looptraining mogelijk (Merry, 2014). Het behandelplan omvat daarmee meerdere beslissingen waarbij ruimte is voor samen beslissen. Dit is bij uitstek het geval bij beslissingen waarbij meerdere redelijke opties bestaan en de uiteindelijke keuze afhangt van de persoonlijke voorkeuren en waarden van de patiënt, of bij beslissingen waarbij de betrokkenheid en toewijding van de patiënt cruciaal zijn voor de uitvoering van de behandeling, zoals bij leefstijlkeuzes (van der Horst, 2023).
Uit de knelpuntenanalyse (gericht op samen beslissen) blijkt dat therapeuten vaak het gevoel hebben dat gesuperviseerde pijninducerende looptraining de primair in te zetten interventie moet zijn. Voor veel therapeuten is het onvoldoende duidelijk wat de voor- en nadelen van de verschillende mogelijke behandelopties zijn binnen de behandeling van patiënten met sPAV. Dit terwijl inzicht hebben in de beschikbare wetenschappelijke evidentie, en daarmee in de waarde van de verschillende behandelopties, juist van belang is voor het effectief toepassen van samen beslissen. Het aanbieden van deze kennis, naast de kennis uit de KNGF-richtlijn sPAV uit 2014 , kan fysio-/oefentherapeuten ondersteunen tijdens het samen beslissen, en helpen om patiënten met sPAV goed te laten participeren tijdens het proces van samen beslissen. Dit is vooral waardevol tijdens de option talk. Option talk, oftewel het optiegesprek, is een van de essentiële stappen in het proces van samen beslissen en omvat het informeren van de patiënt over de mogelijke behandelopties, inclusief bijbehorende voor- en nadelen, op basis van de beschikbare (of soms beperkte) wetenschappelijke kennis en klinische expertise (Elwyn, 2017; Stiggelbout, 2015).
Binnen deze module C.8.2 wordt ingegaan op de waarde van een zelfstandig uitgevoerde beweeginterventie ten opzichte van een gesuperviseerde beweeginterventie bij patiënten met sPAV. Binnen (inter)nationale richtlijnen is de primair aanbevolen interventie voor patiënten met sPAV gesuperviseerde training (Aboyans, 2018; Bartelink, 2014; Gerhard-Herman, 2017; Society for Vascular Surgery Lower Extremity Guidelines Writing, 2015). Echter, ook zelfstandig trainen kan waardevolle gewenste effecten hebben. Uit de knelpuntenanalyse blijkt dat het voor therapeuten onduidelijk is wat de waarde is van zelfstandig trainen en in welke gevallen dit een relevante behandeloptie is om aan te bieden ten opzichte van gesuperviseerd trainen. In de praktijk wordt vaak gekozen voor een gesuperviseerde beweeginterventie. Echter, soms sluit gesuperviseerde training niet goed aan bij de mogelijkheden en de hulpvraag van en/of de gewenste uitkomsten voor patiënten.
Om therapeuten inzicht te geven in de beschikbare wetenschappelijke evidentie is het van belang om aanbevelingen te formuleren voor de gewenste en ongewenste effecten van een zelfstandig uitgevoerde beweeginterventie ten opzichte van een gesuperviseerde beweeginterventie bij patiënten met sPAV. Hiertoe is de volgende uitgangsvraag geformuleerd:
Uitgangsvraag
Kan in plaats van een gesuperviseerde beweeginterventie ook gekozen worden voor een zelfstandig uitgevoerde beweeginterventie bij patiënten met sPAV?
Conclusies op basis van de literatuur
Op basis van de conclusies van de geselecteerde literatuur kunnen een aantal resultaten worden geformuleerd. Deze ‘Gestandaardiseerde formuleringen van de resultaten’ worden gevormd door de grootte van het effect en de bewijskracht te combineren en ze doen een uitspraak over de zekerheid van het bewijs dat in de literatuur is gevonden (Langendam & Kuijpers, 2022).
Cruciale uitkomstmaten:
- Een gesuperviseerde beweeginterventie resulteert waarschijnlijk in een grotere verbetering van het fysiek functioneren (gemeten als de functionele loopafstand en de maximale loopafstand met de loopbandtest) ten opzichte van een zelfstandig uitgevoerde beweeginterventie bij patiënten met sPAV.
Toelichting: Het geselecteerde systematische literatuuronderzoek beschrijft een statistisch significant en klinisch relevant positief effect op de functionele loopafstand (SMD 0.51 hoger) en een significant en niet-klinisch relevant positief effect op de maximale loopafstand (SMD 0.37 hoger) in het voordeel van een gesuperviseerde beweeginterventie. Zowel een zelfstandig uitgevoerde beweeginterventie als een gesuperviseerde beweeginterventie had positieve effecten op fysiek functioneren. De bewijskracht van deze resultaten is redelijk. Hierdoor zijn we redelijk zeker over het effect dat vanuit de literatuur is aangetoond.
- Het wetenschappelijke bewijs is zeer onzeker over het effect van een zelfstandig uitgevoerde beweeginterventie op fysiek functioneren (gemeten met de WIQ) ten opzichte van een gesuperviseerde beweeginterventie bij patiënten met sPAV.
Toelichting: Het geselecteerde systematische literatuuronderzoek beschrijft dat zowel trainen met supervisie als zelfstandig trainen positieve effecten heeft op zelf-gerapporteerd fysiek functioneren. Een niet-significant, niet-klinisch relevant effect (MD -5.00 lager) is gevonden op de WIQ (totaalscore) in het nadeel van gesuperviseerd trainen. De bewijskracht van de resultaten was zeer laag, waardoor we zeer onzeker zijn over het effect dat vanuit de literatuur is aangetoond.
- Het wetenschappelijke bewijs is zeer onzeker over het effect van een zelfstandig uitgevoerde beweeginterventie op kwaliteit van leven (gemeten met de SF-36) ten opzichte van een gesuperviseerde beweeginterventie bij patiënten met sPAV.
Toelichting: Het geselecteerde systematische literatuuronderzoek beschrijft dat zowel trainen met supervisie als zelfstandig trainen positieve effecten heeft op kwaliteit van leven. Een niet-significant, niet-klinisch relevant effect (MD 0.00) is gevonden op de SF-36 physical component summary, en een niet-significant, niet-klinisch relevant effect (MD 1.19 hoger in het voordeel van gesuperviseerd trainen) op de SF-36 mental component summary. De bewijskracht van de resultaten was zeer laag, waardoor we zeer onzeker zijn over het effect dat vanuit de literatuur is aangetoond.
- Slechts één studie rapporteerde resultaten over het fysiek functioneren gemeten met de 6MWT. In dit geval is ervoor gekozen om de resultaten narratief te beschrijven en is geen conclusie geformuleerd volgens de GRADE-methodiek.
- Het geselecteerde systematische literatuuronderzoek beschrijft geen sterfgevallen gerelateerd aan een van de beweeginterventies.
- Er zijn geen studies gevonden die resultaten hebben beschreven op de overige cruciale uitkomstmaten: mate van pijn of arbeidsparticipatie.
Belangrijke uitkomstmaten:
- Een van de geselecteerde studies beschrijft resultaten over ongewenste effecten gerelateerd aan een van de interventies. Deze studie vond geen ongewenste effecten.
Rationale van de aanbeveling
De werkgroep heeft besloten om geen nieuwe aanbeveling(en) te formuleren voor deze richtlijnmodule, maar te verwijzen naar de aanbevelingen in de bestaande KNGF-richtlijn sPAV en de KNGF-richtlijn Zorg op afstand. (opent in nieuw tabblad) Hierbij waren er een aantal criteria (zie Verantwoording; ‘Van bewijs naar aanbeveling’) die zwaar en minder zwaar hebben gewogen.
Uit de resultaten van het systematische literatuuronderzoek kan worden geconcludeerd dat gesuperviseerde beweeginterventies waarschijnlijk grotere gewenste effecten hebben op het fysiek functioneren op korte termijn (<1 jaar) ten opzichte van zelfstandig uitgevoerde beweeginterventies. We zijn zeer onzeker of de effecten van gesuperviseerde beweeginterventies dan wel die van zelfstandig trainen groter zijn op kwaliteit van leven. De resultaten suggereren dat zowel gesuperviseerde als zelfstandig uitgevoerde beweeginterventies mogelijk positieve effecten hebben op fysiek functioneren en kwaliteit van leven, maar dat de positieve effecten van gesuperviseerde beweeginterventies groter zijn.
Een achterbanraadpleging onder patiënten met sPAV laat zien dat patiënten grote waarde hechten aan gesuperviseerd trainen, maar dat variatie bestaat in de voorkeur en waardering van patiënten ten aanzien van gesuperviseerd of zelfstandig trainen.
De werkgroep beoordeelt dat de resultaten van het systematische literatuuronderzoek en de voorkeuren van patiënten laten zien dat zelfstandig uitgevoerde beweeginterventies een aanvulling kunnen zijn en in individuele gevallen een alternatief kunnen zijn binnen de fysio-/oefentherapeutische behandeling van patiënten met sPAV. Echter, de werkgroep benadrukt dat een gesuperviseerde beweeginterventie de eerste-keuzebehandeling zou moeten zijn.
De economische overwegingen en kosteneffectiviteit zijn gelijkwaardig voor gesuperviseerde beweeginterventies en zelfstandig uitgevoerde beweeginterventies. De werkgroep verwacht dat het aanbieden van zelfstandig uitgevoerde beweeginterventies als aanvulling op, of in individuele gevallen als alternatief voor, gesuperviseerde beweeginterventies kan zorgen voor een toename van de gezondheidsgelijkheid, doordat de aangeboden zorg beter kan worden afgestemd op de individuele patiënt (inclusieve zorg). De overige criteria van het proces van bewijs naar aanbeveling (aanvaardbaarheid en haalbaarheid) worden als niet-bezwaarlijk bevonden in het aanbieden van zelfstandig uitgevoerde beweeginterventies naast gesuperviseerde beweeginterventies, mits het zelfstandig trainen daadwerkelijk wordt aangevuld met adequate begeleiding en evaluatiemomenten.
Concluderend beoordeelt de werkgroep dat het wetenschappelijke bewijs en de overige criteria van het proces van bewijs naar aanbeveling niet leiden tot nieuwe aanbevelingen ten opzichte van de huidige KNGF-richtlijn sPAV en de KNGF-richtlijn Zorg op afstand.
Literatuur
Zoeken en selecteren
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende onderzoeksvraag:
- Wat is het effect van een zelfstandig uitgevoerde beweeginterventie ten opzichte van een gesuperviseerde beweeginterventie op het fysiek functioneren, de kwaliteit van leven, de mate van pijn, de levensverwachting en de arbeidsparticipatie bij patiënten met symptomatisch Perifeer Arterieel Vaatlijden (sPAV)?
Relevante uitkomstmaten
De werkgroep achtte het fysiek functioneren, de kwaliteit van leven, de mate van pijn, de levensverwachting en de arbeidsparticipatie cruciale uitkomstmaten voor de besluitvorming. De werkgroep achtte ongewenste effecten gerelateerd aan een van de interventies, belangrijke uitkomstmaten.
Per uitkomstmaat:
- Fysiek functioneren
- Zes minuten wandeltest (6MWT): Uit de wetenschappelijke literatuur blijkt dat een verschil van acht meter als belangrijk effect beschouwd kan worden bij patiënten met PAV (klinisch relevant verschil) (McDermott, 2021). De werkgroep beschouwt* deze waarden ook als klinisch relevant voor patiënten met sPAV.
- Loopbandtest: De werkgroep definieerde*, op basis van de wetenschappelijke literatuur, een verschil van 250 meter (functionele loopafstand) en 305 meter (maximale loopafstand) als belangrijk effect bij patiënten met sPAV (klinisch relevant verschil) (van den Houten, 2016a).
- Shuttle Walk Test (SWT): Uit de wetenschappelijke literatuur blijkt dat een verschil van 174 seconden als belangrijk effect beschouwd kan worden bij patiënten met COPD (klinisch relevant verschil) (Zatloukal, 2019). Omdat wetenschappelijke literatuur over de klinische relevantie bij patiënten met sPAV ontbreekt, beschouwt* de werkgroep deze waarden als voldoende gelijkwaardig en daarmee als ook klinisch relevant voor patiënten met sPAV.
- Walking Impairment Questionnaire (WIQ): De werkgroep definieerde*, op basis van de wetenschappelijke literatuur, een verschil van 0.11 punten (op schaal van 0 tot 1, waarbij een hogere score correspondeert met een betere mate van fysiek functioneren) als belangrijk effect bij patiënten met sPAV (klinisch relevant verschil) (Conijn, 2015).
- Kwaliteit van leven
- 36-Item Short Form Health Survey (SF-36): Uit de wetenschappelijke literatuur blijkt dat een verschil van 10 punten (physical functioning, bodily pain, general health en mental health), 12.5 punten (physical role, vitality en social functioning) en 8.3 punten (emotional role) als belangrijk effect beschouwd kan worden bij patiënten met COPD (klinisch relevant verschil) (Wyrwich, 2005). De schaal van de SF-36 loopt van 0 tot 100, waarbij een hogere score correspondeert met een betere kwaliteit van leven. Omdat wetenschappelijke literatuur over de klinische relevantie bij patiënten met sPAV ontbreekt, beschouwt* de werkgroep deze waarden als voldoende gelijkwaardig en daarmee als ook klinisch relevant voor patiënten met sPAV.
- Vascular Quality of Life Questionnaire-6 (VascuQol-6): De werkgroep definieerde*, op basis van de wetenschappelijke literatuur, een verschil van 1.7 punten (op een schaal van 6 tot 24, waarbij een hogere score correspondeert met een betere kwaliteit van leven) als belangrijk effect bij patiënten met sPAV (klinisch relevant verschil) (Nordanstig, 2017).
- EuroQol (EQ-5D): Uit de wetenschappelijke literatuur blijkt dat een verschil van 0.028 punten (op een schaal van -1 tot 1, waarbij een hogere score correspondeert met een betere kwaliteit van leven) als belangrijk effect beschouwd kan worden bij patiënten met COPD (klinisch relevant verschil) (Bae, 2020). Omdat wetenschappelijke literatuur over de klinische relevantie bij patiënten met sPAV ontbreekt, beschouwt* de werkgroep deze waarden als voldoende gelijkwaardig en daarmee als ook klinisch relevant voor patiënten met sPAV.
- Mate van pijn
- Numerical pain rating scale (NPRS): Uit de wetenschappelijke literatuur blijkt dat een verschil van 2 punten (op een schaal van 0 tot 10, waarbij een hogere score correspondeert met een hogere mate van pijn) als belangrijk effect beschouwd kan worden bij patiënten met chronische pijn (klinisch relevant verschil) (Farrar, 2001). Omdat wetenschappelijke literatuur over de klinische relevantie bij patiënten met sPAV ontbreekt, beschouwt* de werkgroep deze waarden als voldoende gelijkwaardig en daarmee als ook klinisch relevant voor patiënten met sPAV.
- Levensverwachting
- Mortaliteit: De werkgroep definieerde* een verschil van 1 op 100 personen als belangrijk effect bij patiënten met sPAV (klinisch relevant verschil).
- Arbeidsparticipatie
- Voor het meten van de arbeidsparticipatie is op voorhand geen meetinstrument met bijbehorende grenzen van klinische relevantie vastgesteld.
- Ongewenste effecten
- Major Adverse Events (ernstige ongewenste voorvallen): De werkgroep definieerde* een verschil van 1 op 50 personen als belangrijk effect bij patiënten met sPAV (klinisch relevant verschil)
- Ziekenhuisopnames: De werkgroep definieerde* een verschil van 1 op 50 personen als belangrijk effect bij patiënten met sPAV (klinisch relevant verschil).
*De werkgroep benadrukt dat het per individu kan verschillen of een effect wel of niet als klinisch relevant wordt beschouwd. Dit kan bijvoorbeeld afhankelijk zijn van de individuele hulpvraag en/of therapiedoelen. Desondanks zijn voor de start van het literatuuronderzoek bovenstaande specifieke grenzen voor klinische relevantie vastgesteld. De genoemde meetinstrumenten met bijbehorende criteria dienen als leidraad voor deze richtlijnmodule, met ruimte voor aanpassingen op basis van individuele patiëntbehoeften. De meetinstrumenten genoemd in de generieke KNGF-richtlijn sPAV (opent in nieuw tabblad) blijven de basis vormen voor diagnostiek en evaluatie.
Zoekactie van de literatuur
Op 17 augustus 2023 is door L. Marcellis (met ondersteuning van informatiespecialist A. Tillema) een systematische zoekactie uitgevoerd in MEDLINE, Embase, Cinahl en Cochrane (zie bijlage C.8.4-1 (opent in nieuw tabblad)voor de zoekverantwoording). De systematische zoekactie leverde 4.602 unieke treffers op. Na screening (door D. Conijn (DC), L. Marcellis (LM), M. Simon (MS) en T. Hoogeboom (TH)) van de titel en het abstract op de inclusiecriteria en exclusiecriteria (zie tabel 1) zijn 4.451 artikelen geëxcludeerd. Gekozen werd om artikelen van voor 2005 te excluderen omdat er een duidelijke toename zichtbaar was van het aantal publicaties in 2005. Artikelen waarvan het op basis van titel en abstract niet duidelijk was of deze voldeden aan de inclusiecriteria werden dubbel gescreend door LM en vervolgens onderling besproken. Van 148 studies is het volledige artikel gescreend door LM, waarbij twijfelgevallen dubbel werden gescreend door DC en vervolgens onderling werden besproken. Uiteindelijk leverde de zoekactie negentien studies (gerapporteerd in 22 artikelen) op voor modules C.8.1, C.8.2, C.8.3 en C.8.4.
Voor module C.8.2 werden twee studies geselecteerd, één systematic review (SR) en één randomized controlled trial (RCT) (Hageman, 2018; Sandberg, 2023). Om overlap van resultaten tussen verschillende systematische literatuuronderzoeken te beperken, is het literatuuronderzoek met de hoogste methodologische kwaliteit volgens de AMSTAR 2-score (gescoord door LM en TH), in overleg met de werkgroep, geselecteerd, waarbij ook rekening werd gehouden met hoe recent het literatuuronderzoek was (Shea, 2017). Om de meest recente RCT’s te kunnen includeren in de literatuurconclusie, is de SR aangevuld met een RCT uit 2023. Zie bijlage C.8.2-2 (opent in nieuw tabblad) voor het stroomdiagram van het inclusieproces. De artikelen die op basis van de volledige tekst zijn geëxcludeerd, en de reden van exclusie zijn weergegeven in bijlage C.8.2-3 (opent in nieuw tabblad).
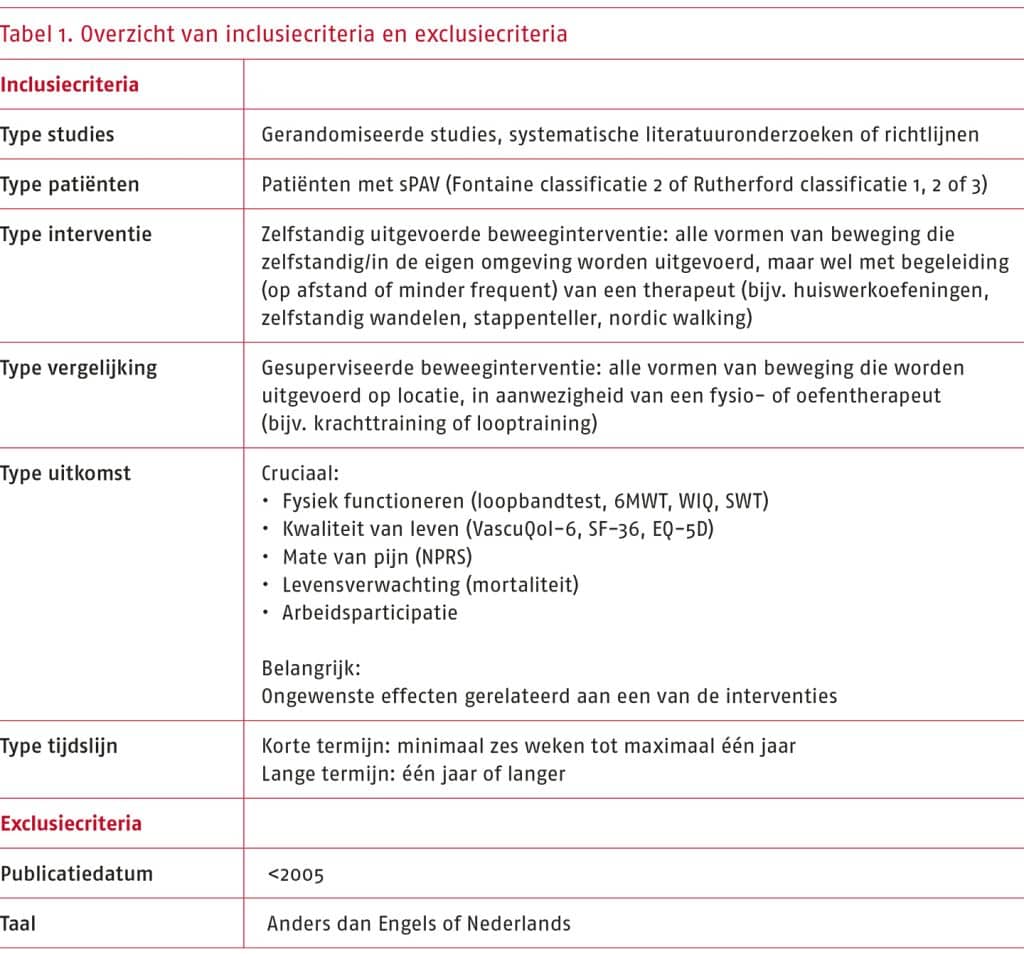
Karakteristieken van geïncludeerde studies
De kenmerken van de twee geïncludeerde studies zijn weergegeven in bijlage C.8.2-4 (opent in nieuw tabblad).
Het systematische literatuuronderzoek van Hageman et al. beschrijft acht geïncludeerde studies die zelfstandig uitgevoerde beweeginterventie vergelijken met een gesuperviseerde beweeginterventie (Hageman, 2018). De studies zijn uitgevoerd in de Verenigde Staten (n=7) en het Verenigd Koninkrijk (n=1). De zoekactie includeerde studies tot 16 december 2016. De acht studies includeerden in totaal 379 patiënten met sPAV. De gemiddelde leeftijd van patiënten in de interventiegroep (zelfstandig uitgevoerde beweeginterventie, n=189) varieerde van 62 tot 70.3 jaar en van patiënten in de controlegroep (gesuperviseerde beweeginterventie, n=190) van 64 tot 67.9 jaar. Het percentage vrouwen in de interventie- en controlegroep varieerde respectievelijk van 20 tot 66% en 27 tot 55%. Patiënten in de interventiegroepen voerden een thuisoefenprogramma uit, bestaande uit twee tot drie oefensessies per week gedurende een periode van twaalf weken (zeven studies) of zes maanden (één studie). Alle studies gaven patiënten specifieke oefeninstructies om zelfstandig te trainen. Oefensessies bestonden uit looptraining tot matige of intense pijn optrad, gevolgd door een korte rustperiode. De duur van de oefensessies varieerde van de 15 minuten (aanvang trainingsperiode) tot 55 minuten (einde trainingsperiode). Een zelfstandig uitgevoerde beweeginterventie betekende dat patiënten de training zelfstanding uitvoerden maar wel begeleiding kregen van een zorgprofessional, zowel persoonlijk (vier studies) als telefonisch (vier studies). De frequentie van dit contact varieerde van wekelijks (vier studies), tweewekelijks (één studie), driewekelijks (één studie) tot maandelijks (twee studies). Twee studies startten met een zelfstandige trainingsperiode van twaalf weken, gevolgd door een niet-gesuperviseerde follow-upperiode van twaalf weken. Patiënten in de controlegroepen voerden gesuperviseerde beweeginterventies uit, bestaande uit twee tot drie oefensessies per week gedurende een periode van twaalf weken. De gesuperviseerde interventies bestonden uit looptraining op een loopband met variërende intensiteit tot matige of intense pijn optrad, gevolgd door een korte rustperiode. In één studie werd looptraining (primaire training) aangevuld met cardiovasculaire training (arm- en beenfietsen). De duur van de gesuperviseerde oefensessies varieerde van 15 minuten (aanvang trainingsperiode) tot 60 minuten (einde trainingsperiode). Drie studies startten met een gesuperviseerde trainingsperiode van twaalf weken, gevolgd door een niet-gesuperviseerde follow-upperiode van twaalf weken.
De RCT van Sandberg et al. beschrijft 110 patiënten met sPAV (Sandberg, 2023). De studie werd uitgevoerd in Zweden. Patiënten in beide groepen trainden drie keer per week, 50 minuten lang, gedurende een periode van twaalf maanden. Patiënten in de interventiegroep (n=56, leeftijd 71.8 ± 6.5 jaar, 37.5% vrouw) voerden een thuisoefenprogramma uit, bestaande uit zowel loop- als krachtoefeningen. Patiënten trainden tot een intensiteit (claudicatioklachten) van graad ≥17 op een 6-20-graads Borg-schaal. Patiënten hadden gedurende de eerste zes maanden tweewekelijks telefonisch contact met een fysiotherapeut. Gedurende maand zeven tot en met maand twaalf was er geen contact. Patiënten in de controlegroep (n=54, leeftijd 72.2 ± 7.5 jaar, 42.6% vrouw) voerden hetzelfde oefenprogramma uit als patiënten in de interventiegroep, maar dan met supervisie van een fysiotherapeut gedurende de eerste zes maanden. Beide groepen kregen aanvullend het advies om zelfstandig nordic walking (klachten inducerend) uit te voeren, minimaal drie keer per week voor minimaal 30 minuten.
Individuele studiekwaliteit (RoB)
Het risico op vertekening (risk of bias, RoB) van het systematische literatuuronderzoek is door TH en LM gescoord met behulp van de AMSTAR 2 (Shea, 2017). Het risico op vertekening (RoB) van de RCT is dubbel gescoord door TH en LM met behulp van de Cochrane Risk-of-Bias-2 tool (Higgins, 2019). Inconsistentie in het oordeel op de verschillende items is onderling besproken door TH en LM, waarna consensus is bereikt.
Een overzicht van de beoordeling van de studiekwaliteit voor zowel de RCT als het systematische literatuuronderzoek is weergegeven in bijlage C.8.2-5 (opent in nieuw tabblad)Risk-of-bias-tabel. Ook het risico op vertekening van de geïncludeerde studies in het systematische literatuuronderzoek van Hageman et al. is bijgevoegd in bijlage C.8.2-5 (opent in nieuw tabblad) Risk-of-biastabel. Hageman et al. scoorden het risico op vertekening van de geïncludeerde studies met behulp van de Cochrane Risk-of-Bias-1 tool (Higgins, 2011).
Effectiviteit en bewijskracht
Zie de Toelichting voor de conclusies op basis van de literatuur. Hieronder volgt een beschrijving van de effectiviteit en de bewijskracht voor de vergelijking(en).
Zelfstandig uitgevoerde beweeginterventie versus gesuperviseerde beweeginterventie
Het effect van een zelfstandig uitgevoerde beweeginterventie vergeleken met een gesuperviseerde beweeginterventie op fysiek functioneren en kwaliteit van leven is beschreven in acht studies, die werden geïncludeerd in het geselecteerde systematische literatuuronderzoek van Hageman et al. (Allen, 2010; Gardner, 2014; Gardner, 2011; Patterson, 1997; Regensteiner, 1997; Sandercock, 2007; Savage, 2001; Treat-Jacobson, 2009). Een overzicht van de resultaten uit Hageman et al. wordt weergegeven in tabel 2. Zie bijlage C.8.2-6 (opent in nieuw tabblad) voor de forest plots van de uitkomsten op fysiek functioneren (loopbandtest functionele loopafstand/-tijd, loopbandtest maximale loopafstand/-tijd en WIQ totaalscore) en kwaliteit van leven (SF-36 physical component summary en SF-36 mental component summary). Hieronder worden de effectiviteit en bewijskracht per uitkomstmaat beschreven.
Het geïncludeerde RCT rapporteert resultaten op fysiek functioneren (6MWT en WIQ). De WIQ-data konden niet worden geïncludeerd in de meta-analyse vanwege niet normaal verdeelde data. Door deze niet-normale verdeling waren de resultaten niet goed vergelijkbaar met de andere studies. Tevens hebben Hageman et al. enkel studies geïncludeerd die gebruikmaakten van de loopbandtest, wat maakt dat deze RCT de enige studie is die gebruikmaakt van de 6MWT. Om die reden is ervoor gekozen om ook de resultaten op de 6MWT niet te includeren in de meta-analyse, en daarmee alle resultaten van het geïncludeerde RCT narratief te beschrijven (Sandberg, 2023).
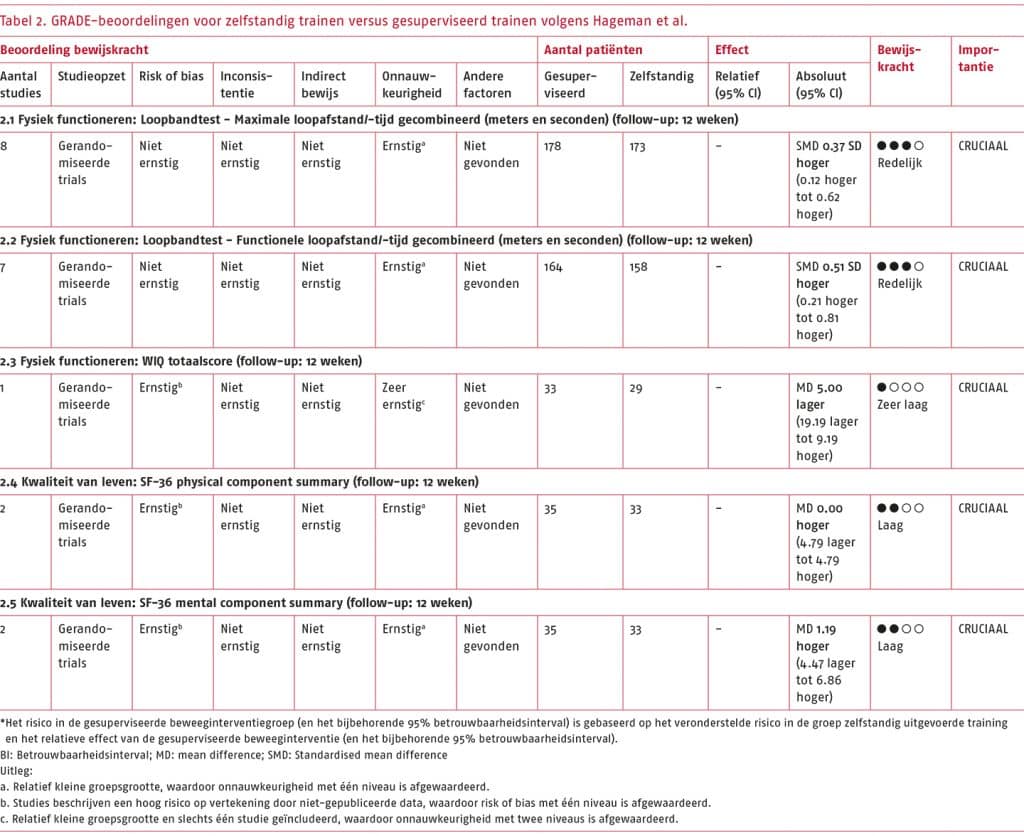
Vergelijking 1. Fysiek functioneren – Loopbandtest functionele loopafstand (follow-up na 12 weken)
In zeven studies is de effectiviteit van een gesuperviseerde beweeginterventie vergeleken met die van een zelfstandig uitgevoerde beweeginterventie op fysiek functioneren, gemeten als functionele loopafstand met de loopbandtest (Allen, 2010; Gardner, 2014; Gardner, 2011; Patterson, 1997; Regensteiner, 1997; Savage, 2001; Treat-Jacobson, 2009). Het gestandaardiseerde gemiddelde verschil (SMD) tussen de groepen was 0.51 SD (95% BI 0.21 tot 0.81; p=0.0009; n=164 groep gesuperviseerde training en n=158 groep zelfstandig trainen) in het voordeel van de groep gesuperviseerde training. Dit effect wordt door de werkgroep als een significant en klinisch relevant effect beschouwd (Sawilowsky, 2009).
De bewijskracht is door Hageman et al. met een niveau verlaagd tot redelijk, gezien het risico op vertekening door de gevonden onnauwkeurigheid (-1 niveau).
Vergelijking 2. Fysiek functioneren – Loopbandtest maximale loopafstand (follow-up na 12 weken)
In acht studies is de effectiviteit van een gesuperviseerde beweeginterventie vergeleken met die van een zelfstandig uitgevoerde beweeginterventie op fysiek functioneren, gemeten als maximale loopafstand met de loopbandtest (Allen, 2010; Gardner, 2014; Gardner, 2011; Patterson, 1997; Regensteiner, 1997; Sandercock, 2007; Savage, 2001; Treat-Jacobson, 2009). Het gestandaardiseerde gemiddelde verschil (SMD) tussen de groepen was 0.37 SD (95% BI 0.12 tot 0.62; p=0.004; n=178 gesuperviseerde training en n=173 groep zelfstandig trainen) in het voordeel van de groep gesuperviseerde training. Dit effect wordt door de werkgroep als een significant en niet-klinisch relevant effect beschouwd (Sawilowsky, 2009).
De bewijskracht is door Hageman et al. met een niveau verlaagd tot redelijk, gezien het risico op vertekening door de gevonden onnauwkeurigheid (-1 niveau).
Vergelijking 3. Fysiek functioneren – WIQ totaalscore (follow-up na 12 weken)
In één studie is de effectiviteit van een gesuperviseerde beweeginterventie vergeleken met die van een zelfstandig uitgevoerde beweeginterventie op fysiek functioneren, gemeten met de WIQ totaalscore (Gardner, 2011). Het gemiddelde verschil (MD) tussen de groepen was -5.00 punten (95%-BI -19.19 tot 9.19; p=niet gerapporteerd, n=33 groep gesuperviseerde training en n=29 groep zelfstandig trainen) in het nadeel van de groep gesuperviseerde training. Dit effect wordt door de werkgroep als een niet-significant en niet-klinisch relevant effect beschouwd (Conijn, 2015).
De bewijskracht is door Hageman et al. met drie niveaus verlaagd tot zeer laag, gezien het risico op vertekening door de gevonden onnauwkeurigheid (-2 niveaus) en door de individuele studiekwaliteit (-1 niveau). De werkgroep heeft besloten om de bewijskracht verder te verlagen, gezien de gevonden onnauwkeurigheid doordat het betrouwbaarheidsinterval een niet-klinisch relevant effect bevat (van -2 niveaus naar -3 niveaus).
Vergelijking 4. Kwaliteit van leven – SF-36 physical component summary (follow-up na 12 weken)
In twee studies is de effectiviteit van een gesuperviseerde beweeginterventie vergeleken met die van een zelfstandig uitgevoerde beweeginterventie op kwaliteit van leven, gemeten met de SF-36 physical component summary (Patterson, 1997; Savage, 2001). Het gemiddelde verschil (MD) tussen de groepen was 0.00 punten (95%-BI -4.79 tot 4.79; p=1.0, n=35 groep gesuperviseerde training en n=33 groep zelfstandig trainen). Dit effect wordt door de werkgroep als een niet-significant en niet-klinisch relevant effect beschouwd (Wyrwich, 2005).
De bewijskracht is door Hageman et al. met twee niveaus verlaagd tot laag, gezien het risico op vertekening door de gevonden onnauwkeurigheid (-1 niveau) en door de individuele studiekwaliteit (-1 niveau). De werkgroep heeft besloten om de bewijskracht verder te verlagen naar zeer laag, gezien de gevonden onnauwkeurigheid doordat het betrouwbaarheidsinterval een niet-klinisch relevant effect bevat (van -1 niveau naar -2 niveaus).
Vergelijking 5. Kwaliteit van leven – SF-36 mental component summary (follow-up na 12 weken)
In twee studies is de effectiviteit van een gesuperviseerde beweeginterventie vergeleken met die van een zelfstandig uitgevoerde beweeginterventie op kwaliteit van leven, gemeten met de SF-36 mental component summary (Patterson, 1997; Savage, 2001). Het gemiddelde verschil (MD) tussen de groepen was 1.19 punten (95%-BI -4.47 tot 6.86; p=0.68, n=35 groep gesuperviseerde training en n=33 groep zelfstandig trainen) in het voordeel van de groep gesuperviseerde training. Dit effect wordt door de werkgroep als een niet-significant en niet-klinisch relevant effect beschouwd (Wyrwich, 2005).
De bewijskracht is door Hageman et al. met twee niveaus verlaagd tot laag, gezien het risico op vertekening door de gevonden onnauwkeurigheid (-1 niveau) en door de individuele studiekwaliteit (-1 niveau). De werkgroep heeft besloten om de bewijskracht verder te verlagen naar zeer laag, gezien de gevonden onnauwkeurigheid doordat het betrouwbaarheidsinterval een niet-klinisch relevant effect bevat (van -1 niveau naar -2 niveaus) en door de gevonden inconsistentie als gevolg van klinische heterogeniteit (-1 niveau).
Levensverwachting – Mortaliteit
Het geïncludeerde systematische literatuuronderzoek beschrijft dat geen sterfgevallen gerelateerd aan een van de twee beweeginterventies, werden gevonden in de acht geïncludeerde studies. Het literatuuronderzoek beschrijft wel dat één studie twee sterfgevallen rapporteerde in de groep gesuperviseerde training, maar dat niet werd benoemd wat de redenen van overlijden waren.
Overige uitkomstmaten
Er zijn geen studies gevonden die resultaten hebben beschreven op de overige cruciale uitkomstmaten: mate van pijn en arbeidsparticipatie.
Ongewenste effecten
De studie van Sandberg et al. rapporteerde dat ongewenste effecten gerelateerd aan een van de interventies, niet zijn voorgevallen (Sandberg, 2023).
Individuele RCT
Sandberg et al.
De studie van Sandberg et al. rapporteerde data op fysiek functioneren na drie, zes en twaalf maanden (gemeten als pijnvrije en maximale loopafstand met de 6MWT en de WIQ). De 6MWT-data worden gepresenteerd als gemiddelde (95%-BI). De WIQ-data worden gepresenteerd als mediaan (IQR) vanwege een niet-normale verdeling van de data (zie tabel 3).
Verschillen tussen de groepen worden voor alle drie de uitkomstmaten gerapporteerd als niet-significant op alle tijdsmomenten. De bevindingen van deze RCT over functionele en maximale loopafstand zijn daarmee tegengesteld aan de resultaten van het systematische literatuuronderzoek, waarin significante verschillen werden gevonden in het voordeel van gesuperviseerde training (gemeten met de loopbandtest). De bevindingen over de WIQ bevestigen de resultaten van het systematische literatuuronderzoek, dat ook geen significante verschillen vond op de WIQ.
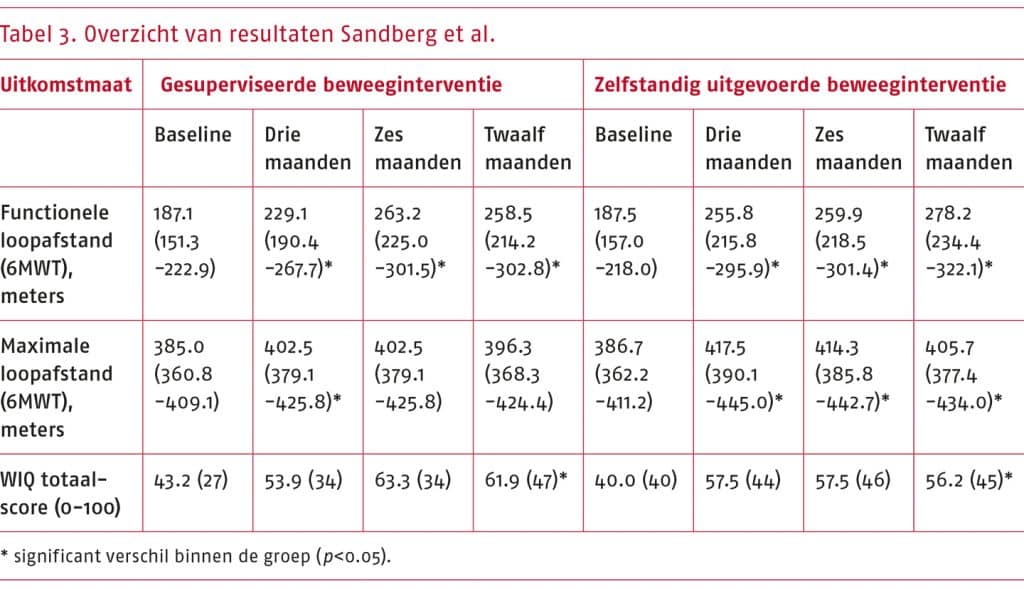
Van bewijs naar aanbeveling
Criteria
Het onderdeel van bewijs naar aanbeveling bevat negen criteria, die hieronder worden opgesomd.
Gewenste effecten
Een overzicht van de resultaten uit de systematische literatuuranalyse wordt weergegeven in tabel 4. De resultaten uit de individuele RCT zijn deels tegengesteld aan de bevindingen uit de literatuuranalyse, aangezien de RCT op loopafstand (gemeten met 6MWT) geen significante verschillen vond tussen gesuperviseerd trainen en zelfstandig trainen. De bevindingen op de WIQ uit de individuele RCT bevestigen de resultaten uit de literatuuranalyse (beide niet-significant).
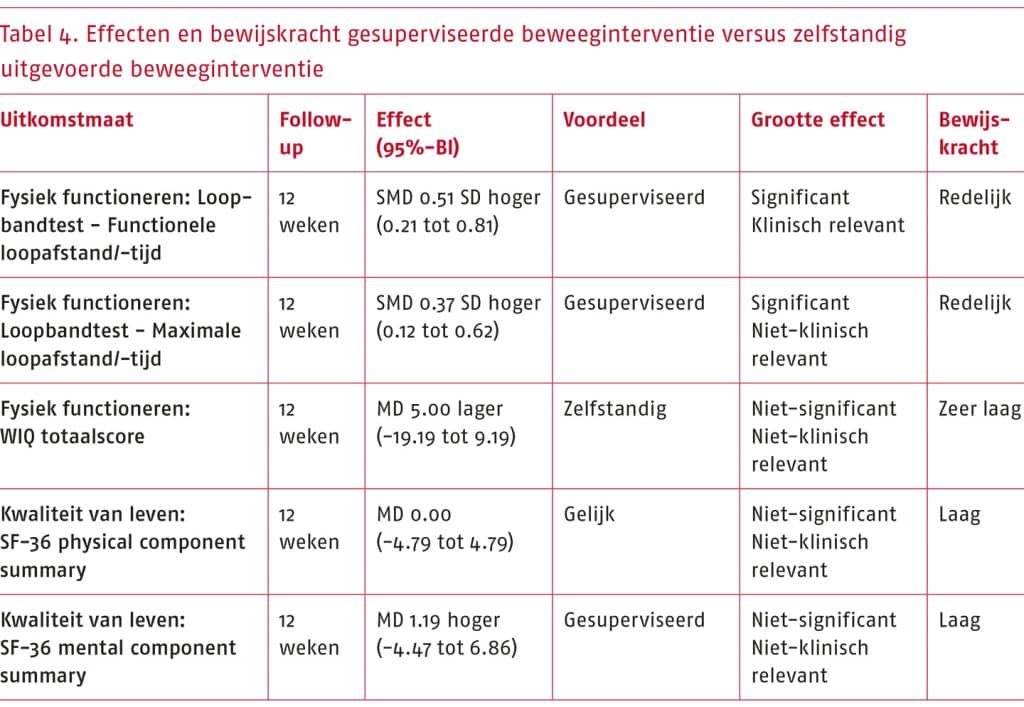
De werkgroep beoordeelt de gewenste effecten op het fysiek functioneren (gemeten als functionele of maximale loopafstand) van gesuperviseerde training ten opzichte van zelfstandig uitgevoerde training voor patiënten met sPAV als significant en klinisch relevant voor functionele loopafstand en significant en niet-klinisch relevant voor maximale loopafstand. De bevindingen laten zien dat zowel gesuperviseerde als zelfstandige training zorgt voor verbetering van het fysiek functioneren gemeten als de functionele en maximale loopafstand. Echter, gesuperviseerde training zorgt voor een significante en klinisch relevante grotere verbetering in de functionele loopafstand vergeleken met zelfstandige training.
De werkgroep beoordeelt de gewenste effecten op het fysiek functioneren (gemeten met de WIQ) van gesuperviseerde training ten opzichte van zelfstandige training als niet-significant en niet-klinisch relevant. De bevindingen laten zien dat zowel gesuperviseerde als zelfstandige training zorgt voor verbetering van het fysiek functioneren gemeten met de WIQ.
De werkgroep beoordeelt de gewenste effecten op de kwaliteit van leven (gemeten met de SF-36) van gesuperviseerde training ten opzichte van zelfstandige training als niet-significant en niet-klinisch relevant. De bevindingen laten zien dat zowel gesuperviseerde als zelfstandige training zorgt voor verbetering van de kwaliteit van leven bij patiënten met sPAV.
De werkgroep geeft aan dat het aannemelijk is dat zowel het inzetten van gesuperviseerde training als zelfstandig uitgevoerde training waardevolle gewenste effecten heeft om het fysiek functioneren en de kwaliteit van leven bij patiënten met sPAV te verbeteren. De werkgroep beoordeelt de gewenste effecten van gesuperviseerde training op fysiek functioneren als groter dan de gewenste effecten op fysiek functioneren van zelfstandige training.
Ongewenste effecten
De werkgroep beoordeelt de kans op ongewenste effecten van zelfstandig uitgevoerde training ten opzichte van gesuperviseerde training voor patiënten met sPAV als klein. Alhoewel de geselecteerde studies hier weinig informatie over rapporteren, is de werkgroep van mening dat zowel het uitvoeren van gesuperviseerde training als het uitvoeren van zelfstandige training voor patiënten met sPAV veilig is. Het geïncludeerde systematische literatuuronderzoek rapporteert geen sterfgevallen gerelateerd aan een van de interventies, en de geïncludeerde RCT rapporteert geen voorgevallen ongewenste effecten.
Door Gommans et al. is in een systematisch literatuuronderzoek onderzoek gedaan naar de veiligheid van gesuperviseerde beweeginterventies bij patiënten met sPAV, waarbij werd gekeken naar de complicatieratio (aantal ongewenste effecten per aantal trainingsuren) (Gommans, 2015). Deze systematische review includeerde 74 artikelen (waarvan 49 artikelen met als interventie gesuperviseerde looptraining) en rapporteerde een complicatieratio van één ongewenst voorval per 10.340 trainingsuren. Gommans et al. concluderen dat gesuperviseerde beweeginterventies veilig zijn met een buitengewoon lage complicatieratio. De werkgroep beoordeelt dat deze studie aantoont dat gesuperviseerde looptraining veilig en daarmee verantwoord is.
De werkgroep beoordeelt zelfstandig uitgevoerde training als verantwoord, op voorwaarde dat zelfstandig trainen inhoudt dat de patiënt de beweeginterventie hoofdzakelijk thuis/in de eigen omgeving uitvoert, maar dat begeleiding en monitoring van de therapeut nog steeds aanwezig zijn (dit kan door zorg op afstand of door het inplannen van fysieke zittingen om het behandelplan te evalueren en de vooruitgang te evalueren).
Kwaliteit van bewijs
De werkgroep beoordeelt de bewijskracht van de gewenste effecten als redelijk op de uitkomst fysiek functioneren gemeten als functionele en maximale loopafstand met de loopbandtest, en als zeer laag op de uitkomst fysiek functioneren gemeten met de WIQ. De bewijskracht van de gewenste effecten op de uitkomst kwaliteit van leven (gemeten met de SF-36) wordt beoordeeld als laag. Het is hierbij van belang om rekening te houden met het feit dat de bewijskracht met name is afgewaardeerd als gevolg van het risico op vertekening door de individuele studiekwaliteit en door de kleine onderzoekspopulaties.
Waarden en voorkeuren van patiënten
De werkgroep is tot het oordeel gekomen dat patiënten grote waarde hechten aan gesuperviseerde looptraining, maar dat daar wel variatie in zit tussen patiënten. Er bestaat een groep patiënten die de voorkeur heeft om met name zelfstandig met training aan de slag te gaan. Er zijn echter ook patiënten die graag een stok achter de deur (in de vorm van intensieve supervisie) willen hebben of nodig hebben om de training vol te kunnen houden. De werkgroep beoordeelt dat vooral over de mate van supervisie de voorkeuren uiteenlopen.
Dit wordt ondersteund door een achterbanraadpleging (n=60 patiënten met sPAV) van Stichting Harteraad. Hoewel uit de resultaten van deze raadpleging blijkt dat 65% van de patiënten een voorkeur heeft voor gesuperviseerde training, hebben de overige patiënten of een voorkeur voor zelfstandig trainen (30%), of ze geven aan geen specifieke voorkeur te hebben (5%). Redenen waarom patiënten een voorkeur hebben voor gesuperviseerde training zijn motivatie en stimulatie door de begeleiding, meer toezicht op de uitvoering van de training en de mogelijk gebruik te maken van een loopband. Redenen waarom patiënten een voorkeur hebben voor zelfstandig uitgevoerde training zijn het behoud van de eigen regie (zelf de tijd en plaats kunnen bepalen), meer afwisseling in training en makkelijker van de training een gewoonte kunnen maken.
Balans gewenste en ongewenste effecten
De werkgroep is tot het oordeel gekomen dat de gewenste effecten van het aanbieden van zelfstandig uitgevoerde training als alternatief voor gesuperviseerde training zeker de ongewenste effecten overtreffen, maar dat de gewenste effecten van gesuperviseerd trainen groter zijn dan de gewenste effecten van zelfstandig trainen.
De motivatie hiervoor is:
- Uit de effecten en de bewijskracht blijkt dat de gewenste effecten van gesuperviseerde beweeginterventies groter zijn op het gebied van de functionele loopafstand dan wanneer de patiënt zelfstandig traint. Echter, op de overige uitkomstmaten is geen van de interventies superieur aan de ander. Zowel gesuperviseerde beweeginterventies als zelfstandig uitgevoerde beweeginterventies hebben positieve effecten op het fysiek functioneren en de kwaliteit van leven van patiënten met sPAV. Zelfstandig uitgevoerde beweeginterventies zijn daarmee een mogelijk alternatief voor gesuperviseerde beweeginterventies, met relevante gewenste effecten en zonder relevante ongewenste effecten.
- Er zijn geen aanwijzingen dat zelfstandig uitgevoerde beweeginterventies onveiliger zijn dan gesuperviseerde beweeginterventies bij patiënten met sPAV.
- Patiënten met sPAV hebben verschillende voorkeuren voor de mate van supervisie en hechten veel waarde aan het mogen uitspreken van een voorkeur voor de mate van supervisie. Dit maakt dat er vanuit patiëntperspectief geen generieke voorkeur is voor gesuperviseerde of zelfstandig uitgevoerde beweeginterventies.
Economische overwegingen en kosteneffectiviteit
De werkgroep beoordeelt de benodigde middelen voor zelfstandig uitgevoerde beweeginterventies ten opzichte van gesuperviseerde beweeginterventies als vergelijkbaar. Zowel gesuperviseerde als zelfstandig uitgevoerde beweeginterventies zijn wisselend van aard, en variëren van trainen in een oefenruimte van de therapeut, waar oefenmateriaal aanwezig moet zijn, tot zelfstandig trainen, waar ook materialen of lidmaatschappen voor nodig kunnen zijn.
Gesuperviseerde beweeginterventies brengen hogere directe (maatschappelijke) kosten met zich mee dan zelfstandig uitgevoerde beweeginterventies, vanwege de kosten voor een therapeutisch consult. Een studie van Ulfsdotter et al. rapporteert dat zelfstandig trainen mogelijk meer kosteneffectief is dan gesuperviseerde training (Ulfsdottir, 2023), vermoedelijk te verklaren doordat minder consulten worden ingezet. Echter, gesuperviseerde beweegtraining is een aangetoond kosteneffectieve behandeling (Fokkenrood, 2014; van Asselt, 2011; van den Houten, 2016b) en uiteindelijk is kosteneffectiviteit met name afhankelijk van de therapietrouw van de patiënt. De werkgroep is daarom van mening dat zelfstandige training mogelijk vergelijkbaar is qua kosteneffectiviteit, maar dat de keuze voor zelfstandig uitgevoerde training wel moet aansluiten op de mogelijkheden van de patiënt, om daarmee toename van zorgkosten op langere termijn door bijvoorbeeld verminderde zelfredzaamheid te voorkomen.
De werkgroep verwacht dat economische overwegingen vanuit de patiënt weinig invloed hebben op de keuze voor de mate van supervisie, aangezien in Nederland gesuperviseerde beweegtraining wordt vergoed uit de basisverzekering. Door de mate van supervisie aan te laten sluiten op de voorkeuren van de patiënt, verwacht de werkgroep wel dat effecten van therapie mogelijk vergroot worden (door o.a. hogere motivatie en therapietrouw), wat een positief effect kan hebben op het voorkomen van invasieve behandelingen, het verlagen van zorggebruik en daarmee het beperken van zorgkosten.
Gelijkheid
De werkgroep verwacht dat het aanbieden van zelfstandig trainen naast gesuperviseerd trainen zal leiden tot een mogelijke toename van de gezondheidsgelijkheid.
Uit de knelpuntenanalyse onder therapeuten en uit de literatuur komt naar voren dat men bezorgd is dat het toepassen van samen beslissen (zoals het kiezen voor een bepaalde mate van supervisie) een risico vormt voor de gezondheidsgelijkheid, door de gedachte dat samen beslissen meer waardevol is voor hoger opgeleide personen, die beter in staat zijn om op te komen voor hun behoeften en een hoger niveau van gezondheidsvaardigheden hebben (Coulter, 2011; Legare, 2008). Een systematic review van Durand et al. laat echter zien dat samen beslissen juist leidt tot een toename van gezondheidsgelijkheid, mits de informatievoorziening wordt aangepast aan de behoeften van de individuele patiënt (Durand, 2014).
De werkgroep beoordeelt dat het bespreekbaar maken van de mate van supervisie zorgt voor een betere aansluiting van de zorg op de wensen en mogelijkheden van de individuele patiënt met sPAV en daarmee voor een betere aansluiting van de zorg op een grotere groep patiënten (inclusieve zorg). De werkgroep benadrukt ook dat gesuperviseerde beweegtraining in geen geval zal leiden tot een afname van de gezondheidsgelijkheid. Gesuperviseerde beweegtraining is in Nederland namelijk toegankelijk voor alle patiënten met sPAV (opgenomen in basisverzekering) en tevens is de spreiding van het aantal fysio-/oefentherapeuten voor patiënten met sPAV zodanig dat iedereen de mogelijkheid heeft om in de woonomgeving therapie te volgen.
Aanvaardbaarheid
De werkgroep verwacht dat het aanbieden van zelfstandig trainen als aanvulling op gesuperviseerd trainen door alle belangrijke stakeholders zal worden geaccepteerd, mits de zelfstandig uitgevoerde beweeginterventies aangevuld worden met adequate begeleiding en monitoring (eventueel zorg op afstand) die aansluiten bij de behoeften en mogelijkheden van de individuele patiënt.
Haalbaarheid
De implementatie van het aanbieden van zelfstandig trainen naast gesuperviseerd trainen wordt door de werkgroep als realistisch beoordeeld. De norm is dat een beweeginterventie wordt aangeboden waarin altijd een bepaalde mate van supervisie door een fysio-/oefentherapeut aanwezig is. Dit kan bijvoorbeeld een vorm van blended care inhouden, waarbij een patiënt na een uitgebreide face-to-face intake hoofdzakelijk zelfstandig traint en contact houdt met de therapeut om de effecten te evalueren en de training waar nodig bij te stellen.
Eventuele additionele overwegingen
De werkgroep is van mening dat de volgende overwegingen ook van belang zijn bij het aanbieden van zelfstandig uitgevoerde beweeginterventies naast gesuperviseerde beweeginterventies:
- Het is van belang dat de therapeut altijd samen met de patiënt de voortgang van de behandeling evalueert (door inzet van gestandaardiseerde meetinstrumenten) (opent in nieuw tabblad).
- Bij het aanbieden van zowel zelfstandig trainen als gesuperviseerd trainen blijft een belangrijke rol weggelegd voor de therapeut om ziekte-inzicht, actieve leefstijl en zelfmanagement van de patiënt te bevorderen.
- Het is van belang dat de behandeling altijd start met een uitgebreide fysieke intake waarin veel ruimte is voor voorlichting. Vanuit daar kan de therapeut samen met de patiënt beslissen over de in te zetten mate van supervisie.
- Het is van belang dat patiënten positieve ervaringen opdoen met beweging. Training of beweging moet niet met tegenzin worden uitgevoerd; het streven moet zijn dat de ervaringen van patiënten met het bewegen de verwachtingen overtreffen, om zo optimale resultaten te behalen. Daarbij kan het van meerwaarde zijn om zelfstandig trainen aan te bieden naast gesuperviseerd trainen.
- De mate van supervisie kan altijd heroverwogen worden gedurende het behandeltraject, dit kan bijvoorbeeld afhankelijk zijn van de voortgang van de behandeling of van de voorkeuren en wensen van de patiënt.
Kennislacunes
- De kwaliteit van bewijs is voor alle uitkomstmaten, met uitzondering van functionele en maximale loopafstand, op zeer lage of lage kwaliteit van bewijs uitgekomen. Om gericht een uitspraak te kunnen doen over de effectiviteit, dienen er meer studies uitgevoerd te worden bij patiënten met sPAV, waarbij gesuperviseerd trainen wordt vergeleken met een zelfstandig uitgevoerde beweeginterventie, op uitkomstmaten zoals kwaliteit van leven, mate van pijn en arbeidsparticipatie.
Aboyans, V., Ricco, J. B., Bartelink, M. E. L., Bjorck, M., Brodmann, M., Cohnert, T., Collet, J. P., Czerny, M., De Carlo, M., Debus, S., Espinola-Klein, C., Kahan, T., Kownator, S., Mazzolai, L., Naylor, A. R., Roffi, M., Rother, J., Sprynger, M., Tendera, M., et al. (2018). 2017 ESC Guidelines on the Diagnosis and Treatment of Peripheral Arterial Diseases, in collaboration with the European Society for Vascular Surgery (ESVS): Document covering atherosclerotic disease of extracranial carotid and vertebral, mesenteric, renal, upper and lower extremity arteriesEndorsed by: the European Stroke Organization (ESO)The Task Force for the Diagnosis and Treatment of Peripheral Arterial Diseases of the European Society of Cardiology (ESC) and of the European Society for Vascular Surgery (ESVS). Eur Heart J, 39(9), 763-816. https://doi.org/10.1093/eurheartj/ehx095
Allen, J. D., Stabler, T., Kenjale, A., Ham, K. L., Robbins, J. L., Duscha, B. D., Dobrosielski, D. A.& Annex, B. H. (2010). Plasma nitrite flux predicts exercise performance in peripheral arterial disease after 3months of exercise training. Free Radic Biol Med, 49(6), 1138-1144. https://doi.org/10.1016/j.freeradbiomed.2010.06.033
Bae, E., Choi, S. E., Lee, H., Shin, G.& Kang, D. (2020). Validity of EQ-5D utility index and minimal clinically important difference estimation among patients with chronic obstructive pulmonary disease. BMC Pulm Med, 20(1), 73. https://doi.org/10.1186/s12890-020-1116-z
Bartelink, M. E. L., Elsman, B. H. P., Oostindjer, A., Stoffers, H. E. J. H., Wiersma, T. J.& Geraets, J. J. X. R. (2014). NHG-Standaard Perifeer arterieel vaatlijden. Huisarts Wet, 57(2), 81-81.
Conijn, A. P., Jonkers, W., Rouwet, E. V., Vahl, A. C., Reekers, J. A.& Koelemay, M. J. (2015). Introducing the Concept of the Minimally Important Difference to Determine a Clinically Relevant Change on Patient-Reported Outcome Measures in Patients with Intermittent Claudication. Cardiovasc Intervent Radiol, 38(5), 1112-1118. https://doi.org/10.1007/s00270-015-1060-0
Coulter, A., Collins, A.& King’s Fund, C. (2011). Making shared decision-making a reality : no decision about me, without me. King’s Fund.
Durand, M. A., Carpenter, L., Dolan, H., Bravo, P., Mann, M., Bunn, F.& Elwyn, G. (2014). Do interventions designed to support shared decision-making reduce health inequalities? A systematic review and meta-analysis. PLoS One, 9(4), e94670. https://doi.org/10.1371/journal.pone.0094670
Elwyn, G., Durand, M. A., Song, J., Aarts, J., Barr, P. J., Berger, Z., Cochran, N., Frosch, D., Galasinski, D., Gulbrandsen, P., Han, P. K. J., Harter, M., Kinnersley, P., Lloyd, A., Mishra, M., Perestelo-Perez, L., Scholl, I., Tomori, K., Trevena, L., et al. (2017). A three-talk model for shared decision making: multistage consultation process. BMJ, 359, j4891. https://doi.org/10.1136/bmj.j4891
Farrar, J. T., Young, J. P., Jr., LaMoreaux, L., Werth, J. L.& Poole, M. R. (2001). Clinical importance of changes in chronic pain intensity measured on an 11-point numerical pain rating scale. Pain, 94(2), 149-158. https://doi.org/10.1016/S0304-3959(01)00349-9
Fokkenrood, H. J., Scheltinga, M. R., Koelemay, M. J., Breek, J. C., Hasaart, F., Vahl, A. C.& Teijink, J. A. (2014). Significant savings with a stepped care model for treatment of patients with intermittent claudication. Eur J Vasc Endovasc Surg, 48(4), 423-429. https://doi.org/10.1016/j.ejvs.2014.04.020
Gardner, A. W., Parker, D. E., Montgomery, P. S.& Blevins, S. M. (2014). Step-monitored home exercise improves ambulation, vascular function, and inflammation in symptomatic patients with peripheral artery disease: a randomized controlled trial. J Am Heart Assoc, 3(5), e001107. https://doi.org/10.1161/JAHA.114.001107
Gardner, A. W., Parker, D. E., Montgomery, P. S., Scott, K. J.& Blevins, S. M. (2011). Efficacy of quantified home-based exercise and supervised exercise in patients with intermittent claudication: a randomized controlled trial. Circulation, 123(5), 491-498. https://doi.org/10.1161/CIRCULATIONAHA.110.963066
Gerhard-Herman, M. D., Gornik, H. L., Barrett, C., Barshes, N. R., Corriere, M. A., Drachman, D. E., Fleisher, L. A., Fowkes, F. G., Hamburg, N. M., Kinlay, S., Lookstein, R., Misra, S., Mureebe, L., Olin, J. W., Patel, R. A., Regensteiner, J. G., Schanzer, A., Shishehbor, M. H., Stewart, K. J., et al. (2017). 2016 AHA/ACC Guideline on the Management of Patients With Lower Extremity Peripheral Artery Disease: Executive Summary: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. Circulation, 135(12), e686-e725. https://doi.org/10.1161/CIR.0000000000000470
Gommans, L. N., Fokkenrood, H. J., van Dalen, H. C., Scheltinga, M. R., Teijink, J. A.& Peters, R. J. (2015). Safety of supervised exercise therapy in patients with intermittent claudication. J Vasc Surg, 61(2), 512-518 e512. https://doi.org/10.1016/j.jvs.2014.08.070
Hageman, D., Fokkenrood, H. J., Gommans, L. N., van den Houten, M. M.& Teijink, J. A. (2018). Supervised exercise therapy versus home-based exercise therapy versus walking advice for intermittent claudication. Cochrane Database Syst Rev, 4, CD005263. https://doi.org/10.1002/14651858.CD005263.pub4
Higgins, J. P., Altman, D. G., Gøtzsche, P. C., Jüni, P., Moher, D., Oxman, A. D., Savović, J., Schulz, K. F., Weeks, L.& Sterne, J. A. (2011). The Cochrane Collaboration’s tool for assessing risk of bias in randomised trials. BMJ, 343.
Higgins, J. P., Savović, J., Page, M. J., Elbers, R. G.& Sterne, J. A. (2019). Assessing risk of bias in a randomized trial. Cochrane handbook for systematic reviews of interventions, 205-228.
Langendam, M.& Kuijpers, T. (2022). Toepassen GRADE voor interventies: tool. The Dutch GRADE Network.
Legare, F., Ratte, S., Gravel, K.& Graham, I. D. (2008). Barriers and facilitators to implementing shared decision-making in clinical practice: update of a systematic review of health professionals’ perceptions. Patient Educ Couns, 73(3), 526-535. https://doi.org/10.1016/j.pec.2008.07.018
McDermott, M. M., Tian, L., Criqui, M. H., Ferrucci, L., Conte, M. S., Zhao, L., Li, L., Sufit, R., Polonsky, T. S., Kibbe, M. R., Greenland, P., Leeuwenburgh, C.& Guralnik, J. M. (2021). Meaningful change in 6-minute walk in people with peripheral artery disease. J Vasc Surg, 73(1), 267-276 e261. https://doi.org/10.1016/j.jvs.2020.03.052
Merry, A. H. H., Teijink, J. A. W., Jongert, M. W. A., Poelgeest, A., Van Der Voort, S. S. E. M., Bartelink, M. E. L., Stoffers, H. E. J. H., Brooymans, F., Hendriks, H. J. M.& De Bie, R. A. (2014). KNGF-richtlijn Symptomatisch perifeer arterieel vaatlijden. www.kngfrichtlijnen.nl.
Nordanstig, J., Pettersson, M., Morgan, M., Falkenberg, M.& Kumlien, C. (2017). Assessment of Minimum Important Difference and Substantial Clinical Benefit with the Vascular Quality of Life Questionnaire-6 when Evaluating Revascularisation Procedures in Peripheral Arterial Disease. Eur J Vasc Endovasc Surg, 54(3), 340-347. https://doi.org/10.1016/j.ejvs.2017.06.022
Patterson, R. B., Pinto, B., Marcus, B., Colucci, A., Braun, T.& Roberts, M. (1997). Value of a supervised exercise program for the therapy of arterial claudication. J Vasc Surg, 25(2), 312-318; discussion 318-319. https://doi.org/10.1016/s0741-5214(97)70352-5
Regensteiner, J. G., Meyer, T. J., Krupski, W. C., Cranford, L. S.& Hiatt, W. R. (1997). Hospital vs home-based exercise rehabilitation for patients with peripheral arterial occlusive disease. Angiology, 48(4), 291-300. https://doi.org/10.1177/000331979704800402
Sandberg, A., Back, M., Cider, A., Jivegard, L., Sigvant, B., Wittboldt, S.& Nordanstig, J. (2023). Effectiveness of supervised exercise, home-based exercise, or walk advice strategies on walking performance and muscle endurance in patients with intermittent claudication (SUNFIT trial): a randomized clinical trial. Eur J Cardiovasc Nurs, 22(4), 400-411. https://doi.org/10.1093/eurjcn/zvac070
Sandercock, G. R., Hodges, L. D., Das, S. K.& Brodie, D. A. (2007). The impact of short term supervised and home-based walking programmes on heart rate variability in patients with peripheral arterial disease. J Sports Sci Med, 6(4), 471-476. https://www.ncbi.nlm.nih.gov/pubmed/24149480
Savage, P., Ricci, M. A., Lynn, M., Gardner, A., Knight, S., Brochu, M.& Ades, P. (2001). Effects of home versus supervised exercise for patients with intermittent claudication. J Cardiopulm Rehabil, 21(3), 152-157. https://doi.org/10.1097/00008483-200105000-00006
Sawilowsky, S. (2009). New Effect Size Rules of Thumb. Journal of Modern Applied Statistical Methods, 8(2).
Shea, B. J., Reeves, B. C., Wells, G., Thuku, M., Hamel, C., Moran, J., Moher, D., Tugwell, P., Welch, V., Kristjansson, E.& Henry, D. A. (2017). AMSTAR 2: a critical appraisal tool for systematic reviews that include randomised or non-randomised studies of healthcare interventions, or both. Bmj, 358, j4008. https://doi.org/10.1136/bmj.j4008
Society for Vascular Surgery Lower Extremity Guidelines Writing, G., Conte, M. S., Pomposelli, F. B., Clair, D. G., Geraghty, P. J., McKinsey, J. F., Mills, J. L., Moneta, G. L., Murad, M. H., Powell, R. J., Reed, A. B., Schanzer, A., Sidawy, A. N.& Society for Vascular, S. (2015). Society for Vascular Surgery practice guidelines for atherosclerotic occlusive disease of the lower extremities: management of asymptomatic disease and claudication. J Vasc Surg, 61(3 Suppl), 2S-41S. https://doi.org/10.1016/j.jvs.2014.12.009
Stiggelbout, A. M., Pieterse, A. H.& De Haes, J. C. (2015). Shared decision making: Concepts, evidence, and practice. Patient Educ Couns, 98(10), 1172-1179. https://doi.org/10.1016/j.pec.2015.06.022
Treat-Jacobson, D., Bronas, U. G.& Leon, A. S. (2009). Efficacy of arm-ergometry versus treadmill exercise training to improve walking distance in patients with claudication. Vasc Med, 14(3), 203-213. https://doi.org/10.1177/1358863X08101858
Ulfsdottir, H., Back, M., Cider, A., Jivegard, L., Sandberg, A., Nordanstig, J.& Svensson, M. (2023). Cost-Effectiveness of Exercise Therapy in Patients with Intermittent Claudication-A Comparison of Supervised Exercise, Home-Based Structured Exercise, and Walk Advice from the SUNFIT Trial. J Clin Med, 12(16). https://doi.org/10.3390/jcm12165277
van Asselt, A. D., Nicolai, S. P., Joore, M. A., Prins, M. H., Teijink, J. A.& Exercise Therapy in Peripheral Arterial Disease Study, G. (2011). Cost-effectiveness of exercise therapy in patients with intermittent claudication: supervised exercise therapy versus a ‘go home and walk’ advice. Eur J Vasc Endovasc Surg, 41(1), 97-103. https://doi.org/10.1016/j.ejvs.2010.06.024
van den Houten, M. M., Gommans, L. N., van der Wees, P. J.& Teijink, J. A. (2016a). Minimally Important Difference of the Absolute and Functional Claudication Distance in Patients with Intermittent Claudication. Eur J Vasc Endovasc Surg, 51(3), 404-409. https://doi.org/10.1016/j.ejvs.2015.11.008
van den Houten, M. M., Lauret, G. J., Fakhry, F., Fokkenrood, H. J., van Asselt, A. D., Hunink, M. G.& Teijink, J. A. (2016b). Cost-effectiveness of supervised exercise therapy compared with endovascular revascularization for intermittent claudication. Br J Surg, 103(12), 1616-1625. https://doi.org/10.1002/bjs.10247
van der Horst, D. E. M., Garvelink, M. M., Bos, W. J. W., Stiggelbout, A. M.& Pieterse, A. H. (2023). For which decisions is Shared Decision Making considered appropriate? – A systematic review. Patient Educ Couns, 106, 3-16. https://doi.org/10.1016/j.pec.2022.09.015
Wyrwich, K. W., Tierney, W. M., Babu, A. N., Kroenke, K.& Wolinsky, F. D. (2005). A comparison of clinically important differences in health-related quality of life for patients with chronic lung disease, asthma, or heart disease. Health Serv Res, 40(2), 577-591. A comparison of clinically important differences in health-related quality of life for patients with chronic lung disease, asthma, or heart disease – PubMed
Zatloukal, J., Ward, S., Houchen-Wolloff, L., Harvey-Dunstan, T.& Singh, S. (2019). The minimal important difference for the endurance shuttle walk test in individuals with chronic obstructive pulmonary disease following a course of pulmonary rehabilitation. Chronic Respiratory Disease, 16. https://doi.org/10.1177/1479973119853828
C.8.3 De keuze voor pijnvrije en/of niet-pijnvrije looptraining
Aanbevelingen
- Zet samen beslissen (persoonsgerichte zorg) in om samen met de patiënt een keuze te maken voor de in te zetten pijnintensiteit van de looptraining, gericht op het bevorderen van het fysiek functioneren en de kwaliteit van leven, binnen de fysio-/oefentherapeutische behandeling van patiënten met symptomatisch Perifeer Arterieel Vaatlijden (sPAV).
- Volg hierbij de vier stappen van het proces van samen beslissen zoals beschreven in module ‘A.8.2 Achtergrond (opent in nieuw tabblad)’ .
o Betrek bij stap twee ‘option talk’:
- de beschikbare wetenschappelijke kennis over de pijnintensiteit van de looptraining (zie ‘Toelichting: Conclusies op basis van de literatuur C.8.3’ );
- de klinische expertise van de therapeut met betrekking tot pijnvrije en niet-pijnvrije looptraining;
- de voor- en nadelen van pijnvrije of niet-pijnvrije looptraining (waarin o.a. aandacht is voor de FITT-factoren: Frequentie, Intensiteit, Tijd, en Type van de looptraining);
- de trainingsprincipes (zoals de specificiteit van pijnvrije of niet-pijnvrije looptraining in relatie tot de trainingsdoelen en de mogelijkheid om met een bepaalde pijnintensiteit de minimaal vereiste drempel voor een trainingsprikkel – en vervolgens een trainingseffect – te kunnen bereiken);
- de verwachte uitkomsten van pijnvrije of niet-pijnvrije looptraining (zie ‘Verantwoording: Effectiviteit en bewijskracht C.8.3’ );
- de invloed en de gevolgen van de pijnintensiteit op de persoonlijke situatie en mogelijkheden van de patiënt (o.a. comorbiditeit, bewegingsangst en arbeidsomstandigheden).
- Evalueer de voortgang van de behandeling op gezette tijden (zie KNGF-richtlijn sPAV ) en zet samen beslissen in om samen met de patiënt te bespreken of de gekozen pijnintensiteit nog voldoende op hem is afgestemd.
| Definitie ‘pijnintensiteit van de training’ of ‘mate van pijn tijdens de training’ Wanneer binnen deze module wordt gesproken over ‘pijnintensiteit van de training’ of ‘mate van pijn tijdens de training’ wordt bedoeld: de pijnklachten die een patiënt aan zijn onderste extremiteit ervaart ten gevolge van claudicatio intermittens. |
Beschrijving
Uit de bevindingen van de beschikbare wetenschappelijke literatuur kan niet worden geconcludeerd dat niet-pijnvrije looptraining beter of slechter is voor het fysiek functioneren en de kwaliteit van leven dan pijnvrije looptraining. Kortom, we zijn zeer onzeker of de ene vorm van training effectiever is dan de andere. Uit de voorkeuren van patiënten, de klinische expertise van therapeuten en de voor- en nadelen van de interventies blijkt dat zowel pijnvrije als niet-pijnvrije looptraining als relevante behandeloptie wordt beschouwd. In deze module wordt hierdoor geen aanbeveling gegeven voor één specifieke behandeloptie, maar wordt het toepassen van samen beslissen om te komen tot een keuze voor de pijnintensiteit van de training, nog belangrijker om het fysiek functioneren en de kwaliteit van leven te bevorderen binnen de fysio-/oefentherapeutische behandeling van patiënten met sPAV.
Aanleiding
Conform (inter)nationale richtlijnen is gesuperviseerde beweegtraining of looptraining de primair aanbevolen behandeling voor patiënten met symptomatisch Perifeer Arterieel Vaatlijden (sPAV) (Aboyans, 2018; Bartelink, 2014; Merry, 2014; Society for Vascular Surgery Lower Extremity Guidelines Writing, 2015). Desalniettemin zijn voor het vormgeven van het fysio-/oefentherapeutische behandelplan verschillende vormen en doseringen van beweeg- of looptraining mogelijk (Merry, 2014). Het behandelplan omvat daarmee meerdere beslissingen waarbij ruimte is voor samen beslissen. Dit is bij uitstek het geval bij beslissingen waarbij meerdere redelijke opties bestaan en de uiteindelijke keuze afhangt van de persoonlijke voorkeuren en waarden van de patiënt, of bij beslissingen waarbij de betrokkenheid en toewijding van de patiënt cruciaal zijn voor de uitvoering van de behandeling, zoals bij leefstijlkeuzes (van der Horst, 2023).
Uit de knelpuntenanalyse (gericht op samen beslissen) blijkt dat therapeuten vaak het gevoel hebben dat gesuperviseerde pijninducerende looptraining de primair in te zetten interventie moet zijn. Voor veel therapeuten is het onvoldoende duidelijk wat de voor- en nadelen van de verschillende mogelijke behandelopties zijn binnen de behandeling van patiënten met sPAV. Dit terwijl inzicht hebben in de beschikbare wetenschappelijke evidentie, en daarmee in de waarde van de verschillende behandelopties, juist van belang is voor het effectief toepassen van samen beslissen. Het aanbieden van deze kennis, naast de kennis uit de KNGF-richtlijn sPAV uit 2014 , kan fysio-/oefentherapeuten ondersteunen tijdens het samen beslissen, en helpen om patiënten met sPAV goed te laten participeren tijdens het proces van samen beslissen. Dit is vooral waardevol tijdens de option talk. Option talk, oftewel het optiegesprek, is een van de essentiële stappen in het proces van samen beslissen en omvat het informeren van de patiënt over de mogelijke behandelopties, inclusief bijbehorende voor- en nadelen, op basis van de beschikbare (of soms beperkte) wetenschappelijke kennis en klinische expertise (Elwyn, 2017; Stiggelbout, 2015).
Binnen deze module C.8.3 wordt ingegaan op de waarde van pijnvrije looptraining ten opzichte van niet-pijnvrije looptraining bij patiënten met sPAV. Veelal wordt geadviseerd om te trainen tot gemiddelde tot maximale claudicatioklachten, om vervolgens een rustpauze in te lassen tot de klachten weer zijn verdwenen (Fakhry, 2012; Gerhard-Herman, 2017; Gommans, 2014). Uit de knelpuntenanalyse blijkt dat het voor therapeuten onduidelijk is wat de waarde is van pijnvrije (loop)training en in welke gevallen dit een relevante behandeloptie is om aan te bieden ten opzichte van niet-pijnvrije looptraining. In de praktijk wordt nu vaak gekozen voor niet-pijnvrije looptraining. Echter is dit niet altijd goed uitvoerbaar door patiënten of kan zorgen voor verminderde motivatie, wat weer een negatieve invloed kan hebben op therapietrouw en zelfredzaamheid.
Om therapeuten inzicht te geven in de beschikbare wetenschappelijke evidentie is het van belang om aanbevelingen te formuleren voor de gewenste en ongewenste effecten van pijnvrije looptraining ten opzichte van niet-pijnvrije looptraining bij patiënten met sPAV. Hiertoe is de volgende uitgangsvraag geformuleerd:
Uitgangsvraag
Kan in plaats van niet-pijnvrije looptraining ook gekozen worden voor pijnvrije looptraining bij patiënten met sPAV?
Conclusies op basis van de literatuur
Binnen de huidige module C.8.3 zijn de resultaten van de geselecteerde literatuur niet geïncludeerd in een meta-analyse en zijn geen gestandaardiseerde resultaten geformuleerd conform de GRADE-methodiek (Langendam, 2022).
Cruciale uitkomstmaten:
- Drie geselecteerde studies rapporteerden resultaten over het effect van pijnvrije looptraining ten opzichte van niet-pijnvrije looptraining op fysiek functioneren (gemeten als de totale loopafstand met de zes minuten wandeltest (6MWT), of de functionele en maximale loopafstand met de loopbandtest) bij patiënten met sPAV. Eén studie rapporteerde data (totale loopafstand (6MWT) en maximale loopafstand (loopbandtest)) met een follow-up van zes en twaalf maanden, één studie rapporteerde data (functionele en maximale loopafstand (loopbandtest)) met een follow-up van drie maanden en één studie rapporteerde niet-normaal verdeelde data (functionele en maximale loopafstand (loopbandtest)) met een follow-up van drie maanden. Vanwege deze verschillen waren de resultaten van de studies niet goed te vergelijken en is ervoor gekozen om de resultaten over het effect op fysiek functioneren enkel narratief te beschrijven en is geen conclusie geformuleerd volgens de GRADE-methodiek.
- Twee geselecteerde studies rapporteerden resultaten over het effect van pijnvrije looptraining ten opzichte van niet-pijnvrije looptraining op kwaliteit van leven (gemeten met de SF-36 of de WIQ) bij patiënten met sPAV. Eén studie rapporteerde niet-normaal verdeelde data met een follow-up van drie maanden, en één studie rapporteerde normaal verdeelde data met een follow-up van zes en twaalf maanden. Vanwege deze verschillen waren de resultaten van de studies niet goed te vergelijken en is ervoor gekozen om de resultaten over het effect op kwaliteit van leven narratief te beschrijven en is geen conclusie geformuleerd volgens de GRADE-methodiek.
- Er zijn geen studies gevonden die resultaten hebben beschreven op de overige cruciale uitkomstmaten: mate van pijn, levensverwachting en arbeidsparticipatie.
Belangrijke uitkomstmaten:
- Twee van de drie geselecteerde studies beschreven resultaten over ongewenste effecten gerelateerd aan een van de interventies. Eén studie rapporteerde geen ongewenste effecten, en één studie rapporteerde geen verschillen in ongewenste effecten tussen pijnvrije looptraining en niet-pijnvrije looptraining. In deze studie werd in beide groepen één ongewenst voorval beschreven waardoor patiënten deelname aan de studie moesten beëindigen (supraventriculaire aritmie en angina pectoris).
Rationale van de aanbeveling
De werkgroep heeft besloten om een sterke aanbeveling voor het toepassen van samen beslissen op te nemen in deze richtlijnmodule. Hierbij waren er een aantal criteria (zie Verantwoording; ‘Van bewijs naar aanbeveling’) die zwaar en minder zwaar hebben gewogen.
Uit de resultaten van het systematische literatuuronderzoek kan niet worden geconcludeerd dat niet-pijnvrije looptraining beter is voor het fysiek functioneren en de kwaliteit van leven op korte termijn (<1 jaar) dan pijnvrije looptraining. Tegelijkertijd kan ook niet worden geconcludeerd dat pijnvrije looptraining beter is voor het fysiek functioneren en de kwaliteit van leven dan niet-pijnvrije looptraining. Kortom, we zijn zeer onzeker of de ene vorm van training effectiever is dan de andere. Wel suggereren de resultaten dat zowel pijnvrije als niet-pijnvrije looptraining mogelijk positieve effecten hebben op fysiek functioneren en kwaliteit van leven. Het besluit van de werkgroep dat hieruit voortkomt, is dat pijnvrije looptraining mogelijk niet onderdoet voor niet-pijnvrije looptraining wanneer men kijkt naar de effecten op fysiek functioneren en kwaliteit van leven, en daarmee een goed alternatief kan zijn binnen de fysio-/oefentherapeutische behandeling van patiënten met sPAV.
Een achterbanraadpleging onder patiënten met sPAV laat zien dat veel variatie bestaat in de voorkeur en waardering van patiënten ten aanzien van de pijnintensiteit van de looptraining. Patiënten hechten veel waarde aan het kunnen kiezen voor een bepaalde pijnintensiteit.
De werkgroep beoordeelt dat de resultaten van het systematische literatuuronderzoek en de voorkeuren van patiënten laten zien dat voor zowel pijnvrije als niet-pijnvrije looptraining geldt dat de gewenste effecten (positieve effecten op fysiek functioneren en kwaliteit van leven) de ongewenste effecten overtreffen.
De economische overwegingen en kosteneffectiviteit zijn gelijkwaardig voor pijnvrije en niet-pijnvrije looptraining. De werkgroep verwacht dat het aanbieden van pijnvrije looptraining naast niet-pijnvrije looptraining kan zorgen voor een toename van de gezondheidsgelijkheid, doordat de aangeboden zorg beter kan worden afgestemd op de individuele patiënt (inclusieve zorg). De overige criteria van het proces van bewijs naar aanbeveling (aanvaardbaarheid en haalbaarheid) worden als niet-bezwaarlijk bevonden in het aanbieden van andere vormen van pijnvrije looptraining naast niet-pijnvrije looptraining.
Concluderend is het wetenschappelijk bewijs onzeker voor het effect van pijnvrije looptraining ten opzichte van niet-pijnvrije looptraining, maar beoordeelt de werkgroep dat de gunstige effecten en de voorkeuren van patiënten overheersend zijn, waardoor er een sterke aanbeveling is geformuleerd voor het toepassen van samen beslissen om te komen tot een keuze voor de pijnintensiteit.
Literatuur
Zoeken en selecteren
Onderzoeksvraag
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende onderzoeksvraag:
- Wat is het effect van pijnvrije looptraining ten opzichte van niet-pijnvrije looptraining op het fysiek functioneren, de kwaliteit van leven, de mate van pijn, de levensverwachting en de arbeidsparticipatie bij patiënten met symptomatisch Perifeer Arterieel Vaatlijden (sPAV)?
Relevante uitkomstmaten
De werkgroep achtte het fysiek functioneren, de kwaliteit van leven, de mate van pijn, de levensverwachting en de arbeidsparticipatie cruciale uitkomstmaten voor de besluitvorming. De werkgroep achtte ongewenste effecten gerelateerd aan een van de interventies, belangrijke uitkomstmaten.
Per uitkomstmaat:
- Fysiek functioneren
- Zes minuten wandeltest (6MWT): Uit de wetenschappelijke literatuur blijkt dat een verschil van acht meter als belangrijk effect beschouwd kan worden bij patiënten met PAV (klinisch relevant verschil) (McDermott, 2021b). De werkgroep beschouwt* deze waarden ook als klinisch relevant voor patiënten met sPAV.
- Loopbandtest: De werkgroep definieerde*, op basis van de wetenschappelijke literatuur, een verschil van 250 meter (functionele loopafstand) en 305 meter (maximale loopafstand) als belangrijk effect bij patiënten met sPAV (klinisch relevant verschil) (van den Houten, 2016a).
- Shuttle Walk Test (SWT): Uit de wetenschappelijke literatuur blijkt dat een verschil van 174 seconden als belangrijk effect beschouwd kan worden bij patiënten met COPD (klinisch relevant verschil) (Zatloukal, 2019). Omdat wetenschappelijke literatuur over de klinische relevantie bij patiënten met sPAV ontbreekt, beschouwt* de werkgroep deze waarden als voldoende gelijkwaardig en daarmee als ook klinisch relevant voor patiënten met sPAV.
- Walking Impairment Questionnaire (WIQ): De werkgroep definieerde*, op basis van de wetenschappelijke literatuur, een verschil van 0.11 punten (op een schaal van 0 tot 1, waarbij een hogere score correspondeert met een betere mate van fysiek functioneren) als belangrijk effect bij patiënten met sPAV (klinisch relevant verschil) (Conijn, 2015).
- Kwaliteit van leven
- 36-Item Short Form Health Survey (SF-36): Uit de wetenschappelijke literatuur blijkt dat een verschil van 10 punten (physical functioning, bodily pain, general health en mental health), 12.5 punten (physical role, vitality en social functioning) en 8.3 punten (emotional role) als belangrijk effect beschouwd kan worden bij patiënten met COPD (klinisch relevant verschil) (Wyrwich, 2005). De schaal van de SF-36 loopt van 0 tot 100, waarbij een hogere score correspondeert met een betere kwaliteit van leven. Omdat wetenschappelijke literatuur over de klinische relevantie bij patiënten met sPAV ontbreekt, beschouwt* de werkgroep deze waarden als voldoende gelijkwaardig en daarmee als ook klinisch relevant voor patiënten met sPAV.
- Vascular Quality of Life Questionnaire-6 (VascuQol-6): De werkgroep definieerde*, op basis van de wetenschappelijke literatuur, een verschil van 1.7 punten (op een schaal van 6 tot 24, waarbij een hogere score correspondeert met een betere kwaliteit van leven) als belangrijk effect bij patiënten met sPAV (klinisch relevant verschil) (Nordanstig, 2017).
- EuroQol (EQ-5D): Uit de wetenschappelijke literatuur blijkt dat een verschil van 0.028 punten (op een schaal van -1 tot 1, waarbij een hogere score correspondeert met een betere kwaliteit van leven) als belangrijk effect beschouwd kan worden bij patiënten met COPD (klinisch relevant verschil) (Bae, 2020). Omdat wetenschappelijke literatuur over de klinische relevantie bij patiënten met sPAV ontbreekt, beschouwt* de werkgroep deze waarden als voldoende gelijkwaardig en daarmee als ook klinisch relevant voor patiënten met sPAV.
- Mate van pijn
- Numerical pain rating scale (NPRS): Uit de wetenschappelijke literatuur blijkt dat een verschil van 2 punten (op een schaal van 0 tot 10, waarbij een hogere score correspondeert met een hogere mate van pijn) als belangrijk effect beschouwd kan worden bij patiënten met chronische pijn (klinisch relevant verschil) (Farrar, 2001). Omdat wetenschappelijke literatuur over de klinische relevantie bij patiënten met sPAV ontbreekt, beschouwt* de werkgroep deze waarden als voldoende gelijkwaardig en daarmee als ook klinisch relevant voor patiënten met sPAV.
- Levensverwachting
- Mortaliteit: De werkgroep definieerde* een verschil van 1 op 100 personen als belangrijk effect bij patiënten met sPAV (klinisch relevant verschil).
- Arbeidsparticipatie
- Voor het meten van de arbeidsparticipatie is op voorhand geen meetinstrument met bijbehorende grenzen van klinische relevantie vastgesteld.
- Ongewenste effecten
- Major Adverse Events (ernstige ongewenste voorvallen): De werkgroep definieerde* een verschil van 1 op 50 personen als belangrijk effect bij patiënten met sPAV (klinisch relevant verschil).
- Ziekenhuisopnames: De werkgroep definieerde* een verschil van 1 op 50 personen als belangrijk effect bij patiënten met sPAV (klinisch relevant verschil).
* De werkgroep benadrukt dat het per individu kan verschillen of een effect wel of niet als klinisch relevant wordt beschouwd. Dit kan bijvoorbeeld afhankelijk zijn van de individuele hulpvraag en/of therapiedoelen. Desondanks zijn voor de start van het literatuuronderzoek bovenstaande specifieke grenzen voor klinische relevantie vastgesteld. De genoemde meetinstrumenten met bijbehorende criteria dienen als leidraad voor deze richtlijnmodule, met ruimte voor aanpassingen op basis van individuele patiëntbehoeften. De meetinstrumenten (opent in nieuw tabblad) genoemd in de generieke KNGF-richtlijn sPAV blijven de basis vormen voor diagnostiek en evaluatie.
Zoekactie
Op 17 augustus 2023 is door L. Marcellis (met ondersteuning van informatiespecialist A. Tillema) een systematische zoekactie uitgevoerd in MEDLINE, Embase, Cinahl en Cochrane (zie bijlage C.8.4-1 (opent in nieuw tabblad) voor de zoekverantwoording). De systematische zoekactie leverde 4.602 unieke treffers op. Na screening (door D. Conijn (DC), L. Marcellis (LM), M. Simon (MS) en T. Hoogeboom (TH)) van de titel en het abstract op de inclusiecriteria en exclusiecriteria (zie tabel 1) zijn 4.451 artikelen geëxcludeerd. Gekozen werd om artikelen van voor 2005 te excluderen omdat er een duidelijke toename zichtbaar was van het aantal publicaties in 2005. Artikelen waarvan het op basis van titel en abstract niet duidelijk was of deze voldeden aan de inclusiecriteria werden dubbel gescreend door LM en vervolgens onderling besproken. Van 148 studies is het volledige artikel gescreend door LM waarbij twijfelgevallen dubbel werden gescreend door DC en vervolgens onderling werden besproken. Uiteindelijk leverde de zoekactie negentien studies (gerapporteerd in 22 artikelen) op voor modules C.8.1, C.8.2, C.8.3 en C.8.4.
Voor module C.8.3 werden drie studies geselecteerd (McDermott, 2021a; Mika, 2013; Novaković, 2019). Zie bijlage C.8.3-2 (opent in nieuw tabblad) voor het stroomdiagram van het inclusieproces. De artikelen die op basis van de volledige tekst zijn geëxcludeerd, en de reden van exclusie zijn weergegeven in bijlage C.8.3-3 (opent in nieuw tabblad).
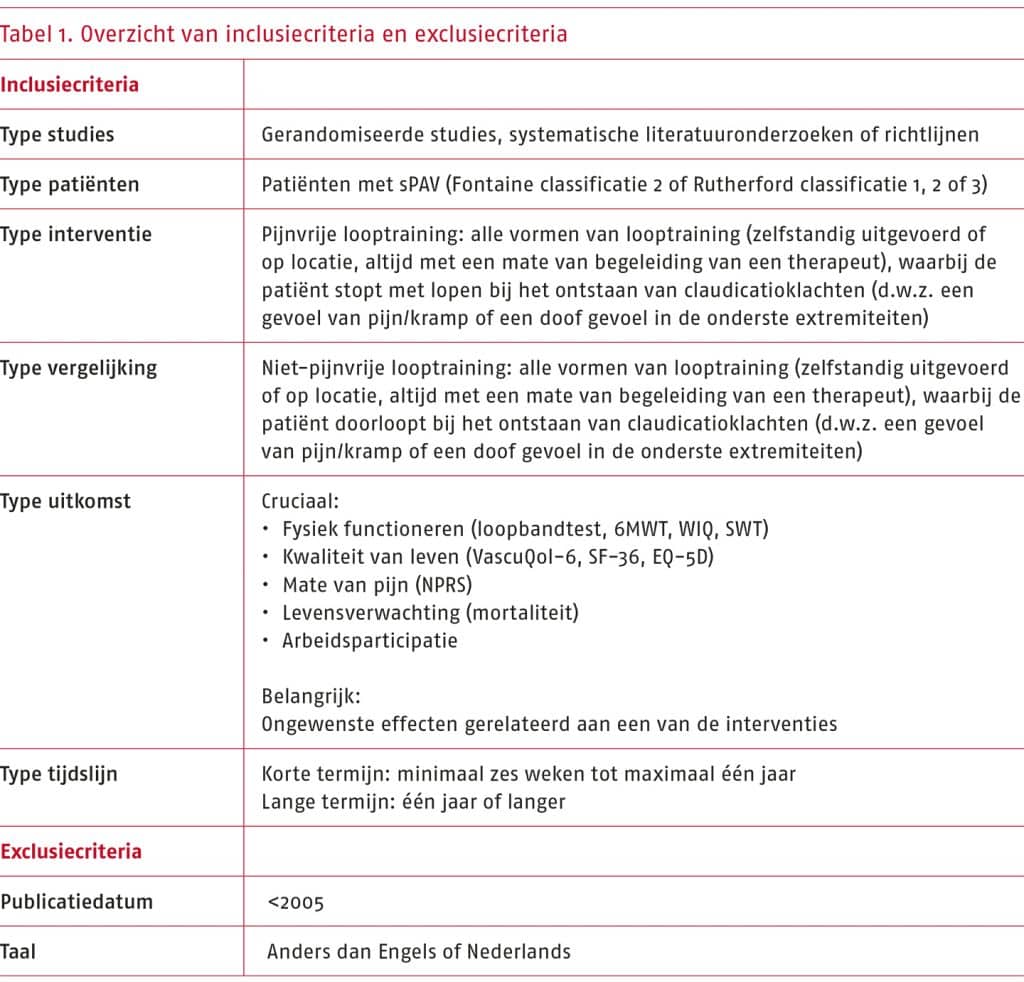
Karakteristieken van geïncludeerde studies
De kenmerken van de geïncludeerde studies zijn weergegeven in bijlage C.8.3-4 (opent in nieuw tabblad). De drie ingesloten studies includeerden in totaal 324 patiënten met sPAV.
De RCT van McDermott et al. beschrijft 240 patiënten met sPAV (McDermott, 2021a). De studie werd uitgevoerd in de Verenigde Staten. De uitgevoerde interventie door patiënten in de interventiegroep (n=116, leeftijd 69.8 ± 10.1 jaar, 46.6% vrouw) was looptraining in een tempo zonder ischemische beenklachten. Patiënten in de controlegroep (n=124, leeftijd 68.8 ± 8.7 jaar, 48.4% vrouw) voerden looptraining uit in een tempo dat matige tot ernstige ischemische beenklachten induceerde. Beide groepen trainden niet-gesuperviseerd met een geadviseerde frequentie van vijf keer per week, tot 50 minuten per sessie, gedurende twaalf maanden. Alle patiënten droegen een activiteitenmeter tijdens de training en hadden wekelijks telefonisch contact met een coach.
De RCT van Novaković et al. beschrijft 24 patiënten met sPAV (Novaković, 2019). De studie werd uitgevoerd in Slovenië. De uitgevoerde interventie door patiënten in de interventiegroep (n=12, leeftijd 65.6 ± 11.0 jaar, 18% vrouw) was looptraining op een loopband. Patiënten liepen tot twee derde van de afstand waarop pijnklachten ontstaan (functionele loopafstand) en wisselden dit af met minimaal vijf minuten actief herstel op een hometrainer (zonder weerstand). Patiënten in de controlegroep (n=12, leeftijd 65.1 ± 7.6 jaar, 40% vrouw) voerden looptraining uit op een loopband tot het optreden van matige claudicatioklachten (graad 3 tot 4 op een 5-puntsschaal) en wisselden dit af met minimaal vijf minuten actief herstel op een hometrainer (zonder weerstand) tot de pijnklachten waren verdwenen. Beide groepen trainden gesuperviseerd, met een duur van 60 minuten en een frequentie van twee of drie keer – afhankelijk van de voorkeur van de patiënt – per week gedurende twaalf weken (maximaal 36 sessies in totaal).
De RCT van Mika et al. beschrijft 60 patiënten met sPAV (Mika, 2013). De studie werd uitgevoerd in Polen. De uitgevoerde interventie door patiënten in de interventiegroep (n=30, leeftijd 65.2 ± 8.0 jaar, 36% vrouw) was looptraining op een loopband. Patiënten liepen tot het ontstaan van claudicatioklachten (graad 2 op een 5-puntsschaal) en wisselden dit af met rust tot de pijnklachten waren verdwenen. Patiënten in de controlegroep (n=30, leeftijd 64.8 ± 7.2 jaar, 41% vrouw) voerden looptraining uit op een loopband. Patiënten liepen tot het optreden van matige claudicatioklachten (graad 4 op een 5-puntsschaal) en wisselden dit af met rust tot de pijnklachten waren verdwenen. Beide groepen trainden gesuperviseerd gedurende twaalf weken, met een duur van 35 minuten (start training) tot 60 minuten (na twaalf weken) en een frequentie van drie keer per week.
Individuele studiekwaliteit (RoB)
Het risico op vertekening (risk of bias, RoB) van de gerandomiseerde studies is dubbel gescoord door LM en DC, LM en TH of LM en MS met behulp van de Cochrane Risk-of-Bias-2 tool (Higgins, 2019). Inconsistentie in het oordeel op de verschillende items is onderling besproken (LM en DC, LM en TH of LM en MS), waarna consensus is bereikt. Een overzicht van de beoordeling van de studiekwaliteit (RoB) per studie is weergegeven in bijlage C.8.3-5 (opent in nieuw tabblad) Risk-of-bias-tabel.
Effectiviteit en bewijskracht
Zie de Toelichting voor de conclusies op basis van de literatuur. Hieronder volgt een beschrijving van de effectiviteit en de bewijskracht voor de vergelijking(en).
Pijnvrije looptraining versus niet-pijnvrije looptraining
Het effect van pijnvrije looptraining vergeleken met dat van niet-pijnvrije looptraining bij patiënten met sPAV is beschreven in drie studies (McDermott, 2021a; Mika, 2013; Novaković, 2019). Geen van de drie studies is geïncludeerd in een meta-analyse. Eén studie kon niet worden geïncludeerd vanwege niet-normaal verdeelde data (Novaković, 2019). De overige twee studies rapporteerden data op verschillende meetmomenten (drie maanden (Mika, 2013), of zes en twaalf maanden (McDermott, 2021a)). Hieronder worden de uitkomstmaten per studie narratief beschreven.
Individuele RCT’s
McDermott et al.
De studie van McDermott et al. rapporteerde data over fysiek functioneren (gemeten als totale loopafstand met de 6MWT na zes en twaalf maanden, maximale looptijd met de loopbandtest na twaalf maanden, en WIQ distance en speed na zes en twaalf maanden) en kwaliteit van leven (gemeten met SF-36 physical functioning na zes en twaalf maanden) (McDermott, 2021a). Alle data worden gepresenteerd als gemiddelde verandering (95%-BI) (zie tabel 2).
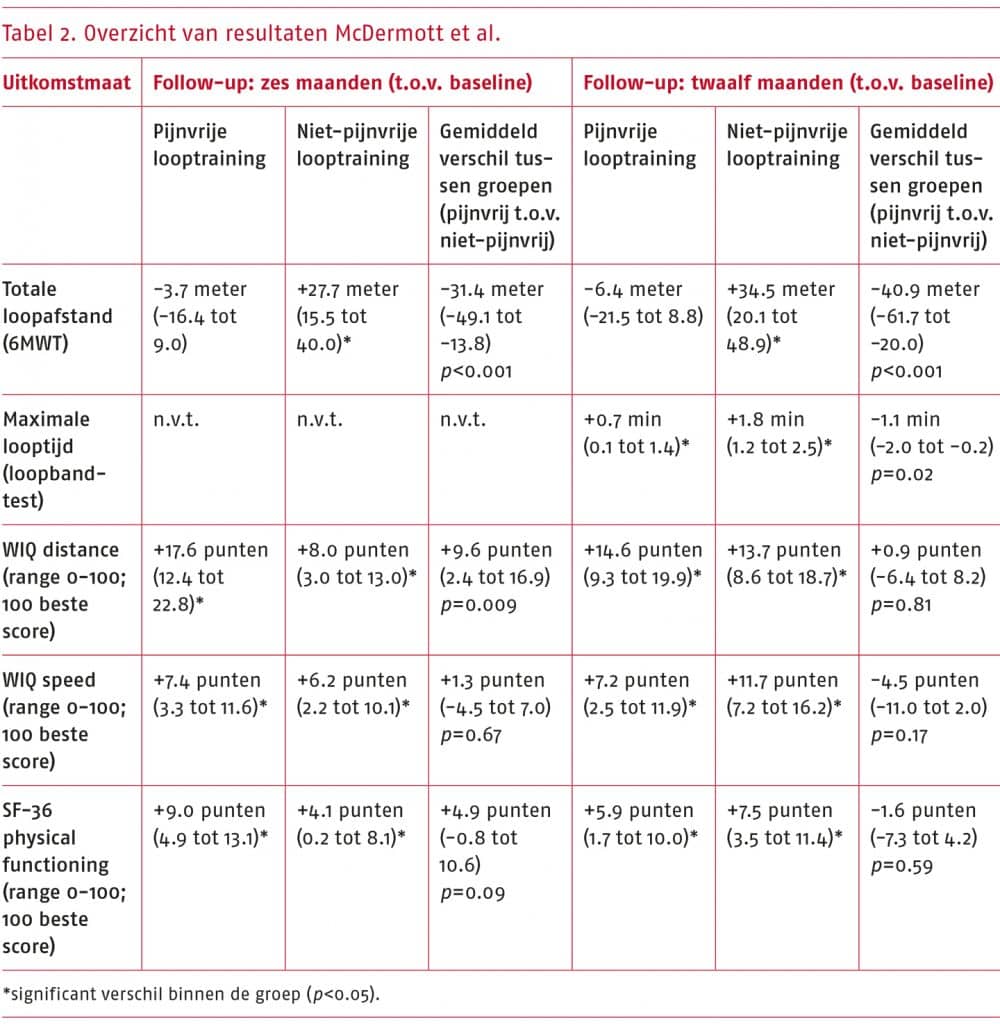
Novaković et al.
De studie van Novaković et al. rapporteerde data na drie maanden over fysiek functioneren (gemeten als functionele loopafstand en maximale loopafstand met de loopbandtest) en kwaliteit van leven (gemeten met de SF-36). Alle data worden gepresenteerd als mediaan (IQR) vanwege een niet-normale verdeling van de data (zie tabel 3). De studie beschrijft dat geen significante verschillen werden gevonden tussen de groepen (p-waarden niet gerapporteerd) (Novaković, 2019).
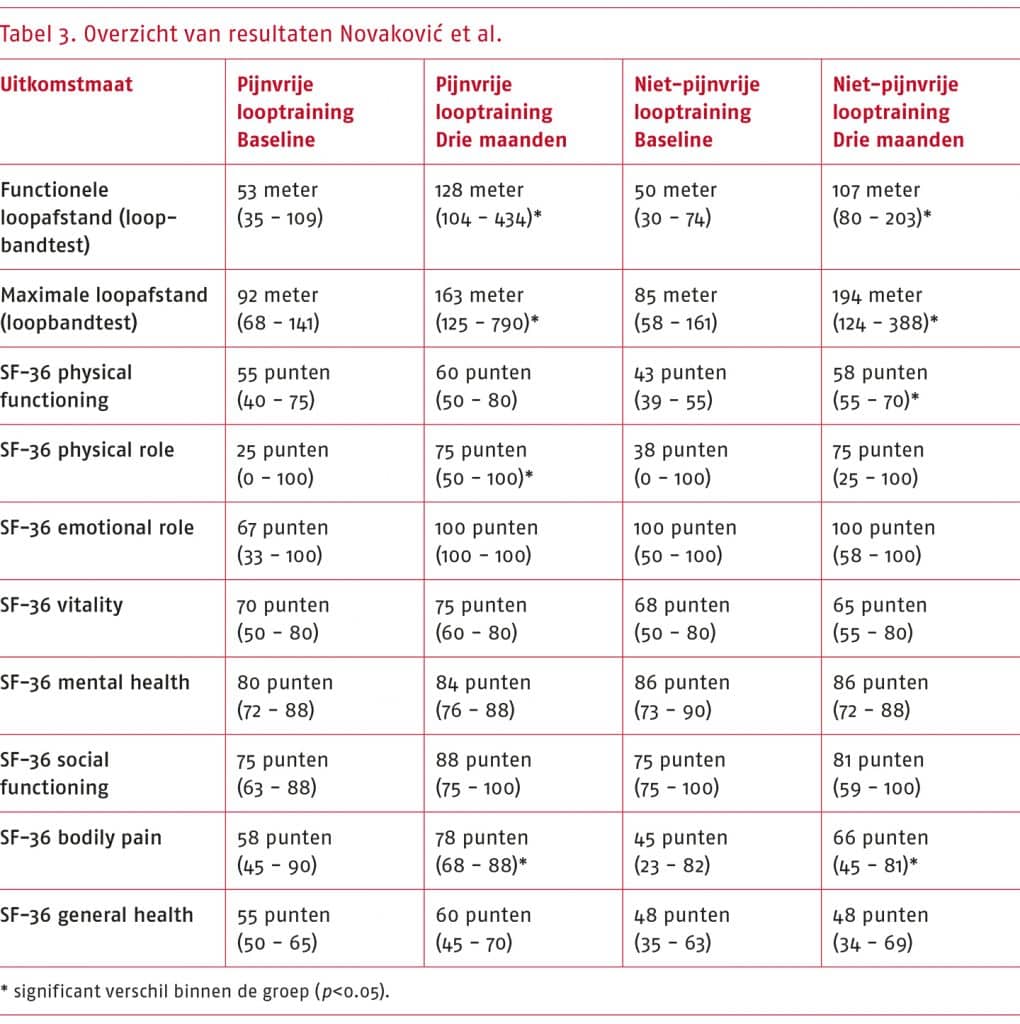
Mika et al.
De studie van Mika et al. rapporteerde data na drie maanden over fysiek functioneren (gemeten als functionele looptijd en maximale looptijd met de loopbandtest) (Mika, 2013). Alle data worden gepresenteerd als gemiddelde ± SD (zie tabel 4).
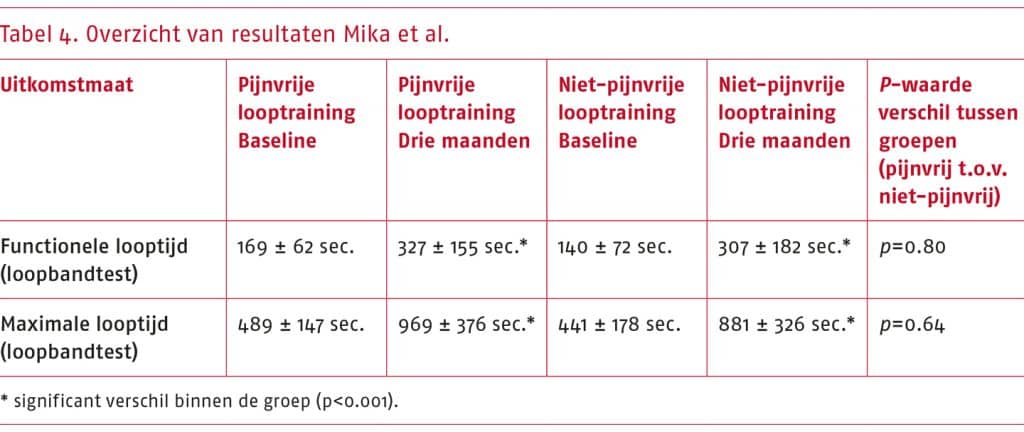
Ongewenste effecten
Twee studies beschreven resultaten met betrekking tot ongewenste effecten (McDermott, 2021a; Novaković, 2019). De studie van McDermott et al. rapporteerde 74 ongewenste voorvallen in de groep pijnvrije looptraining (0,64 ongewenste voorvallen per patiënt) en 80 ongewenste voorvallen in de groep niet-pijnvrije looptraining (0,65 ongewenste voorvallen per patiënt). Slechts één ongewenst voorval per groep was gerelateerd aan deelname aan de studie: één patiënt in de groep pijnvrije training ontwikkelde supraventriculaire aritmie tijdens de baselinetesten, en één patiënt in de groep niet-pijnvrije training ontwikkelde pijn op de borst tijdens de training. Beide patiënten ondergingen een operatie voor het plaatsen van een coronaire stent (McDermott, 2021a). De studie van Novaković et al. rapporteerde dat sterfgevallen, ongewenste voorvallen of neveneffecten van interventies niet zijn voorgevallen (Novaković, 2019).
Overige uitkomstmaten
Er zijn geen studies gevonden die resultaten hebben beschreven op de overige cruciale uitkomstmaten (mate van pijn, levensverwachting en arbeidsparticipatie).
Van bewijs naar aanbeveling
Criteria
Het onderdeel van bewijs naar aanbeveling bevat negen criteria, die hieronder worden opgesomd.
Gewenste effecten
De werkgroep heeft geen gestandaardiseerde gewenste effecten geformuleerd middels GRADE, omdat de resultaten uit de geselecteerde literatuur enkel narratief zijn beschreven.
De beschreven effecten vanuit de literatuur laten zien dat zowel pijnvrije looptraining als niet-pijnvrije looptraining zorgt voor een statistisch significante verbetering van het fysiek functioneren en de kwaliteit van leven bij patiënten met sPAV. Slechts één van de drie geïncludeerde studies rapporteert (tegengestelde) significante verschillen tussen pijnvrije en niet-pijnvrije looptraining. Het fysiek functioneren (gemeten als totale loopafstand met de 6MWT en maximale loopafstand met de loopbandtest) verbeterde in de studie van McDermott et al. significant beter in de groep niet-pijnvrije looptraining ten opzichte van de groep pijnvrije looptraining (McDermott, 2021a). Daarnaast rapporteren McDermott et al. dat zowel het fysiek functioneren (gemeten als WIQ distance na zes maanden) als de kwaliteit van leven (gemeten als SF-36 physical functioning na zes maanden) significant meer verbeterde in de groep pijnvrije looptraining ten opzichte van de groep niet-pijnvrije looptraining (McDermott, 2021a). De werkgroep beoordeelt alleen het gevonden effect op de totale loopafstand (6MWT) als klinisch relevant. De overige twee studies rapporteren wel significante verbeteringen op fysiek functioneren binnen de groepen, maar geen significante verschillen tussen de groepen (Mika, 2013; Novaković, 2019).
De werkgroep beoordeelt dat het aannemelijk is dat zowel het inzetten van pijnvrije looptraining als het inzetten van niet-pijnvrije looptraining waardevolle gewenste effecten heeft om het fysiek functioneren en de kwaliteit van leven bij patiënten met sPAV te verbeteren.
Ongewenste effecten
De werkgroep beoordeelt de kans op ongewenste effecten van niet-pijnvrije looptraining ten opzichte van pijnvrije looptraining als klein en is van mening dat het uitvoeren van zowel niet-pijnvrije als pijnvrije looptraining voor patiënten met sPAV veilig is. Twee van de drie studies rapporteerden informatie over ongewenste effecten gerelateerd aan een van de interventies. Eén studie rapporteerde geen ongewenste effecten, en één studie rapporteerde geen verschillen in ongewenste effecten tussen pijnvrije looptraining en niet-pijnvrije looptraining (de studie rapporteerde één ongewenst voorval per groep).
Door Gommans et al. is in een systematisch literatuuronderzoek onderzoek gedaan naar de veiligheid van gesuperviseerde beweeginterventies bij patiënten met sPAV, waarbij werd gekeken naar de complicatieratio (aantal ongewenste effecten per aantal trainingsuren) (Gommans, 2015). Deze systematische review includeerde 74 artikelen (waarvan 49 artikelen met als interventie gesuperviseerde looptraining) en rapporteerde een complicatieratio van één ongewenst voorval per 10.340 trainingsuren. Gommans et al. concluderen dat gesuperviseerde beweeginterventies veilig zijn voor patiënten met sPAV met een buitengewoon lage complicatieratio. De werkgroep beoordeelt dat deze studie aantoont dat trainen met begeleiding van een fysio- of oefentherapeut, onafhankelijk of het looptraining met of zonder pijnklachten betreft, veilig en daarmee verantwoord is.
De werkgroep wil benadrukken dat iedere patiënt zorgvuldige monitoring en daarmee een bepaalde mate van begeleiding van een fysio- of oefentherapeut moet krijgen om de veiligheid te kunnen garanderen. Dit kan variëren van trainen met supervisie in de praktijkruimte van de therapeut, tot zelfstandig trainen met supervisie van de therapeut op afstand.
Kwaliteit van bewijs
De systematische literatuuranalyse levert geen directe input voor de bewijskracht voor het beantwoorden van de uitgangsvraag. Hierdoor heeft de werkgroep geen kwaliteit van bewijs op basis van de GRADE-beoordeling geformuleerd.
Waarden en voorkeuren van patiënten
De werkgroep is tot het oordeel gekomen dat patiënten grote waarde hechten aan de gekozen trainingsintensiteit (de mate van pijn waarmee getraind wordt) en dat daar weinig variatie in zit tussen patiënten. De werkgroep beoordeelt dat voorkeuren van patiënten omtrent pijnintensiteit tijdens het trainen uiteenlopen en dat deze per patiënt verschillend zullen zijn.
Dit wordt ondersteund door een achterbanraadpleging (n=60 patiënten met sPAV) van Stichting Harteraad. Uit de resultaten van deze raadpleging blijkt dat 55% van de patiënten een voorkeur heeft voor niet-pijnvrije looptraining, 35% een voorkeur heeft voor pijnvrije looptraining, en 10% geen specifieke voorkeur heeft. Redenen waarom patiënten een voorkeur hebben voor niet-pijnvrije looptraining zijn de ervaring dat dit een effectieve trainingsvorm is, gewenning aan pijnklachten en daardoor minder last van de pijn, en de mogelijkheid om alsnog te kunnen stoppen als de pijn te erg wordt. Redenen waarom patiënten een voorkeur hebben voor pijnvrije looptraining zijn de onmogelijkheid om door te lopen met pijn, het feit dat de pijn demotiverend is en de ervaring dat het stoppen voordat de pijn ontstaat, zorgt voor een sneller herstel.
Balans gewenste en ongewenste effecten
De werkgroep is tot het oordeel gekomen dat de gewenste effecten van het aanbieden van pijnvrije looptraining als alternatief voor niet-pijnvrije looptraining zeker de ongewenste effecten overtreffen.
De motivatie hiervoor is:
- Zowel pijnvrije looptraining als niet-pijnvrije looptraining heeft positieve effecten op het fysiek functioneren en de kwaliteit van leven van patiënten met sPAV. Uit de resultaten van de wetenschappelijke literatuur kan niet worden geconcludeerd dat de gewenste effecten van niet-pijnvrije looptraining groter zijn dan de gewenste effecten van pijnvrije looptraining. Pijnvrije looptraining is daarmee een geschikt alternatief voor niet-pijnvrije looptraining, met vergelijkbare gewenste effecten zonder relevante ongewenste effecten.
- Er zijn geen aanwijzingen dat niet-pijnvrije looptraining onveiliger is dan pijnvrije looptraining bij patiënten met sPAV.
- Patiënten met sPAV hebben verschillende voorkeuren voor de pijnintensiteit tijdens de looptraining en hechten veel waarde aan het kunnen kiezen voor een bepaalde mate van pijn tijdens het trainen. Dit maakt dat vanuit patiëntperspectief geen generieke voorkeur bestaat voor pijnvrije of niet-pijnvrije looptraining.
- De werkgroep verwacht dat het aanpassen van de trainingsvorm aan de voorkeuren van de patiënt, en dus zowel pijnvrije als niet-pijnvrije looptraining aanbieden, een positieve invloed kan hebben op therapietrouw, motivatie en zelfmanagement, wat weer kan bijdragen aan mogelijk positievere effecten van training (Daley, 2003; Lin, 2019; Parfitt, 2004).
Economische overwegingen en kosteneffectiviteit
De werkgroep beoordeelt de benodigde middelen voor pijnvrije looptraining ten opzichte van niet-pijnvrije looptraining als vergelijkbaar. De keuze voor een bepaalde mate van pijn heeft geen invloed op de benodigde middelen.
Gesuperviseerde beweegtraining is een aangetoond kosteneffectieve behandeling (Fokkenrood, 2014; van Asselt, 2011; van den Houten, 2016b). De werkgroep vindt het aannemelijk dat zowel pijnvrije als niet-pijnvrije looptraining onder gesuperviseerde beweegtraining valt. De werkgroep beoordeelt beide interventies qua kosteneffectiviteit dan ook gelijk aan elkaar.
De werkgroep verwacht dat economische overwegingen vanuit de patiënt geen invloed hebben op de keuze voor de pijnintensiteit. Wel verwacht de werkgroep dat het laten aansluiten van de pijnintensiteit op de voorkeuren en wensen van de patiënt de effecten van therapie mogelijk vergroot (door o.a. hogere motivatie en therapietrouw), wat een positief effect kan hebben op het voorkomen van invasieve behandelingen, het verlagen van zorggebruik en daarmee het beperken van zorgkosten.
Gelijkheid
De werkgroep verwacht dat het aanbieden van pijnvrije looptraining naast niet-pijnvrije looptraining zal leiden tot een mogelijke toename van de gezondheidsgelijkheid.
Uit de knelpuntenanalyse onder therapeuten en uit de literatuur komt naar voren dat men bezorgd is dat het toepassen van samen beslissen (zoals het aanbieden van pijnvrije naast niet-pijnvrije looptraining) een risico vormt voor de gezondheidsgelijkheid, door de gedachte dat samen beslissen meer waardevol is voor hoger opgeleide personen, die beter in staat zijn om op te komen voor hun behoeften en een hoger niveau van gezondheidsvaardigheden hebben (Coulter, 2011; Legare, 2008). Een systematic review van Durand et al. laat echter zien dat samen beslissen juist leidt tot een toename van gezondheidsgelijkheid, mits de informatievoorziening wordt aangepast aan de behoeften van de individuele patiënt (Durand, 2014).
De werkgroep beoordeelt dat het aanbieden van pijnvrije looptraining als alternatief voor niet-pijnvrije looptraining zorgt voor een betere aansluiting van de zorg op de wensen, voorkeuren en mogelijkheden van de individuele patiënt met sPAV en daarmee zorgt voor een betere aansluiting van de zorg op een grotere groep patiënten (inclusieve zorg).
Aanvaardbaarheid
De werkgroep verwacht dat het aanbieden van zowel pijnvrije als niet-pijnvrije looptraining door alle belangrijke stakeholders zal worden geaccepteerd.
Haalbaarheid
De implementatie van het aanbieden van zowel pijnvrije als niet-pijnvrije looptraining wordt door de werkgroep als realistisch beoordeeld. De norm is dat een beweeginterventie wordt aangeboden waarin altijd een bepaalde mate van supervisie door een fysio-/oefentherapeut aanwezig is. Hierbij kan in samenspraak met de patiënt worden bepaald, afhankelijk van de individuele wensen en doelen, welke mate van pijn wordt aangehouden tijdens het trainen. De werkgroep voorziet mogelijk gunstige effecten in de praktijk bij het aanbieden van pijnvrije looptraining (mits van toepassing op de individuele patiënt), omdat het advies aan de patiënt vereenvoudigd kan worden (enkel het aanmoedigen van meer loop- of beweegactiviteit, in plaats van het aanmoedigen van meer loopactiviteit met pijnklachten).
Het aanbieden van pijnvrije looptraining kan betekenen dat therapeuten, patiënten of andere stakeholders, zoals huisartsen en vaatchirurgen, gewoontes moeten doorbreken waarin niet-pijnvrije looptraining als enige mogelijke trainingsvorm wordt gezien.
Eventuele additionele overwegingen
De werkgroep is van mening dat de volgende overwegingen ook van belang zijn bij het aanbieden van pijnvrije en niet-pijnvrije looptraining:
- Het is van belang dat de therapeut altijd samen met de patiënt de voortgang van de behandeling evalueert (door inzet van gestandaardiseerde meetinstrumenten (opent in nieuw tabblad)).
- Bij patiënten met sPAV kunnen comorbiditeiten of niet-sPAV gerelateerde pijnklachten aanwezig zijn die een beperking opleveren bij het fysiek functioneren of de trainbaarheid. Het is van belang dat de therapeut bij het aanbieden van (loop)training en het bespreken van de pijnintensiteit op het gebied van claudicatioklachten, ook rekening houdt met niet sPAV-gerelateerde pijn die een patiënt mogelijk ervaart (denk aan nociplastische pijn, of pijnklachten door comorbiditeiten als knie- of heupartrose).
- Bij het aanbieden van zowel pijnvrije als niet-pijnvrije looptraining blijft een belangrijke rol weggelegd voor de therapeut om coping, ziekte-inzicht, leefstijl en zelfmanagement van de patiënt te bevorderen. Ook wanneer wordt gekozen voor pijnvrije looptraining is het bijvoorbeeld belangrijk dat een patiënt alsnog inziet en ervaart dat doorlopen met claudicatioklachten niet schadelijk is voor het lichaam.
- De werkgroep raadt aan dat therapeut en patiënt bij het kiezen van de in te zetten pijnintensiteit rekening houden met onder andere de individuele doelen en arbeidsomstandigheden van de patiënt, en de bijbehorende specificiteit van de training. De gekozen trainingsintensiteit moet kunnen zorgen voor de benodigde trainingsprikkel waarmee de patiënt ook daadwerkelijk progressie kan boeken.
- Het is van belang dat patiënten positieve ervaringen opdoen met beweging. Training of beweging moet niet met tegenzin worden uitgevoerd; het streven moet zijn dat de ervaringen van patiënten met het bewegen de verwachtingen overtreffen, om zo optimale resultaten te behalen. Daarbij kan het van meerwaarde zijn om pijnvrije (loop)training aan te bieden naast niet-pijnvrije (loop)training.
- De pijnintensiteit kan altijd heroverwogen worden gedurende het behandeltraject, dit kan bijvoorbeeld afhankelijk zijn van de voortgang van de behandeling of van de voorkeuren en wensen van de patiënt.
Kennislacunes
- Vanwege de heterogeniteit in de geselecteerde literatuur en vanwege de beperkt beschikbare literatuur is geen gestandaardiseerd resultaat geformuleerd conform de GRADE-methodiek. Om gericht een uitspraak te kunnen doen over de effectiviteit van pijnvrije looptraining ten opzichte van niet-pijnvrije looptraining dienen meer studies uitgevoerd te worden bij patiënten met sPAV, waarbij pijnvrij trainen wordt vergeleken met niet-pijnvrij trainen, op uitkomstmaten zoals fysiek functioneren, kwaliteit van leven, mate van pijn, levensverwachting en arbeidsparticipatie.
Aboyans, V., Ricco, J. B., Bartelink, M. E. L., Bjorck, M., Brodmann, M., Cohnert, T., Collet, J. P., Czerny, M., De Carlo, M., Debus, S., Espinola-Klein, C., Kahan, T., Kownator, S., Mazzolai, L., Naylor, A. R., Roffi, M., Rother, J., Sprynger, M., Tendera, M., et al. (2018). 2017 ESC Guidelines on the Diagnosis and Treatment of Peripheral Arterial Diseases, in collaboration with the European Society for Vascular Surgery (ESVS): Document covering atherosclerotic disease of extracranial carotid and vertebral, mesenteric, renal, upper and lower extremity arteriesEndorsed by: the European Stroke Organization (ESO)The Task Force for the Diagnosis and Treatment of Peripheral Arterial Diseases of the European Society of Cardiology (ESC) and of the European Society for Vascular Surgery (ESVS). Eur Heart J, 39(9), 763-816. https://doi.org/10.1093/eurheartj/ehx095
Bae, E., Choi, S. E., Lee, H., Shin, G.& Kang, D. (2020). Validity of EQ-5D utility index and minimal clinically important difference estimation among patients with chronic obstructive pulmonary disease. BMC Pulm Med, 20(1), 73. https://doi.org/10.1186/s12890-020-1116-z
Bartelink, M. E. L., Elsman, B. H. P., Oostindjer, A., Stoffers, H. E. J. H., Wiersma, T. J.& Geraets, J. J. X. R. (2014). NHG-Standaard Perifeer arterieel vaatlijden. Huisarts Wet, 57(2), 81-81.
Conijn, A. P., Jonkers, W., Rouwet, E. V., Vahl, A. C., Reekers, J. A.& Koelemay, M. J. (2015). Introducing the Concept of the Minimally Important Difference to Determine a Clinically Relevant Change on Patient-Reported Outcome Measures in Patients with Intermittent Claudication. Cardiovasc Intervent Radiol, 38(5), 1112-1118. https://doi.org/10.1007/s00270-015-1060-0
Coulter, A., Collins, A.& King’s Fund, C. (2011). Making shared decision-making a reality : no decision about me, without me. King’s Fund.
Daley, A. M., IW. (2003). Preferred exercise mode and affective responses in physically active adults. Psychology of Sport and Exercise, 4(4), 347-356.
Durand, M. A., Carpenter, L., Dolan, H., Bravo, P., Mann, M., Bunn, F.& Elwyn, G. (2014). Do interventions designed to support shared decision-making reduce health inequalities? A systematic review and meta-analysis. PLoS One, 9(4), e94670. https://doi.org/10.1371/journal.pone.0094670
Elwyn, G., Durand, M. A., Song, J., Aarts, J., Barr, P. J., Berger, Z., Cochran, N., Frosch, D., Galasinski, D., Gulbrandsen, P., Han, P. K. J., Harter, M., Kinnersley, P., Lloyd, A., Mishra, M., Perestelo-Perez, L., Scholl, I., Tomori, K., Trevena, L., et al. (2017). A three-talk model for shared decision making: multistage consultation process. BMJ, 359, j4891. https://doi.org/10.1136/bmj.j4891
Fakhry, F., van de Luijtgaarden, K. M., Bax, L., den Hoed, P. T., Hunink, M. G., Rouwet, E. V.& Spronk, S. (2012). Supervised walking therapy in patients with intermittent claudication. J Vasc Surg, 56(4), 1132-1142. https://doi.org/10.1016/j.jvs.2012.04.046
Farrar, J. T., Young, J. P., Jr., LaMoreaux, L., Werth, J. L.& Poole, M. R. (2001). Clinical importance of changes in chronic pain intensity measured on an 11-point numerical pain rating scale. Pain, 94(2), 149-158. https://doi.org/10.1016/S0304-3959(01)00349-9
Fokkenrood, H. J., Scheltinga, M. R., Koelemay, M. J., Breek, J. C., Hasaart, F., Vahl, A. C.& Teijink, J. A. (2014). Significant savings with a stepped care model for treatment of patients with intermittent claudication. Eur J Vasc Endovasc Surg, 48(4), 423-429. https://doi.org/10.1016/j.ejvs.2014.04.020
Gerhard-Herman, M. D., Gornik, H. L., Barrett, C., Barshes, N. R., Corriere, M. A., Drachman, D. E., Fleisher, L. A., Fowkes, F. G., Hamburg, N. M., Kinlay, S., Lookstein, R., Misra, S., Mureebe, L., Olin, J. W., Patel, R. A., Regensteiner, J. G., Schanzer, A., Shishehbor, M. H., Stewart, K. J., et al. (2017). 2016 AHA/ACC Guideline on the Management of Patients With Lower Extremity Peripheral Artery Disease: Executive Summary: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. Circulation, 135(12), e686-e725. https://doi.org/10.1161/CIR.0000000000000470
Gommans, L. N., Fokkenrood, H. J., van Dalen, H. C., Scheltinga, M. R., Teijink, J. A.& Peters, R. J. (2015). Safety of supervised exercise therapy in patients with intermittent claudication. J Vasc Surg, 61(2), 512-518 e512. https://doi.org/10.1016/j.jvs.2014.08.070
Gommans, L. N., Saarloos, R., Scheltinga, M. R., Houterman, S., de Bie, R. A., Fokkenrood, H. J.& Teijink, J. A. (2014). Editor’s choice–The effect of supervision on walking distance in patients with intermittent claudication: a meta-analysis. Eur J Vasc Endovasc Surg, 48(2), 169-184. https://doi.org/10.1016/j.ejvs.2014.04.019
Higgins, J. P., Savović, J., Page, M. J., Elbers, R. G.& Sterne, J. A. (2019). Assessing risk of bias in a randomized trial. Cochrane handbook for systematic reviews of interventions, 205-228.
Langendam, M. K., T. . (2022). Toepassen GRADE voor interventies tool. https://nl.gradeworkinggroup.org/docs/Tool_GRADE_voor_interventies_juni2022_final.pdf
Legare, F., Ratte, S., Gravel, K.& Graham, I. D. (2008). Barriers and facilitators to implementing shared decision-making in clinical practice: update of a systematic review of health professionals’ perceptions. Patient Educ Couns, 73(3), 526-535. https://doi.org/10.1016/j.pec.2008.07.018
Lin, E., Nguyen, C. H.& Thomas, S. G. (2019). Completion and adherence rates to exercise interventions in intermittent claudication: Traditional exercise versus alternative exercise – a systematic review. Eur J Prev Cardiol, 26(15), 1625-1633. https://doi.org/10.1177/2047487319846997
McDermott, M. M., Spring, B., Tian, L., Treat-Jacobson, D., Ferrucci, L., Lloyd-Jones, D., Zhao, L., Polonsky, T., Kibbe, M. R., Bazzano, L., Guralnik, J. M., Forman, D. E., Rego, A., Zhang, D., Domanchuk, K., Leeuwenburgh, C., Sufit, R., Smith, B., Manini, T., et al. (2021a). Effect of Low-Intensity vs High-Intensity Home-Based Walking Exercise on Walk Distance in Patients With Peripheral Artery Disease: The LITE Randomized Clinical Trial. JAMA, 325(13), 1266-1276. https://doi.org/10.1001/jama.2021.2536
McDermott, M. M., Tian, L., Criqui, M. H., Ferrucci, L., Conte, M. S., Zhao, L., Li, L., Sufit, R., Polonsky, T. S., Kibbe, M. R., Greenland, P., Leeuwenburgh, C.& Guralnik, J. M. (2021b). Meaningful change in 6-minute walk in people with peripheral artery disease. J Vasc Surg, 73(1), 267-276 e261. https://doi.org/10.1016/j.jvs.2020.03.052
Merry, A. H. H., Teijink, J. A. W., Jongert, M. W. A., Poelgeest, A., Van Der Voort, S. S. E. M., Bartelink, M. E. L., Stoffers, H. E. J. H., Brooymans, F., Hendriks, H. J. M.& De Bie, R. A. (2014). KNGF-richtlijn Symptomatisch perifeer arterieel vaatlijden. www.kngfrichtlijnen.nl.
Mika, P., Konik, A., Januszek, R., Petriczek, T., Mika, A., Nowobilski, R., Nizankowski, R.& Szczeklik, A. (2013). Comparison of two treadmill training programs on walking ability and endothelial function in intermittent claudication. Int J Cardiol, 168(2), 838-842. https://doi.org/10.1016/j.ijcard.2012.10.003
Nordanstig, J., Pettersson, M., Morgan, M., Falkenberg, M.& Kumlien, C. (2017). Assessment of Minimum Important Difference and Substantial Clinical Benefit with the Vascular Quality of Life Questionnaire-6 when Evaluating Revascularisation Procedures in Peripheral Arterial Disease. Eur J Vasc Endovasc Surg, 54(3), 340-347. https://doi.org/10.1016/j.ejvs.2017.06.022
Novaković, M., Krevel, B., Rajkovic, U., Vizintin Cuderman, T., Jansa Trontelj, K., Fras, Z.& Jug, B. (2019). Moderate-pain versus pain-free exercise, walking capacity, and cardiovascular health in patients with peripheral artery disease. J Vasc Surg, 70(1), 148-156. https://doi.org/10.1016/j.jvs.2018.10.109
Parfitt, G. G., C. (2004). The effect of choice of exercise mode on psychological responses. Psychology of Sport and Exercise, 5(2), 111-117.
Society for Vascular Surgery Lower Extremity Guidelines Writing, G., Conte, M. S., Pomposelli, F. B., Clair, D. G., Geraghty, P. J., McKinsey, J. F., Mills, J. L., Moneta, G. L., Murad, M. H., Powell, R. J., Reed, A. B., Schanzer, A., Sidawy, A. N.& Society for Vascular, S. (2015). Society for Vascular Surgery practice guidelines for atherosclerotic occlusive disease of the lower extremities: management of asymptomatic disease and claudication. J Vasc Surg, 61(3 Suppl), 2S-41S. https://doi.org/10.1016/j.jvs.2014.12.009
Stiggelbout, A. M., Pieterse, A. H.& De Haes, J. C. (2015). Shared decision making: Concepts, evidence, and practice. Patient Educ Couns, 98(10), 1172-1179. https://doi.org/10.1016/j.pec.2015.06.022
van Asselt, A. D., Nicolai, S. P., Joore, M. A., Prins, M. H., Teijink, J. A.& Exercise Therapy in Peripheral Arterial Disease Study, G. (2011). Cost-effectiveness of exercise therapy in patients with intermittent claudication: supervised exercise therapy versus a ‘go home and walk’ advice. Eur J Vasc Endovasc Surg, 41(1), 97-103. https://doi.org/10.1016/j.ejvs.2010.06.024
van den Houten, M. M., Gommans, L. N., van der Wees, P. J.& Teijink, J. A. (2016a). Minimally Important Difference of the Absolute and Functional Claudication Distance in Patients with Intermittent Claudication. Eur J Vasc Endovasc Surg, 51(3), 404-409. https://doi.org/10.1016/j.ejvs.2015.11.008
van den Houten, M. M., Lauret, G. J., Fakhry, F., Fokkenrood, H. J., van Asselt, A. D., Hunink, M. G.& Teijink, J. A. (2016b). Cost-effectiveness of supervised exercise therapy compared with endovascular revascularization for intermittent claudication. Br J Surg, 103(12), 1616-1625. https://doi.org/10.1002/bjs.10247
van der Horst, D. E. M., Garvelink, M. M., Bos, W. J. W., Stiggelbout, A. M.& Pieterse, A. H. (2023). For which decisions is Shared Decision Making considered appropriate? – A systematic review. Patient Educ Couns, 106, 3-16. https://doi.org/10.1016/j.pec.2022.09.015
Wyrwich, K. W., Tierney, W. M., Babu, A. N., Kroenke, K.& Wolinsky, F. D. (2005). A comparison of clinically important differences in health-related quality of life for patients with chronic lung disease, asthma, or heart disease. Health Serv Res, 40(2), 577-591. A comparison of clinically important differences in health-related quality of life for patients with chronic lung disease, asthma, or heart disease – PubMed
Zatloukal, J., Ward, S., Houchen-Wolloff, L., Harvey-Dunstan, T.& Singh, S. (2019). The minimal important difference for the endurance shuttle walk test in individuals with chronic obstructive pulmonary disease following a course of pulmonary rehabilitation. Chronic Respiratory Disease, 16. https://doi.org/10.1177/1479973119853828
C.8.4 De keuze voor aerobe training en/of krachttraining
Aanbevelingen
- Zet samen beslissen (persoonsgerichte zorg) in om samen met de patiënt een keuze te maken voor aerobe training en/of krachttraining, gericht op het bevorderen van het fysiek functioneren en de kwaliteit van leven, binnen de fysio-/oefentherapeutische behandeling van patiënten met symptomatisch Perifeer Arterieel Vaatlijden (sPAV).
- Volg hierbij de vier stappen van het proces van samen beslissen zoals beschreven in module ‘A.8.2 Achtergrond’ (opent in nieuw tabblad).
o Betrek bij stap twee ‘option talk’:
- de beschikbare wetenschappelijke kennis over aerobe training en krachttraining (zie ‘Toelichting: Conclusies op basis van de literatuur C.8.4’ );
- de klinische expertise van de therapeut met betrekking tot aerobe training en krachttraining;
- de voor- en nadelen van aerobe training of krachttraining (waarin o.a. aandacht is voor de FITT-factoren: Frequentie, Intensiteit, Tijd, en Type van de training);
- de trainingsprincipes (zoals de specificiteit van aerobe training of krachttraining in relatie tot de trainingsdoelen en de mogelijkheid om met aerobe training of krachttraining de minimaal vereiste drempel voor een trainingsprikkel – en vervolgens een trainingseffect – te kunnen bereiken);
- de verwachte uitkomsten van aerobe training en krachttraining (zie ‘Verantwoording: Effectiviteit en bewijskracht C.8.4’ );
- de invloed en de gevolgen van de trainingsvorm op de persoonlijke situatie en mogelijkheden van de patiënt (o.a. comorbiditeit, bewegingsangst en arbeidsomstandigheden).
- Evalueer de voortgang van de behandeling op gezette tijden (zie module C.6 ‘Evaluatie van de behandeling’ (opent in nieuw tabblad)) en zet samen beslissen in om samen met de patiënt te bespreken of de gekozen trainingsvorm nog voldoende op hem is afgestemd.
| Definitie ‘Aerobe training’ Alle vormen van fysieke training of beweging die zich richten op het vergroten van het duuruithoudingsvermogen (opent in nieuw tabblad) .Definitie ‘Krachttraining’ Alle vormen van fysieke training of beweging die zich richten op het vergroten van de maximale kracht, snelkracht, explosieve kracht of het krachtuithoudingsvermogen. |
Beschrijving
Uit de bevindingen van de beschikbare wetenschappelijke literatuur kan niet worden geconcludeerd dat krachttraining beter of slechter is voor het fysiek functioneren en de kwaliteit van leven dan aerobe training. Kortom, we zijn zeer onzeker of de ene vorm van training effectiever is dan de andere. Uit de voorkeuren van patiënten, de klinische expertise van therapeuten, en de voor- en nadelen van de interventies blijkt dat zowel krachttraining als aerobe training als relevante behandelopties wordt beschouwd. In deze module wordt hierdoor geen aanbeveling gegeven voor één specifieke behandeloptie, maar wordt het toepassen van samen beslissen om te komen tot een keuze voor een trainingsvorm, nog belangrijker om het fysiek functioneren en de kwaliteit van leven te bevorderen binnen de fysio-/oefentherapeutische behandeling van patiënten met sPAV.
Aanleiding
Conform (inter)nationale richtlijnen is gesuperviseerde beweegtraining of looptraining de primair aanbevolen behandeling voor patiënten met symptomatisch Perifeer Arterieel Vaatlijden (sPAV) (Aboyans, 2018; Bartelink, 2014; Merry, 2014; Society for Vascular Surgery Lower Extremity Guidelines Writing, 2015). Desalniettemin zijn voor het vormgeven van het fysio-/ oefentherapeutische behandelplan verschillende vormen en doseringen van beweeg- of looptraining mogelijk (Merry, 2014). Het behandelplan omvat daarmee meerdere beslissingen waarbij ruimte is voor samen beslissen. Dit is bij uitstek het geval bij beslissingen waarbij meerdere redelijke opties bestaan en de uiteindelijke keuze afhangt van de persoonlijke voorkeuren en waarden van de patiënt, of bij beslissingen waarbij de betrokkenheid en toewijding van de patiënt cruciaal zijn voor de uitvoering van de behandeling, zoals bij leefstijlkeuzes (van der Horst, 2023).
Uit de knelpuntenanalyse (gericht op samen beslissen) blijkt dat therapeuten vaak het gevoel hebben dat gesuperviseerde pijninducerende looptraining de primair in te zetten interventie moet zijn. Voor veel therapeuten is het onvoldoende duidelijk wat de voor- en nadelen van de verschillende mogelijke behandelopties zijn binnen de behandeling van patiënten met sPAV. Dit terwijl inzicht hebben in de beschikbare wetenschappelijke evidentie, en daarmee in de waarde van de verschillende behandelopties, juist van belang is voor het effectief toepassen van samen beslissen. Het aanbieden van deze kennis, naast de kennis uit de KNGF-richtlijn sPAV uit 2014 , kan fysio-/oefentherapeuten ondersteunen tijdens het samen beslissen, en helpen om patiënten met sPAV goed te laten participeren tijdens het proces van samen beslissen. Dit is vooral waardevol tijdens de option talk. Option talk, oftewel het optiegesprek, is een van de essentiële stappen in het proces van samen beslissen en omvat het informeren van de patiënt over de mogelijke behandelopties, inclusief bijbehorende voor- en nadelen, op basis van de beschikbare (of soms beperkte) wetenschappelijke kennis en klinische expertise (Elwyn, 2017; Stiggelbout, 2015).
Binnen deze module C.8.4 wordt ingegaan op de waarde van krachttraining ten opzichte van aerobe training bij patiënten met sPAV. Binnen (inter)nationale richtlijnen is de primair aanbevolen interventie voor patiënten met sPAV een gesuperviseerde beweeginterventie die hoofdzakelijk bestaat uit aerobe training, zoals looptraining (Aboyans, 2018; Bartelink, 2014; Gerhard-Herman, 2017; Society for Vascular Surgery Lower Extremity Guidelines Writing, 2015). Uit de knelpuntenanalyse blijkt dat het voor therapeuten onduidelijk is wat de waarde is van krachttraining en in welke gevallen die een relevante behandeloptie is om aan te bieden naast, of in plaats van, aerobe training. In de praktijk wordt vaak primair de keuze gemaakt voor aerobe training. Echter, soms sluit aerobe training niet goed aan bij de mogelijkheden en de hulpvraag van en/of de gewenste uitkomsten voor patiënten.
Om therapeuten inzicht te geven in de beschikbare wetenschappelijke evidentie is het van belang om aanbevelingen te formuleren voor de gewenste en ongewenste effecten van krachttraining ten opzichte van aerobe training bij patiënten met sPAV. Hiertoe is de volgende uitgangsvraag geformuleerd:
Uitgangsvraag
Kan in plaats van aerobe training ook gekozen worden voor krachttraining bij patiënten met sPAV?
Conclusies op basis van de literatuur
Op basis van de conclusies van de geselecteerde literatuur kunnen een aantal resultaten worden geformuleerd. Deze ‘Gestandaardiseerde formuleringen van de resultaten’ worden gevormd door de grootte van het effect en de bewijskracht te combineren en ze doen een uitspraak over de zekerheid van het bewijs dat in de literatuur is gevonden (Langendam, 2022).
Cruciale uitkomstmaten:
- Het wetenschappelijke bewijs is zeer onzeker over het effect van krachttraining op fysiek functioneren (gemeten als de totale loopafstand met de zes minuten wandeltest (6MWT), en de functionele en maximale loopafstand met de loopbandtest) ten opzichte van aerobe training bij patiënten met sPAV.
Toelichting: De geselecteerde gerandomiseerde studies beschrijven dat zowel krachttraining als aerobe training positieve effect heeft op het fysiek functioneren. De bewijskracht van de resultaten was zeer laag, waardoor we zeer onzeker zijn over het effect dat vanuit de literatuur is aangetoond.
- Slechts één geselecteerde studie rapporteerde resultaten over het effect van krachttraining op kwaliteit van leven (gemeten met de SF-36) ten opzichte van aerobe training bij patiënten met sPAV. In dit geval is ervoor gekozen om de resultaten narratief te beschrijven en geen conclusie te formuleren volgens de GRADE-methodiek.
- Er zijn geen studies gevonden die resultaten hebben beschreven op de overige cruciale uitkomstmaten: mate van pijn, levensverwachting en arbeidsparticipatie.
Belangrijke uitkomstmaten:
- Een van de geselecteerde studies beschrijft resultaten over ongewenste effecten gerelateerd aan aerobe training of krachttraining. Deze studie includeerde 180 patiënten en rapporteerde uiteindelijk vier ernstige ongewenste voorvallen waardoor patiënten deelname aan de studie moesten beëindigen (beroerte, hartinfarct of revascularisatie van het been), maar vond geen verschillen in ongewenste effecten tussen de groepen.
Rationale van de aanbeveling
De werkgroep heeft besloten om een sterke aanbeveling voor het toepassen van samen beslissen op te nemen in deze richtlijnmodule. Hierbij waren er een aantal criteria (zie Verantwoording; ‘Van bewijs naar aanbeveling’) die zwaar en minder zwaar hebben gewogen.
Uit de resultaten van het systematische literatuuronderzoek kan niet worden geconcludeerd dat aerobe training beter is voor het fysiek functioneren en de kwaliteit van leven op korte termijn (<1 jaar) dan krachttraining. Tegelijkertijd kan ook niet worden geconcludeerd dat krachttraining beter is voor het fysiek functioneren en de kwaliteit van leven dan aerobe training. Kortom, we zijn zeer onzeker of de ene vorm van training effectiever is dan de andere. Wel suggereren de resultaten dat zowel krachttraining als aerobe training mogelijk een positief effect heeft op fysiek functioneren en kwaliteit van leven. Het besluit van de werkgroep dat hieruit voortkomt, is dat krachttraining mogelijk niet onderdoet voor aerobe training wanneer men kijkt naar de effecten op fysiek functioneren en kwaliteit van leven, en daarmee een goed alternatief kan zijn binnen de fysio-/oefentherapeutische behandeling van patiënten met sPAV.
Een achterbanraadpleging onder patiënten met sPAV laat zien dat er variatie bestaat in de voorkeur en waardering van patiënten ten aanzien van krachttraining of aerobe training. Patiënten hechten veel waarde aan het kunnen kiezen tussen verschillende trainingsvormen.
De werkgroep beoordeelt dat de resultaten van het systematische literatuuronderzoek en de voorkeuren van patiënten laten zien dat voor zowel aerobe training als krachttraining geldt dat de gewenste effecten (positieve effecten op fysiek functioneren en kwaliteit van leven) de ongewenste effecten overtreffen.
De economische overwegingen en kosteneffectiviteit zijn gelijkwaardig voor aerobe training en krachttraining. De werkgroep verwacht dat het aanbieden van krachttraining naast aerobe training kan zorgen voor een toename van de gezondheidsgelijkheid, doordat de aangeboden zorg beter kan worden afgestemd op de individuele patiënt (inclusieve zorg). De overige criteria van het proces van bewijs naar aanbeveling (aanvaardbaarheid en haalbaarheid) worden als niet-bezwaarlijk bevonden in het aanbieden van krachttraining naast aerobe training.
Concluderend is het wetenschappelijke bewijs onzeker over het effect van krachttraining ten opzichte van aerobe training, maar beoordeelt de werkgroep dat de gunstige effecten en de voorkeuren van patiënten overheersend zijn, waardoor er een sterke aanbeveling voor het toepassen van samen beslissen om te komen tot een keuze voor de toe te passen trainingsvorm is geformuleerd.
Literatuur
Zoeken en selecteren
Onderzoeksvraag
- Wat is het effect van krachttraining ten opzichte van aerobe training op het fysiek functioneren, de kwaliteit van leven, de mate van pijn, de levensverwachting en de arbeidsparticipatie bij patiënten met symptomatisch Perifeer Arterieel Vaatlijden (sPAV)?
Relevante uitkomstmaten
De werkgroep achtte het fysiek functioneren, de kwaliteit van leven, de mate van pijn, de levensverwachting en de arbeidsparticipatie cruciale uitkomstmaten voor de besluitvorming. De werkgroep achtte ongewenste effecten gerelateerd aan een van de interventies, belangrijke uitkomstmaten.
Per uitkomstmaat:
- Fysiek functioneren
- Zes minuten wandeltest (6MWT): Uit de wetenschappelijke literatuur blijkt dat een verschil van acht meter als belangrijk effect beschouwd kan worden bij patiënten met PAV (klinisch relevant verschil) (McDermott, 2021). De werkgroep beschouwt* deze waarden ook als klinisch relevant voor patiënten met sPAV.
- Loopbandtest: De werkgroep definieerde*, op basis van de wetenschappelijke literatuur, een verschil van 250 meter (functionele loopafstand) en 305 meter (maximale loopafstand) als belangrijk effect bij patiënten met sPAV (klinisch relevant verschil) (van den Houten, 2016a).
- Shuttle Walk Test (SWT): Uit de wetenschappelijke literatuur blijkt dat een verschil van 174 seconden als belangrijk effect beschouwd kan worden bij patiënten met COPD (klinisch relevant verschil) (Zatloukal, 2019). Omdat wetenschappelijke literatuur over de klinische relevantie bij patiënten met sPAV ontbreekt, beschouwt* de werkgroep deze waarden als voldoende gelijkwaardig en daarmee als ook klinisch relevant voor patiënten met sPAV.
- Walking Impairment Questionnaire (WIQ): De werkgroep definieerde*, op basis van de wetenschappelijke literatuur, een verschil van 0.11 punten (op een schaal van 0 tot 1, waarbij een hogere score correspondeert met een betere mate van fysiek functioneren) als belangrijk effect bij patiënten met sPAV (klinisch relevant verschil) (Conijn, 2015).
- Kwaliteit van leven
- 36-Item Short Form Health Survey (SF-36): Uit de wetenschappelijke literatuur blijkt dat een verschil van 10 punten (physical functioning, bodily pain, general health en mental health), 12.5 punten (physical role, vitality en social functioning) en 8.3 punten (emotional role) als belangrijk effect beschouwd kan worden bij patiënten met COPD (klinisch relevant verschil) (Wyrwich, 2005). De schaal van de SF-36 loopt van 0 tot 100, waarbij een hogere score correspondeert met een betere kwaliteit van leven. Omdat wetenschappelijke literatuur over de klinische relevantie bij patiënten met sPAV ontbreekt, beschouwt* de werkgroep deze waarden als voldoende gelijkwaardig en daarmee als ook klinisch relevant voor patiënten met sPAV.
- Vascular Quality of Life Questionnaire-6 (VascuQol-6): De werkgroep definieerde*, op basis van de wetenschappelijke literatuur, een verschil van 1.7 punten (op een schaal van 6 tot 24, waarbij een hogere score correspondeert met een betere kwaliteit van leven) als belangrijk effect bij patiënten met sPAV (klinisch relevant verschil) (Nordanstig, 2017).
- EuroQol (EQ-5D): Uit de wetenschappelijke literatuur blijkt dat een verschil van 0.028 punten (op een schaal van -1 tot 1, waarbij een hogere score correspondeert met een betere kwaliteit van leven) als belangrijk effect beschouwd kan worden bij patiënten met COPD (klinisch relevant verschil) (Bae, 2020). Omdat wetenschappelijke literatuur over de klinische relevantie bij patiënten met sPAV ontbreekt, beschouwt* de werkgroep deze waarden als voldoende gelijkwaardig en daarmee als ook klinisch relevant voor patiënten met sPAV.
- Mate van pijn
- Numerical pain rating scale (NPRS): Uit de wetenschappelijke literatuur blijkt dat een verschil van 2 punten (op een schaal van 0 tot 10, waarbij een hogere score correspondeert met een hogere mate van pijn) als belangrijk effect beschouwd kan worden bij patiënten met chronische pijn (klinisch relevant verschil) (Farrar, 2001). Omdat wetenschappelijke literatuur over de klinische relevantie bij patiënten met sPAV ontbreekt, beschouwt* de werkgroep deze waarden als voldoende gelijkwaardig en daarmee als ook klinisch relevant voor patiënten met sPAV.
- Levensverwachting
- Mortaliteit: De werkgroep definieerde* een verschil van 1 op 100 personen als belangrijk effect bij patiënten met sPAV (klinisch relevant verschil).
- Arbeidsparticipatie
- Voor het meten van de arbeidsparticipatie is op voorhand geen meetinstrument met bijbehorende grenzen van klinische relevantie vastgesteld.
- Ongewenste effecten
- Major Adverse Events (ernstige ongewenste voorvallen): De werkgroep definieerde* een verschil van 1 op 50 personen als belangrijk effect bij patiënten met sPAV (klinisch relevant verschil).
- Ziekenhuisopnames: De werkgroep definieerde* een verschil van 1 op 50 personen als belangrijk effect bij patiënten met sPAV (klinisch relevant verschil).
*De werkgroep benadrukt dat het per individu kan verschillen of een effect wel of niet als klinisch relevant wordt beschouwd. Dit kan bijvoorbeeld afhankelijk zijn van de individuele hulpvraag en/of therapiedoelen. Desondanks zijn voor de start van het literatuuronderzoek bovenstaande specifieke grenzen voor klinische relevantie vastgesteld. De genoemde meetinstrumenten met bijbehorende criteria dienen als leidraad voor deze richtlijnmodule, met ruimte voor aanpassingen op basis van individuele patiëntbehoeften. De meetinstrumenten (opent in nieuw tabblad)genoemd in de generieke KNGF-richtlijn sPAV blijven de basis vormen voor diagnostiek en evaluatie.
Zoekactie
Op 17 augustus 2023 is door L. Marcellis (met ondersteuning van informatiespecialist A. Tillema) een systematische zoekactie uitgevoerd in MEDLINE, Embase, Cinahl en Cochrane (zie bijlage C.8.4-1 (opent in nieuw tabblad)voor de zoekverantwoording). De systematische zoekactie leverde 4.602 unieke treffers op. Na screening (door D. Conijn (DC), L. Marcellis (LM), M. Simon (MS) en T. Hoogeboom (TH)) van de titel en het abstract op de inclusiecriteria en exclusiecriteria (zie tabel 1) zijn 4.451 artikelen geëxcludeerd. Gekozen werd om artikelen van voor 2005 te excluderen omdat er een duidelijke toename zichtbaar was van het aantal publicaties in 2005. Artikelen waarvan het op basis van titel en abstract niet duidelijk was of deze voldeden aan de inclusiecriteria, werden dubbel gescreend door LM en vervolgens onderling besproken. Van 148 studies is het volledige artikel gescreend door LM, waarbij twijfelgevallen dubbel werden gescreend door DC en vervolgens onderling werden besproken. Uiteindelijk leverde de zoekactie negentien studies (gerapporteerd in 22 artikelen) op voor modules C.8.1, C.8.2, C.8.3 en C.8.4.
Voor module C.8.4 werden vier studies (gerapporteerd in 5 artikelen) geselecteerd (Gardner, 2014; Meneses, 2011; Ritti-Dias, 2010; Szymczak, 2016; Van Schaardenburgh, 2017). Zie bijlage C.8.4-2 (opent in nieuw tabblad)voor het stroomdiagram van het inclusieproces. De artikelen die op basis van de volledige tekst zijn geëxcludeerd en de reden van exclusie, zijn weergegeven in bijlage C.8.4-3 (opent in nieuw tabblad).
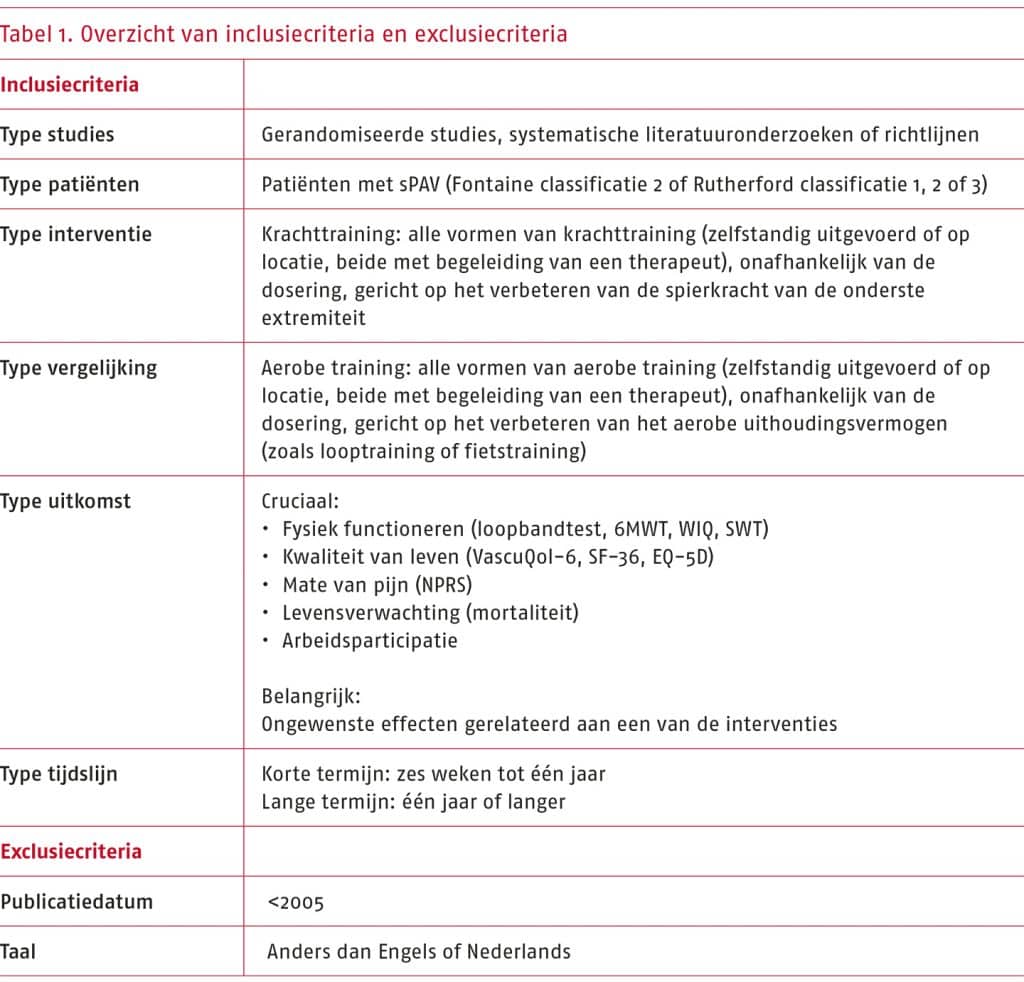
Karakteristieken van geïncludeerde studies
De kenmerken van de geïncludeerde studies zijn weergegeven in bijlage C.8.4-4 (opent in nieuw tabblad). De vier ingesloten studies includeerden in totaal 293 patiënten met sPAV.
De RCT van Van Schaardenburgh et al. beschrijft 29 patiënten met sPAV (Van Schaardenburgh, 2017). De studie werd uitgevoerd in Noorwegen. Patiënten in de interventiegroep (n=14, leeftijd 66 ± 9.3 jaar, 50% vrouw) voerden krachttraining uit in de vorm van de calf raise oefening. De oefening werd herhaald tot pijn optrad in de kuitmusculatuur. Patiënten trainden drie keer per dag gedurende acht weken. Patiënten in de controlegroep (n=15, leeftijd 70 ± 8.2 jaar, 46% vrouw) voerden looptraining tot de pijngrens uit. Patiënten trainden drie keer per week gedurende acht weken. Beide groepen trainden niet-gesuperviseerd en droegen een activiteitenmeter tijdens de training.
De RCT van Szymczak et al. beschrijft 50 patiënten met sPAV (Szymczak, 2016). De studie werd uitgevoerd in Polen. De leeftijd van de patiënten varieerde van 52 tot 75 jaar en het percentage vrouwen was 54%. Patiënten in de interventiegroep (n=26) voerden krachttraining uit bestaande uit zittende oefeningen gericht op de spieren van de onderste extremiteit (3x 15 herhalingen voor elke oefening). Patiënten in de controlegroep (n=24) voerden looptraining uit op een loopband op constante snelheid. Patiënten hielden een rustpauze bij optreden van lichte claudicatioklachten. Beide groepen trainden gesuperviseerd, twee keer per week gedurende twaalf weken.
De RCT van Gardner et al. beschrijft 180 patiënten met sPAV (Gardner, 2014). De studie werd uitgevoerd in de Verenigde Staten. Patiënten in de interventiegroep (n=60, leeftijd 65 ± 9 jaar, 40% vrouw) voerden gesuperviseerde krachttraining uit met lichte weerstand met behulp van krachtapparatuur. Patiënten trainden met een weerstand die na vijftien herhalingen vermoeidheid veroorzaakte (15-rep maximum). De training bestond uit oefeningen voor zowel de bovenste als de onderste extremiteit (1x 15 herhalingen voor iedere oefening). De controlegroep was verdeeld in twee verschillende aerobe interventies. Patiënten in de eerste controlegroep (n=60, leeftijd 65 ± 11 jaar, 52% vrouw) voerden gesuperviseerde looptraining uit op een loopband (snelheid: 3.2 km/h). Patiënten hielden een rustpauze bij optreden van lichte tot matige claudicatioklachten. Patiënten in de tweede controlegroep (n=60, leeftijd 67 ± 10 jaar, 48% vrouw) voerden niet-gesuperviseerde looptraining uit op een zelfgekozen snelheid. Patiënten hielden een rustpauze bij optreden van lichte tot matige claudicatioklachten en kregen viermaal feedback gedurende de trainingsperiode. Alle groepen trainden drie keer per week gedurende twaalf weken en droegen een activiteitenmeter tijdens de training.
De RCT van Ritti-Diaz et al. beschrijft 34 patiënten met sPAV (Meneses, 2011; Ritti-Dias, 2010). De studie werd uitgevoerd in Brazilië. Patiënten in de interventiegroep (n=17, leeftijd 65.7 ± 9.5 jaar, 26.7% vrouw) voerden gesuperviseerde krachttraining uit met behulp van krachtapparatuur. Patiënten trainden met een weerstand die een vermoeidheid van graad 11 tot 13 op een 15-puntsschaal veroorzaakte. De training bestond uit oefeningen voor zowel de bovenste als de onderste extremiteit (3x 10 herhalingen voor iedere oefening). Patiënten in de controlegroep (n=17, leeftijd 64.5 ± 8.8 jaar, 40% vrouw) voerden looptraining uit op een loopband (15x 2 min). Patiënten trainden op een snelheid die een vermoeidheid veroorzaakte van graad 11 tot 13 op een 15-puntsschaal en zorgde voor claudicatioklachten in de laatste 30 seconden van iedere oefenronde. Beide groepen trainden gesuperviseerd, 60 minuten, twee keer per week gedurende twaalf weken.
Individuele studiekwaliteit (RoB)
Het risico op vertekening (risk of bias, RoB) van de gerandomiseerde studies is dubbel gescoord door LM en DC, LM en TH of LM en MS met behulp van de Cochrane Risk-of-Bias-2 tool (Higgins, 2019). Inconsistentie in het oordeel op de verschillende items is onderling besproken (LM en DC, LM en TH of LM en MS), waarna consensus is bereikt. Een overzicht van de beoordeling van de studiekwaliteit (RoB) per studie is weergegeven in bijlage C.8.4-5 (opent in nieuw tabblad) Risk-of-bias-tabel.
Effectiviteit en bewijskracht
Zie de Toelichting voor de conclusies op basis van de literatuur. Hieronder volgt een beschrijving van de effectiviteit en de bewijskracht voor de vergelijking(en).
Krachttraining versus aerobe training
Het effect van krachttraining vergeleken met aerobe training bij patiënten met sPAV is beschreven in vier studies (Gardner, 2014; Meneses, 2011; Ritti-Dias, 2010; Szymczak, 2016; Van Schaardenburgh, 2017). Een overzicht van de resultaten wordt weergegeven in tabel 2. Zie bijlage C.8.4-6 (opent in nieuw tabblad)voor de forest plots van de uitkomsten op fysiek functioneren (totale loopafstand gemeten met de 6MWT, en functionele loopafstand en maximale loopafstand gemeten met de loopbandtest). Hieronder worden de effectiviteit en bewijskracht per uitkomstmaat beschreven.
Eén geselecteerde studie heeft het effect op kwaliteit van leven (SF-36) gemeten en gerapporteerd (Van Schaardenburgh, 2017). In dit geval is ervoor gekozen om de resultaten narratief te beschrijven en de studie niet te includeren in een meta-analyse. Van één studie konden de resultaten op fysiek functioneren niet worden geïncludeerd in de meta-analyse vanwege niet-normaal verdeelde data (Szymczak, 2016). Omdat de resultaten door deze niet-normale verdeling niet goed vergelijkbaar zijn met andere studies, is ervoor gekozen om de resultaten narratief te beschrijven en ook deze studie niet te includeren in een meta-analyse.
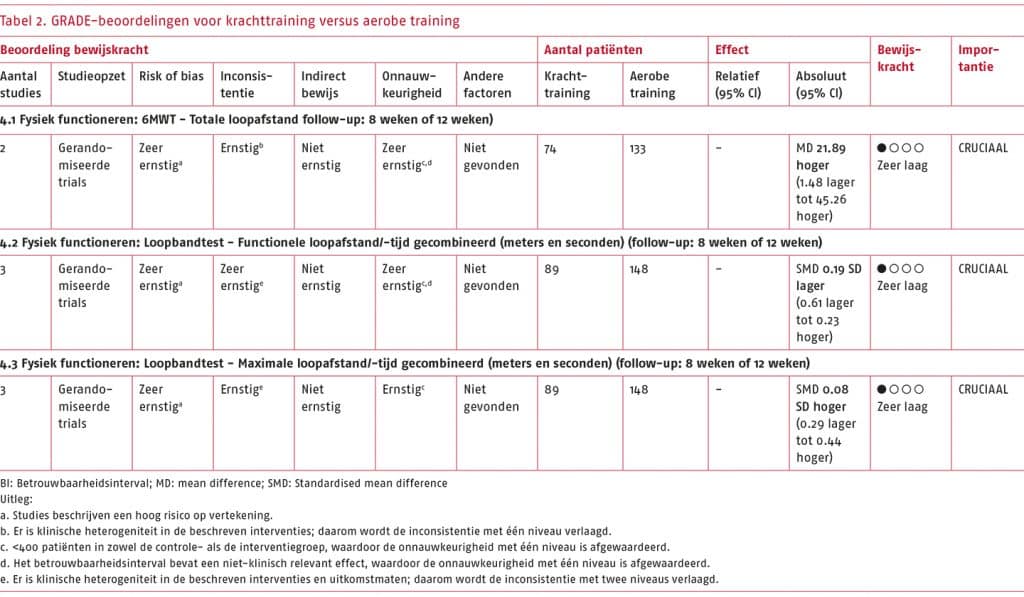
Vergelijking 1. Fysiek functioneren – 6MWT totale loopafstand (follow-up: 8 of 12 weken)
In twee studies is de effectiviteit van krachttraining vergeleken met aerobe training (looptraining) op fysiek functioneren, gemeten als totale loopafstand met de 6MWT (Gardner, 2014; Van Schaardenburgh, 2017). Het gemiddelde verschil (MD) tussen de groepen was 21.89 meter (95%-BI -1.48 tot 45.26; p=0.07, n=74 krachttraininggroep en n=133 aerobe-traininggroep) in het voordeel van de krachttraining. Dit effect wordt door de werkgroep als een niet-significant en klinisch relevant effect beschouwd (McDermott, 2021).
De bewijskracht is met vijf niveaus verlaagd tot zeer laag, gezien het risico op vertekening door de individuele studiekwaliteit (-2 niveaus), door de gevonden inconsistentie (-1 niveau) en door de gevonden onnauwkeurigheid (-2 niveaus).
Vergelijking 2. Fysiek functioneren – Loopbandtest functionele loopafstand (follow-up: 8 of 12 weken)
In drie studies is de effectiviteit van krachttraining vergeleken met aerobe training (looptraining) op fysiek functioneren, gemeten als functionele loopafstand met de loopbandtest (Gardner, 2014; Ritti-Dias, 2010; Van Schaardenburgh, 2017). Het gestandaardiseerde gemiddelde verschil (SMD) tussen de groepen was 0.19 SD (95%-BI -0.61 tot 0.23; p=0.38, n=89 krachttraininggroep en n=148 aerobe-traininggroep) in het voordeel van de aerobe training. Dit effect wordt door de werkgroep als een niet-significant en niet-klinisch relevant effect beschouwd (Sawilowsky, 2009).
De bewijskracht is met zes niveaus verlaagd tot zeer laag, gezien het risico op vertekening door de individuele studiekwaliteit (-2 niveaus), door de gevonden inconsistentie (-2 niveaus) en door de gevonden onnauwkeurigheid (-2 niveaus).
Vergelijking 3. Fysiek functioneren – Loopbandtest maximale loopafstand (follow-up: 8 of 12 weken)
In drie studies is de effectiviteit van krachttraining vergeleken met aerobe training (looptraining) op fysiek functioneren, gemeten als maximale loopafstand met de loopbandtest (Gardner, 2014; Ritti-Dias, 2010; Van Schaardenburgh, 2017). Het gestandaardiseerde gemiddelde verschil (SMD) tussen de groepen was 0.08 SD (95%-BI -0.29 tot 0.44; p=0.68, n=89 krachttraininggroep en n=148 aerobe-traininggroep) in het voordeel van de krachttraining. Dit effect wordt door de werkgroep als een niet-significant en niet-klinisch relevant effect beschouwd (Sawilowsky, 2009).
De bewijskracht is met vier niveaus verlaagd tot zeer laag, gezien het risico op vertekening door de individuele studiekwaliteit (-2 niveaus), door de gevonden inconsistentie (-1 niveau) en door de gevonden onnauwkeurigheid (-1 niveau).
Overige cruciale uitkomstmaten
Er zijn geen studies gevonden die resultaten hebben beschreven op de overige cruciale uitkomstmaten: mate van pijn, levensverwachting en arbeidsparticipatie.
Ongewenste effecten
Eén studie beschreef resultaten op ongewenste effecten (Gardner, 2014). Deze studie van Gardner et al. rapporteerde veertien ongewenste voorvallen gedurende de studie. Vier patiënten (twee in krachttraininggroep en twee in aerobe-traininggroep) moesten deelname aan de studie beëindigen vanwege een ongewenst voorval (beroerte; n=2, hartinfarct; n=1, revascularisatie van been; n=1).
Individuele RCT’s
In drie studies werden resultaten gerapporteerd die niet zijn geïncludeerd in een van de meta-analyses. Reden hiervoor is het presenteren van niet-normaal verdeelde data (Szymczak, 2016), of het betreft studies die resultaten rapporteren op een bepaalde uitkomstmaat (Van Schaardenburgh, 2017) of bepaalde follow-up (Ritti-Dias, 2010). De resultaten van de drie studies worden hieronder narratief beschreven.
Szymczak et al.
De studie van Szymczak et al. rapporteerde data over fysiek functioneren na drie maanden (gemeten als functionele loopafstand en maximale loopafstand met de loopbandtest, en pijnvrije loopafstand en totale loopafstand met de 6MWT). Alle data worden gepresenteerd als mediaan ± range vanwege een niet-normale verdeling van de data (zie tabel 3). De studie beschrijft dat geen statistisch significante verschillen (p-waarden niet gerapporteerd) werden gevonden tussen de groepen (Szymczak, 2016). Deze bevindingen bevestigen de bevindingen van het systematische literatuuronderzoek dat ook niet-significante verschillen op fysiek functioneren liet zien.
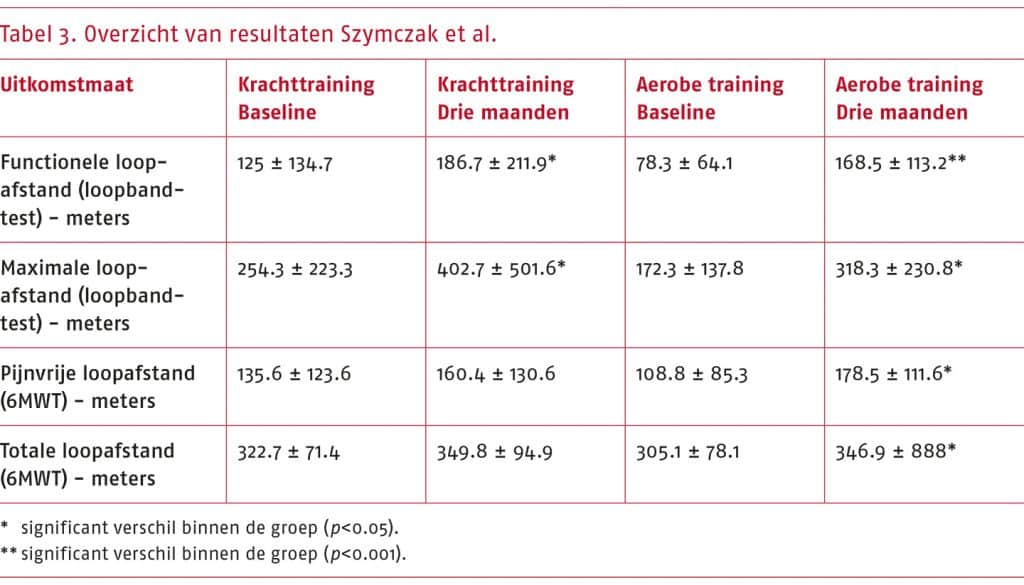
Van Schaardenburgh et al.
De studie van Van Schaardenburgh et al. rapporteerde data over kwaliteit van leven en fysiek functioneren na acht weken (gemeten als pijnvrije loopafstand en maximale loopafstand met de 6MWT voor fysiek functioneren, en met de SF-36 voor kwaliteit van leven). Alle data worden gepresenteerd als gemiddelde ± SEM (zie tabel 4). P-waarden van verschillen tussen groepen worden niet gerapporteerd, waardoor de bevindingen niet direct vergeleken kunnen worden met de bevindingen van het systematische literatuuronderzoek (Van Schaardenburgh, 2017).
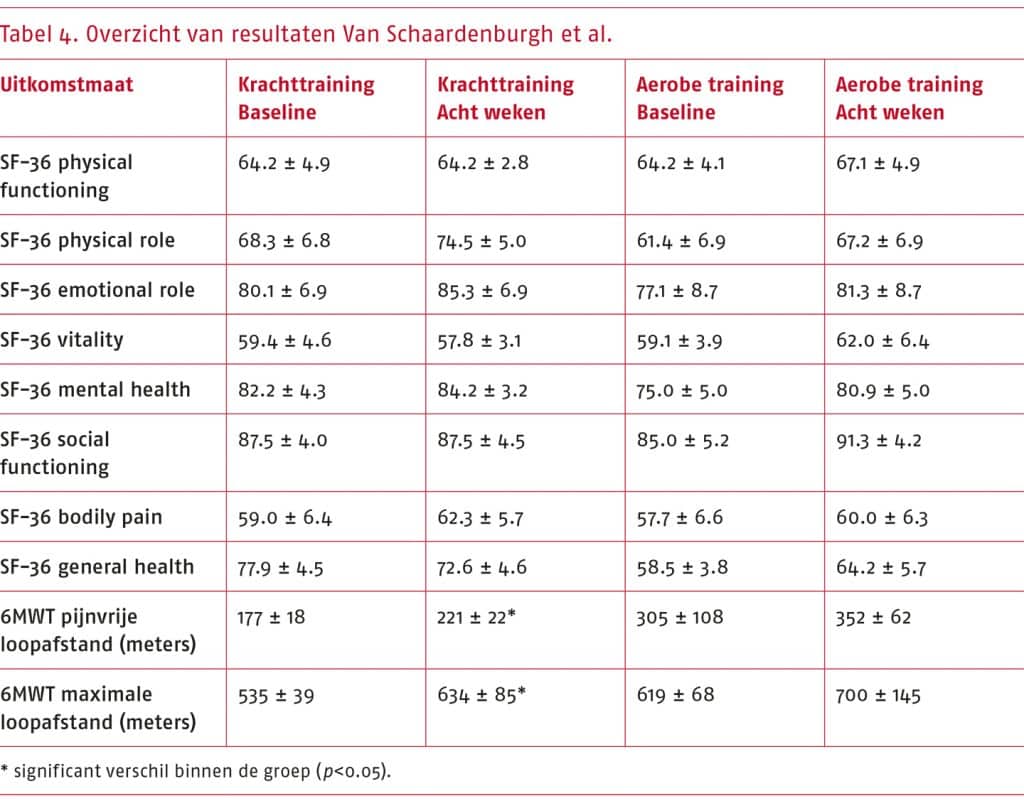
Ritti-Diaz et al.
De studie van Ritti-Diaz et al. rapporteerde resultaten over fysiek functioneren na 24 weken (gemeten als functionele loopafstand en maximale loopafstand met de loopbandtest), na een periode van twaalf weken krachttraining of aerobe training. Data worden gepresenteerd als gemiddelde ± SD (zie tabel 5). P-waarden van verschillen tussen groepen worden niet gerapporteerd, waardoor de bevindingen niet direct vergeleken kunnen worden met de bevindingen van het systematische literatuuronderzoek (Ritti-Dias, 2010).
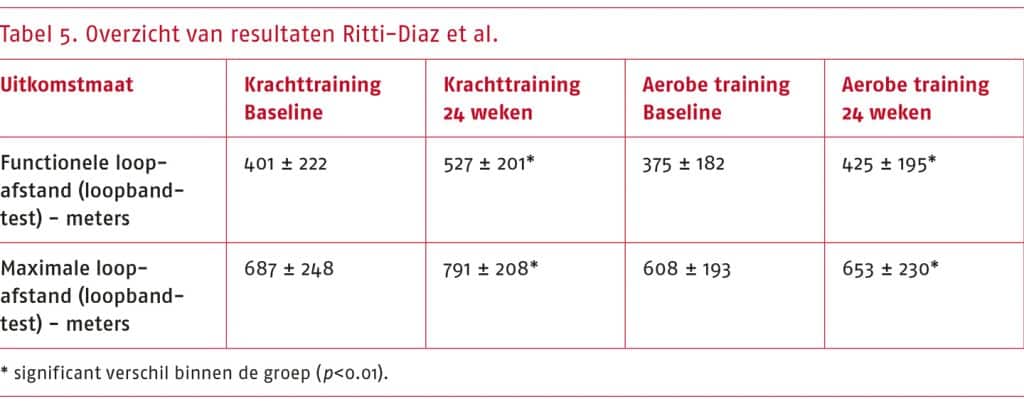
Van bewijs naar aanbeveling
Criteria
Het onderdeel van bewijs naar aanbeveling bevat negen criteria, die hieronder worden opgesomd.
Gewenste effecten
Een overzicht van de resultaten uit de systematische literatuuranalyse wordt weergegeven in tabel 6. Zowel in de resultaten van de literatuuranalyse als in de resultaten van de individuele RCT’s worden tegengestelde effecten gevonden. Echter, alle gevonden verschillen tussen de groepen zijn niet-significant.
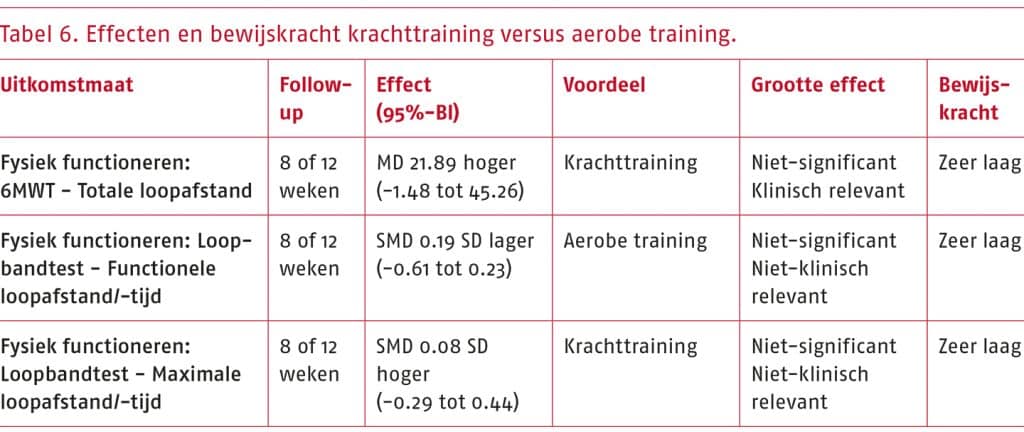
De werkgroep beoordeelt de gewenste effecten op het fysiek functioneren en de kwaliteit van leven van krachttraining ten opzichte van aerobe training voor patiënten met sPAV als niet-significant en niet-klinisch relevant. De werkgroep geeft, op basis van de bevindingen, aan dat het aannemelijk is dat zowel het inzetten van krachttraining als het inzetten van aerobe training waardevolle gewenste effecten heeft om het fysiek functioneren en de kwaliteit van leven van patiënten met sPAV te verbeteren.
Ongewenste effecten
De werkgroep beoordeelt de kans op ongewenste effecten van krachttraining ten opzichte van aerobe training voor patiënten met sPAV als klein. Alhoewel slechts één van de vier studies informatie rapporteert over ongewenste effecten, beoordeelt de werkgroep dat zowel het uitvoeren van krachttraining als het uitvoeren van aerobe training voor patiënten met sPAV veilig is. De studie rapporteert geen verschillen tussen krachttraining en aerobe training op het gebied van ongewenste effecten.
Door Gommans et al. is in een systematisch literatuuronderzoek onderzoek gedaan naar de veiligheid van gesuperviseerde beweeginterventies bij patiënten met sPAV, waarbij werd gekeken naar de complicatieratio (aantal ongewenste effecten per aantal trainingsuren) (Gommans, 2015). Deze systematische review includeerde 74 artikelen (zowel artikelen met aerobe training als interventie als artikelen met krachttraining als interventie) en rapporteerde een complicatieratio van één ongewenst voorval per 10.340 trainingsuren. Gommans et al. concluderen dat gesuperviseerde beweeginterventies veilig zijn voor patiënten met sPAV met een buitengewoon lage complicatieratio. De werkgroep beoordeelt dat deze studie aantoont dat trainen met begeleiding van een fysio- of oefentherapeut, onafhankelijk of het krachttraining of aerobe training betreft, veilig en daarmee verantwoord is.
De werkgroep wil benadrukken dat iedere patiënt zorgvuldige monitoring en daarmee een bepaalde mate van begeleiding van een fysio- of oefentherapeut moet krijgen om de veiligheid te kunnen garanderen. Dit kan variëren van trainen met supervisie in de praktijkruimte van de therapeut, tot zelfstandig trainen met supervisie van de therapeut op afstand.
Kwaliteit van bewijs
De werkgroep beoordeelt de bewijskracht van de gewenste effecten als zeer laag voor patiënten met sPAV op de uitkomst fysiek functioneren (gemeten als totale loopafstand met de 6MWT, en functionele loopafstand en maximale loopafstand met de loopbandtest). Het is hierbij van belang om rekening te houden met het feit dat de bewijskracht met name is afgewaardeerd als gevolg van de gevonden heterogeniteit in interventies en het risico op vertekening door de individuele studiekwaliteit en door de kleine onderzoekspopulaties.
Waarden en voorkeuren van patiënten
De werkgroep is tot het oordeel gekomen dat patiënten grote waarde hechten aan aerobe training, maar dat daar wel variatie in zit tussen patiënten. Er zijn patiënten die de voorkeur hebben voor krachttraining, maar er zijn ook patiënten die liever met aerobe training aan de slag gaan. Het zal per patiënt verschillend zijn wat die voorkeuren zijn.
Dit wordt ondersteund door een achterbanraadpleging (n=60 patiënten met sPAV) van Stichting Harteraad. Hoewel uit de resultaten van deze raadpleging blijkt dat 63% van de patiënten een voorkeur heeft voor aerobe training, hebben de overige patiënten of een voorkeur voor krachttraining (18%), of ze geven aan geen specifieke voorkeur te hebben (18%). Redenen waarom patiënten een voorkeur hebben voor aerobe training zijn het ervaren van een verminderde conditie of liever willen ‘bewegen’ dan aan krachttraining doen. Redenen waarom patiënten een voorkeur hebben voor krachttraining zijn de ervaring dat verbeterde spierkracht in de benen helpt om verder te kunnen lopen, de mogelijkheid om veel verschillende spiergroepen te trainen, en de motivatie door afwisseling in de oefeningen.
Balans gewenste en ongewenste effecten
De werkgroep is tot het oordeel gekomen dat de gewenste effecten van het aanbieden van krachttraining als alternatief voor aerobe training zeker de ongewenste effecten overtreffen.
De motivatie hiervoor is:
- Zowel krachttraining als aerobe training heeft een positief effect op het fysiek functioneren en de kwaliteit van leven van patiënten met sPAV. Uit de effecten en de bewijskracht vanuit de literatuur blijkt geen duidelijke voorkeur voor een van de interventies. Krachttraining is daarmee een geschikt alternatief voor aerobe training, met vergelijkbare gewenste effecten zonder relevante ongewenste effecten.
- Er zijn geen aanwijzingen dat krachttraining onveiliger is dan aerobe training bij patiënten met sPAV.
- Patiënten met sPAV hebben verschillende voorkeuren voor de trainingsvorm en hechten veel waarde aan het kunnen kiezen tussen verschillende trainingsvormen. Dit maakt dat vanuit patiëntperspectief geen generieke voorkeur bestaat voor krachttraining of aerobe training.
- De werkgroep verwacht dat het aanpassen van de trainingsvorm aan de voorkeuren van de patiënt, en dus zowel krachttraining als aerobe training aanbieden, een positieve invloed kan hebben op therapietrouw, motivatie en zelfmanagement, wat weer kan bijdragen aan mogelijk positievere effecten van training (Daley, 2003; Lin, 2019; Parfitt, 2004).
Economische overwegingen en kosteneffectiviteit
De werkgroep beoordeelt de benodigde middelen voor krachttraining ten opzichte van aerobe training als vergelijkbaar. Zowel krachttraining als aerobe training kan wisselend van aard zijn, en variëren van met supervisie trainen in een oefenruimte van de therapeut, tot zelfstandig trainen met of zonder benodigde middelen.
Gesuperviseerde beweegtraining is een aangetoond kosteneffectieve behandeling (Fokkenrood, 2014; van Asselt, 2011; van den Houten, 2016b). De werkgroep vindt het aannemelijk dat zowel krachttraining als aerobe training onder gesuperviseerde beweegtraining valt, omdat beide interventies bestaan uit trainen met een bepaalde mate van supervisie door een fysio- of oefentherapeut. De werkgroep beoordeelt beide interventies qua kosteneffectiviteit dan ook gelijk aan elkaar.
De werkgroep beoordeelt dat het aanbieden van krachttraining naast aerobe training geen directe economische impact heeft. Het kiezen voor krachttraining of aerobe training zal volgens de werkgroep geen invloed hebben op het aantal therapieafspraken en voor de invulling van de interventie bestaat geen economisch gewin op zorgkosten.
De werkgroep verwacht dat economische overwegingen vanuit de patiënt mogelijk invloed hebben op de keuze voor de trainingsvorm. Zo zijn aan aerobe training in de buitenlucht weinig financiële middelen verbonden, terwijl een lidmaatschap bij een sportschool om op een loopband of hometrainer te trainen, wel een investering vereist. Ook krachttraining kan variëren van kosteloze interventies (functionele krachtoefeningen in thuisomgeving) tot interventies waar mogelijk een lidmaatschap aan verbonden is. Door de trainingsvorm aan te laten sluiten op de voorkeuren van de patiënt verwacht de werkgroep dat effecten van therapie mogelijk vergroot worden (door o.a. hogere motivatie en therapietrouw), wat een positief effect kan hebben op het voorkomen van invasieve behandelingen, het verlagen van zorggebruik en daarmee het beperken van zorgkosten.
Gelijkheid
De werkgroep verwacht dat het aanbieden van krachttraining naast aerobe training zal leiden tot een mogelijke toename van de gezondheidsgelijkheid.
Uit de knelpuntenanalyse onder therapeuten en uit de literatuur komt naar voren dat men bezorgd is dat het toepassen van samen beslissen (zoals het aanbieden van krachttraining naast aerobe training) een risico vormt voor de gezondheidsgelijkheid, door de gedachte dat samen beslissen meer waardevol is voor hoger opgeleide personen, die beter in staat zijn om op te komen voor hun behoeften en een hoger niveau van gezondheidsvaardigheden hebben (Coulter, 2011; Legare, 2008). Een systematic review van Durand et al. laat echter zien dat samen beslissen juist leidt tot een toename van gezondheidsgelijkheid, mits de informatievoorziening wordt aangepast aan de behoeften van de individuele patiënt (Durand, 2014).
De werkgroep is van mening dat het aanbieden van krachttraining als alternatief voor aerobe training zorgt voor een betere aansluiting van de zorg op de wensen en mogelijkheden van de individuele patiënt met sPAV (en mogelijke comorbiditeiten) en daarmee zorgt voor een betere aansluiting van de zorg op een grotere groep patiënten (inclusieve zorg).
Aanvaardbaarheid
De werkgroep verwacht dat het aanbieden van krachttraining naast aerobe training door alle belangrijke stakeholders zal worden geaccepteerd.
Ondanks dat gesuperviseerde looptraining momenteel als primaire behandeling geldt binnen de zorg voor patiënten met sPAV in Nederland, verwacht de werkgroep dat alle stakeholders de gewenste variatie die ontstaat door het aanbieden van zowel krachttraining als aerobe training, aanmoedigen.
Haalbaarheid
De implementatie van het aanbieden van krachttraining naast aerobe training wordt door de werkgroep als realistisch beoordeeld. De norm is dat een beweeginterventie wordt aangeboden waarin altijd een bepaalde mate van supervisie door een fysio-/oefentherapeut aanwezig is. Hierbij kan in samenspraak met de patiënt worden bepaald, afhankelijk van de individuele wensen en doelen, of aerobe training en/of krachttraining wordt ingezet. Het aanbieden van zowel krachttraining als aerobe training kan betekenen dat therapeuten, patiënten of andere stakeholders, zoals huisartsen en vaatchirurgen, gewoontes moeten doorbreken waarin looptraining als enige mogelijke trainingsvorm wordt gezien.
Eventuele additionele overwegingen
De werkgroep is van mening dat de volgende overwegingen ook van belang zijn bij het aanbieden van krachttraining naast aerobe training:
- Het is van belang dat de therapeut altijd samen met de patiënt de voortgang van de behandeling evalueert (door inzet van gestandaardiseerde meetinstrumenten (opent in nieuw tabblad)).
- Bij patiënten met sPAV kunnen comorbiditeiten aanwezig zijn die een beperking opleveren bij het fysiek functioneren of de trainbaarheid. Het is van belang dat de therapeut bij het aanbieden van krachttraining of aerobe training rekening houdt met andere fysio-/oefentherapeutische richtlijnen gericht op die comorbiditeiten, en rekening houdt met de mogelijkheden van de patiënt door comorbiditeiten.
- Het is van belang dat de therapeut bij het aanbieden van en voorlichten over zowel aerobe training als krachttraining rekening houdt met de behandeldoelen van de patiënt en de bijbehorende specificiteit van de training. De gekozen trainingsvorm moet afgestemd zijn op de mogelijkheden en wensen van de individuele patiënt, en moet kunnen zorgen voor de benodigde trainingsprikkel bij de patiënt zodat het boeken van progressie mogelijk is.
- Bij het aanbieden van zowel krachttraining als aerobe training blijft een belangrijke rol weggelegd voor de therapeut om ziekte-inzicht en zelfmanagement van de patiënt te bevorderen. Ook wanneer wordt gekozen voor krachttraining kan het bijvoorbeeld belangrijk zijn dat een patiënt inzicht krijgt in en ervaringen opdoet met het lopen in relatie tot ADL-activiteiten.
- Het is van belang dat patiënten positieve ervaringen opdoen met beweging. Training of beweging moet niet met tegenzin worden uitgevoerd; het streven moet zijn dat de ervaringen van patiënten met het bewegen de verwachtingen overtreffen, om zo optimale resultaten te behalen. Daarbij kan het van meerwaarde zijn om krachttraining aan te bieden naast aerobe training.
- De trainingsvorm kan altijd heroverwogen worden gedurende het behandeltraject, dit kan bijvoorbeeld afhankelijk zijn van de voortgang van de behandeling of van de voorkeuren en wensen van de patiënt..
Kennislacunes
- De kwaliteit van bewijs is grotendeels op zeer lage kwaliteit van bewijs uitgekomen. Om gericht een uitspraak te kunnen doen over de effectiviteit van krachttraining ten opzichte van aerobe training, dienen meer studies uitgevoerd te worden bij patiënten met sPAV, waarbij krachttraining wordt vergeleken met verschillende vormen van aerobe training, op uitkomstmaten zoals fysiek functioneren, kwaliteit van leven, mate van pijn, levensverwachting en arbeidsparticipatie.
Aboyans, V., Ricco, J. B., Bartelink, M. E. L., Bjorck, M., Brodmann, M., Cohnert, T., Collet, J. P., Czerny, M., De Carlo, M., Debus, S., Espinola-Klein, C., Kahan, T., Kownator, S., Mazzolai, L., Naylor, A. R., Roffi, M., Rother, J., Sprynger, M., Tendera, M., et al. (2018). 2017 ESC Guidelines on the Diagnosis and Treatment of Peripheral Arterial Diseases, in collaboration with the European Society for Vascular Surgery (ESVS): Document covering atherosclerotic disease of extracranial carotid and vertebral, mesenteric, renal, upper and lower extremity arteriesEndorsed by: the European Stroke Organization (ESO)The Task Force for the Diagnosis and Treatment of Peripheral Arterial Diseases of the European Society of Cardiology (ESC) and of the European Society for Vascular Surgery (ESVS). Eur Heart J, 39(9), 763-816. https://doi.org/10.1093/eurheartj/ehx095
Bae, E., Choi, S. E., Lee, H., Shin, G.& Kang, D. (2020). Validity of EQ-5D utility index and minimal clinically important difference estimation among patients with chronic obstructive pulmonary disease. BMC Pulm Med, 20(1), 73. https://doi.org/10.1186/s12890-020-1116-z
Bartelink, M. E. L., Elsman, B. H. P., Oostindjer, A., Stoffers, H. E. J. H., Wiersma, T. J.& Geraets, J. J. X. R. (2014). NHG-Standaard Perifeer arterieel vaatlijden. Huisarts Wet, 57(2), 81-81.
Conijn, A. P., Jonkers, W., Rouwet, E. V., Vahl, A. C., Reekers, J. A.& Koelemay, M. J. (2015). Introducing the Concept of the Minimally Important Difference to Determine a Clinically Relevant Change on Patient-Reported Outcome Measures in Patients with Intermittent Claudication. Cardiovasc Intervent Radiol, 38(5), 1112-1118. https://doi.org/10.1007/s00270-015-1060-0
Coulter, A., Collins, A.& King’s Fund, C. (2011). Making shared decision-making a reality : no decision about me, without me. King’s Fund.
Daley, A. M., IW. (2003). Preferred exercise mode and affective responses in physically active adults. Psychology of Sport and Exercise, 4(4), 347-356.
Durand, M. A., Carpenter, L., Dolan, H., Bravo, P., Mann, M., Bunn, F.& Elwyn, G. (2014). Do interventions designed to support shared decision-making reduce health inequalities? A systematic review and meta-analysis. PLoS One, 9(4), e94670. https://doi.org/10.1371/journal.pone.0094670
Elwyn, G., Durand, M. A., Song, J., Aarts, J., Barr, P. J., Berger, Z., Cochran, N., Frosch, D., Galasinski, D., Gulbrandsen, P., Han, P. K. J., Harter, M., Kinnersley, P., Lloyd, A., Mishra, M., Perestelo-Perez, L., Scholl, I., Tomori, K., Trevena, L., et al. (2017). A three-talk model for shared decision making: multistage consultation process. BMJ, 359, j4891. https://doi.org/10.1136/bmj.j4891
Farrar, J. T., Young, J. P., Jr., LaMoreaux, L., Werth, J. L.& Poole, M. R. (2001). Clinical importance of changes in chronic pain intensity measured on an 11-point numerical pain rating scale. Pain, 94(2), 149-158. https://doi.org/10.1016/S0304-3959(01)00349-9
Fokkenrood, H. J., Scheltinga, M. R., Koelemay, M. J., Breek, J. C., Hasaart, F., Vahl, A. C.& Teijink, J. A. (2014). Significant savings with a stepped care model for treatment of patients with intermittent claudication. Eur J Vasc Endovasc Surg, 48(4), 423-429. https://doi.org/10.1016/j.ejvs.2014.04.020
Gardner, A. W., Parker, D. E., Montgomery, P. S.& Blevins, S. M. (2014). Step-monitored home exercise improves ambulation, vascular function, and inflammation in symptomatic patients with peripheral artery disease: a randomized controlled trial. J Am Heart Assoc, 3(5), e001107. https://doi.org/10.1161/JAHA.114.001107
Gerhard-Herman, M. D., Gornik, H. L., Barrett, C., Barshes, N. R., Corriere, M. A., Drachman, D. E., Fleisher, L. A., Fowkes, F. G., Hamburg, N. M., Kinlay, S., Lookstein, R., Misra, S., Mureebe, L., Olin, J. W., Patel, R. A., Regensteiner, J. G., Schanzer, A., Shishehbor, M. H., Stewart, K. J., et al. (2017). 2016 AHA/ACC Guideline on the Management of Patients With Lower Extremity Peripheral Artery Disease: Executive Summary: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. Circulation, 135(12), e686-e725. https://doi.org/10.1161/CIR.0000000000000470
Gommans, L. N., Fokkenrood, H. J., van Dalen, H. C., Scheltinga, M. R., Teijink, J. A.& Peters, R. J. (2015). Safety of supervised exercise therapy in patients with intermittent claudication. J Vasc Surg, 61(2), 512-518 e512. https://doi.org/10.1016/j.jvs.2014.08.070
Higgins, J. P., Savović, J., Page, M. J., Elbers, R. G.& Sterne, J. A. (2019). Assessing risk of bias in a randomized trial. Cochrane handbook for systematic reviews of interventions, 205-228.
Langendam, M. K., T. . (2022). Toepassen GRADE voor interventies tool. https://nl.gradeworkinggroup.org/docs/Tool_GRADE_voor_interventies_juni2022_final.pdf
Legare, F., Ratte, S., Gravel, K.& Graham, I. D. (2008). Barriers and facilitators to implementing shared decision-making in clinical practice: update of a systematic review of health professionals’ perceptions. Patient Educ Couns, 73(3), 526-535. https://doi.org/10.1016/j.pec.2008.07.018
Lin, E., Nguyen, C. H.& Thomas, S. G. (2019). Completion and adherence rates to exercise interventions in intermittent claudication: Traditional exercise versus alternative exercise – a systematic review. Eur J Prev Cardiol, 26(15), 1625-1633. https://doi.org/10.1177/2047487319846997
McDermott, M. M., Tian, L., Criqui, M. H., Ferrucci, L., Conte, M. S., Zhao, L., Li, L., Sufit, R., Polonsky, T. S., Kibbe, M. R., Greenland, P., Leeuwenburgh, C.& Guralnik, J. M. (2021). Meaningful change in 6-minute walk in people with peripheral artery disease. J Vasc Surg, 73(1), 267-276 e261. https://doi.org/10.1016/j.jvs.2020.03.052
Meneses, A. L., de Lima, G. H., Forjaz, C. L., Lima, A. H., Silva, G. Q., Cucato, G. G., Rodrigues, S. L., Wolosker, N., Marucci Mde, F.& Dias, R. M. (2011). Impact of a supervised strength training or walking training over a subsequent unsupervised therapy period on walking capacity in patients with claudication. J Vasc Nurs, 29(2), 81-86. https://doi.org/10.1016/j.jvn.2011.01.002
Merry, A. H. H., Teijink, J. A. W., Jongert, M. W. A., Poelgeest, A., Van Der Voort, S. S. E. M., Bartelink, M. E. L., Stoffers, H. E. J. H., Brooymans, F., Hendriks, H. J. M.& De Bie, R. A. (2014). KNGF-richtlijn Symptomatisch perifeer arterieel vaatlijden. www.kngfrichtlijnen.nl.
Nordanstig, J., Pettersson, M., Morgan, M., Falkenberg, M.& Kumlien, C. (2017). Assessment of Minimum Important Difference and Substantial Clinical Benefit with the Vascular Quality of Life Questionnaire-6 when Evaluating Revascularisation Procedures in Peripheral Arterial Disease. Eur J Vasc Endovasc Surg, 54(3), 340-347. https://doi.org/10.1016/j.ejvs.2017.06.022
Parfitt, G. G., C. (2004). The effect of choice of exercise mode on psychological responses. Psychology of Sport and Exercise, 5(2), 111-117.
Ritti-Dias, R. M., Wolosker, N., de Moraes Forjaz, C. L., Carvalho, C. R., Cucato, G. G., Leao, P. P.& de Fatima Nunes Marucci, M. (2010). Strength training increases walking tolerance in intermittent claudication patients: randomized trial. J Vasc Surg, 51(1), 89-95. https://doi.org/10.1016/j.jvs.2009.07.118
Sawilowsky, S. (2009). New Effect Size Rules of Thumb. Journal of Modern Applied Statistical Methods, 8(2).
Society for Vascular Surgery Lower Extremity Guidelines Writing, G., Conte, M. S., Pomposelli, F. B., Clair, D. G., Geraghty, P. J., McKinsey, J. F., Mills, J. L., Moneta, G. L., Murad, M. H., Powell, R. J., Reed, A. B., Schanzer, A., Sidawy, A. N.& Society for Vascular, S. (2015). Society for Vascular Surgery practice guidelines for atherosclerotic occlusive disease of the lower extremities: management of asymptomatic disease and claudication. J Vasc Surg, 61(3 Suppl), 2S-41S. https://doi.org/10.1016/j.jvs.2014.12.009
Stiggelbout, A. M., Pieterse, A. H.& De Haes, J. C. (2015). Shared decision making: Concepts, evidence, and practice. Patient Educ Couns, 98(10), 1172-1179. https://doi.org/10.1016/j.pec.2015.06.022
Szymczak, M., Oszkinis, G.& Majchrzycki, M. (2016). The Impact of Walking Exercises and Resistance Training upon the Walking Distance in Patients with Chronic Lower Limb Ischaemia. Biomed Res Int, 2016, 7515238. https://doi.org/10.1155/2016/7515238
van Asselt, A. D., Nicolai, S. P., Joore, M. A., Prins, M. H., Teijink, J. A.& Exercise Therapy in Peripheral Arterial Disease Study, G. (2011). Cost-effectiveness of exercise therapy in patients with intermittent claudication: supervised exercise therapy versus a ‘go home and walk’ advice. Eur J Vasc Endovasc Surg, 41(1), 97-103. https://doi.org/10.1016/j.ejvs.2010.06.024
van den Houten, M. M., Gommans, L. N., van der Wees, P. J.& Teijink, J. A. (2016a). Minimally Important Difference of the Absolute and Functional Claudication Distance in Patients with Intermittent Claudication. Eur J Vasc Endovasc Surg, 51(3), 404-409. https://doi.org/10.1016/j.ejvs.2015.11.008
van den Houten, M. M., Lauret, G. J., Fakhry, F., Fokkenrood, H. J., van Asselt, A. D., Hunink, M. G.& Teijink, J. A. (2016b). Cost-effectiveness of supervised exercise therapy compared with endovascular revascularization for intermittent claudication. Br J Surg, 103(12), 1616-1625. https://doi.org/10.1002/bjs.10247
van der Horst, D. E. M., Garvelink, M. M., Bos, W. J. W., Stiggelbout, A. M.& Pieterse, A. H. (2023). For which decisions is Shared Decision Making considered appropriate? – A systematic review. Patient Educ Couns, 106, 3-16. https://doi.org/10.1016/j.pec.2022.09.015
Van Schaardenburgh, M., Wohlwend, M., Rognmo, O.& Mattsson, E. (2017). Calf raise exercise increases walking performance in patients with intermittent claudication. J Vasc Surg, 65(5), 1473-1482. https://doi.org/10.1016/j.jvs.2016.12.106
Wyrwich, K. W., Tierney, W. M., Babu, A. N., Kroenke, K.& Wolinsky, F. D. (2005). A comparison of clinically important differences in health-related quality of life for patients with chronic lung disease, asthma, or heart disease. Health Serv Res, 40(2), 577-591. A comparison of clinically important differences in health-related quality of life for patients with chronic lung disease, asthma, or heart disease – PubMed
Zatloukal, J., Ward, S., Houchen-Wolloff, L., Harvey-Dunstan, T.& Singh, S. (2019). The minimal important difference for the endurance shuttle walk test in individuals with chronic obstructive pulmonary disease following a course of pulmonary rehabilitation. Chronic Respiratory Disease, 16. https://doi.org/10.1177/1479973119853828
Auteurs | Ontwikkeling modules C.8 Samen beslissen
Betrokkenheid van belanghebbenden (auteurs)
De projectgroep van de KNGF-richtlijnmodules (Koninklijk Nederlands Genootschap Fysiotherapie) ‘Samen beslissen voor de KNGF-richtlijn symptomatisch Perifeer Arterieel Vaatlijden (sPAV)’ (hierna genoemd ‘Samen beslissen voor de KNGF-richtlijn sPAV’) werd gevormd door de kerngroep, de werkgroep en de klankbordgroep. De kerngroep bestond uit richtlijnadviseurs, beleidsmedewerkers en inhoudsdeskundige wetenschappers. De werkgroep en klankbordgroep van de richtlijnmodules bestonden uit een afvaardiging van inhoudsdeskundige wetenschappers, vertegenwoordiging vanuit het werkveld fysio- en oefentherapie en medici, en vertegenwoordiging van patiënten. De rollen en taken van de belanghebbenden van de richtlijn worden beschreven in de ‘KNGF-richtlijnenmethodiek 2022 ’ (KNGF, 2022).
Patiëntenperspectief en voorkeuren
Gedurende het richtlijnproject zijn de perspectieven, ervaringen, verwachtingen en voorkeuren van patiënten zorgvuldig en meermaals nagegaan en meegewogen. Naast deelname van Stichting Harteraad aan de werkgroep namen Patiëntenfederatie Nederland en Pharos Expertisecentrum Gezondheidsverschillen deel aan de klankbordgroep.
In de voorbereidende fase heeft Stichting Harteraad knelpunten vanuit de zorggebruikers opgehaald. Deze knelpunten zijn in de knelpunteninventarisatie meegewogen bij het vormgeven van het raamwerk. Ook is deze informatie meegenomen in de verdere ontwikkeling van de richtlijnmodules bij onder meer het bepalen van de belangrijkste uitkomstmaten, het beschrijven en wegen van de verschillende overwegingen en het formuleren van de aanbevelingen.
Belangenverstrengeling
Voorafgaand aan en bij afsluiting van het project hebben alle kern-, werk- en klankbordgroepleden een belangenverklaring ingevuld. De belangenverklaringen zijn beoordeeld door de richtlijnadviseurs en indien nodig (bij een ‘conflict of interest’) werden gedurende het richtlijnproject maatregelen getroffen (bijvoorbeeld het niet participeren in het proces ‘van bewijs naar aanbeveling’ in de werk- of klankbordgroep) om (schijn van) oneigenlijke beïnvloeding door belangenverstrengeling zo veel mogelijk te voorkomen, conform de ‘KNGF-richtlijnenmethodiek 2022 (opent in nieuw tabblad)’ (KNGF, 2022).
In de belangenverklaringen is een overzicht opgenomen met de affiliaties (de organisatie of instelling en plaats van de werkzaamheden) van de leden van de projectgroep.
Ontwikkeling
Jaarlijks beoordelen de betrokken inhoudelijk experts (dr. T.J. Hoogeboom en het KNGF) of herziening van de richtlijnmodules noodzakelijk is op basis van inhoudelijke en/of beleidsmatige ontwikkelingen.
Ontwikkeling van de huidige richtlijnmodules heeft modulair plaatsgevonden, conform de ‘KNGF-richtlijnenmethodiek 2022’ (opent in nieuw tabblad) (KNGF, 2022).
Voorbereidingsfase (inclusief knelpuntenanalyse)
De eerste stap in de ontwikkeling van de richtlijnmodules was het samenstellen van de kerngroep, werkgroep en klankbordgroep met daarin vertegenwoordiging van de relevante partijen.
De tweede stap was het uitvoeren van de knelpuntenanalyse gericht op samen beslissen. De knelpuntenanalyse kreeg vorm door raadpleging van fysio- en oefentherapeuten, patiënten en stakeholders die voor de richtlijnmodules relevant zijn. Daarnaast werden de werkgroep en de klankbordgroep systematisch bevraagd en werd vanuit de literatuur (geaggregeerde) informatie over het onderwerp van de richtlijn verzameld. Op basis van de opgehaalde informatie werden knelpunten met betrekking tot samen beslissen geïnventariseerd, opgesteld en geanalyseerd, die zo de basis vormden voor de geprioriteerde uitgangsvragen van de richtlijn.
De activiteiten en methoden die de kerngroep van de KNGF-richtlijnmodules ‘Samen beslissen voor de KNGF-richtlijn sPAV’ heeft geselecteerd voor de knelpuntenanalyse, werden afgestemd op de inhoud van de betreffende richtlijnmodules en de beschikbaarheid van de partijen binnen de looptijd van de voorbereidingsfase. De knelpuntenanalyse bestond uit: 1) een focusgroepbijeenkomst met fysio- en oefentherapeuten, 2) een patiëntenraadpleging, 3) een schriftelijke knelpuntenanalyse, 4) een werkgroepbijeenkomst, 5) een klankbordgroepbijeenkomst, en 6) oriënterend literatuuronderzoek.
De voorbereidingsfase, waarin de knelpuntenanalyse heeft plaatsgevonden, vond plaats tussen oktober 2022 en maart 2023.
Ontwikkelfase
Tijdens de ontwikkelfase heeft één werkgroepbijeenkomst plaatsgevonden, waarin de overwegingen zijn besproken en de aanbevelingen zijn geformuleerd. Daarnaast heeft de klankbordgroep feedback gegeven op de conceptmodules.
De ontwikkelfase vond plaats tussen september 2023 en februari 2024.
Commentaarfase en autorisatiefase
In de commentaarfase zijn de conceptrichtlijnmodules ter commentaar verzonden naar fysio- en oefentherapeuten uit het werkveld. Daarnaast worden deze verzonden naar de partijen die aan de ontwikkeling van de richtlijnmodules hebben bijgedragen of voorafgaand aan het traject aangegeven hebben betrokken te willen worden in de commentaarfase. De richtlijnmodules zijn in een werkveldronde voorgelegd aan fysio- en oefentherapeuten die betrokken zijn bij de zorg voor de patiëntengroep waarop de richtlijnmodules zijn gericht. De verzamelde commentaren zijn samengevoegd in een commentarentabel, die is voorgelegd aan de werkgroep. De werkgroep heeft bepaald welke aanpassingen en/of aanvullingen in de conceptrichtlijnmodules vereist dan wel gewenst waren. De klankbordgroep heeft hierin geadviseerd. Na vaststelling door de werkgroep en de klankbordgroep zijn de richtlijnmodules ter autorisatie voorgelegd aan alle betrokken partijen.
De commentaar- en autorisatiefase vonden plaats tussen februari 2024 en juni 2024.
Disseminatiefase en implementatiefase
Na publicatie van de richtlijnmodules worden diverse implementatieproducten opgeleverd, waaronder:
- patiënteninformatie;
- stappenplan;
- scholing;
- informatievideo’s;
- artikelen in tijdschriften (zowel binnen als buiten de fysio- en oefentherapie, nationaal en internationaal);
- lezingen op congressen en symposia.
De implementatiefase vindt plaats tussen september 2024 en 2025.
De belangrijkste kernonderwerpen vanuit de richtlijnmodules voor de implementatie van samen beslissen in algemene zin zijn:
- Bewustwording en kennis bij fysio– en oefentherapeuten over wat samen beslissen wel is en wat het niet is;
- De bereidheid en vaardigheid bij fysio– en oefentherapeuten om samen beslissen toe te passen in het werkveld.
De belangrijkste kernonderwerpen vanuit de richtlijnmodules voor de implementatie van samen beslissen tussen therapeut en patiënt met sPAV zijn:
- De keuze voor looptraining of andere vormen van beweeginterventies;
- De keuze voor gesuperviseerde of zelfstandig uitgevoerde beweeginterventies;
- De keuze voor pijnvrije of niet-pijnvrije looptraining;
- De keuze voor aerobe training of krachttraining.
De belangrijkste kernonderwerpen over het toevoegen van de module samen beslissen aan de KNGF-richtlijn sPAV zijn:
Kennis van de richtlijnmethodiek van de KNGF-richtlijn sPAV en de nieuwe module over samen beslissen.
Kennislacunes

